Detemir: ຄຳ ແນະ ນຳ ສຳ ລັບການ ນຳ ໃຊ້, analogues
ຕາຕະລາງ 1. ປ່ຽນນ້ ຳ ໜັກ ຂອງຮ່າງກາຍໃນໄລຍະການປິ່ນປົວດ້ວຍ insulin
| ໄລຍະເວລາການສຶກສາ | Insulin detemir ຄັ້ງດຽວ | Insulin detemir ສອງຄັ້ງ | ອິນຊູລິນ Isulin | Insulin glargine |
| 20 ອາທິດ | + 0,7 ກກ | + 1,6 ກກ | ||
| 26 ອາທິດ | + 1,2 ກກ | + 2.8 ກກ | ||
| 52 ອາທິດ | + 2,3 ກກ | + 3,7 ກ | + 4,0 ກກ |
ໃນການສຶກສາ, ການໃຊ້ວິທີການປິ່ນປົວແບບປະສົມປະສານກັບ Levemir ® FlexPen ®ແລະຢາລະລາຍໃນເລືອດຫຼຸດລົງຄວາມສ່ຽງໃນການພັດທະນາການເປັນໂລກເບົາຫວານໃນຕອນກາງຄືນໂດຍ 61–65%, ແຕກຕ່າງຈາກ isofan-insulin.
ການທົດລອງທາງຄລີນິກແບບເປີດເຜີຍແບບສຸ່ມໄດ້ຖືກ ດຳ ເນີນໂດຍຜູ້ປ່ວຍທີ່ເປັນໂລກເບົາຫວານປະເພດ 2 ທີ່ບໍ່ໄດ້ບັນລຸລະດັບ glycemic ຂອງພວກເຂົາຕາມເປົ້າ ໝາຍ ດ້ວຍການປິ່ນປົວດ້ວຍການລະລາຍຂອງປາກ.
ການສຶກສາໄດ້ເລີ່ມຕົ້ນດ້ວຍໄລຍະເວລາກຽມຕົວປະມານ 12 ອາທິດ, ໃນໄລຍະທີ່ຄົນເຈັບໄດ້ຮັບການປິ່ນປົວແບບປະສົມປະສານກັບ liraglutide ໃນການປະສົມປະສານກັບ metformin, ແລະຕໍ່ຕ້ານທີ່ 61% ຂອງຜູ້ປ່ວຍບັນລຸ HbA1 ຄ® FlexPen ®ໃນປະລິມານປະ ຈຳ ວັນດຽວ, ຄົນເຈັບຄົນອື່ນຍັງສືບຕໍ່ໄດ້ຮັບທາດແຫຼວໃນປະສົມກັບ metformin ໃນ 52 ອາທິດຕໍ່ໄປ. ໃນລະຫວ່າງໄລຍະເວລານີ້, ກຸ່ມ ບຳ ບັດ, ຜູ້ທີ່ໄດ້ຮັບ, ນອກ ເໜືອ ຈາກ liraglutide ກັບ metformin, ການສັກຢາປະ ຈຳ ວັນດຽວຂອງ Levemir ® FlexPen daily, ໄດ້ສະແດງໃຫ້ເຫັນເຖິງການຫຼຸດລົງຂອງດັດຊະນີ HbA ຕື່ມອີກ1 ຄ ຈາກເບື້ອງຕົ້ນ 7,6% ຫາ 7.1% ໃນຕອນທ້າຍຂອງໄລຍະເວລາ 52 ອາທິດ, ໃນກໍລະນີທີ່ບໍ່ມີພາວະໂລກເອດສ໌ໃນລະດັບສູງ. ໂດຍການເພີ່ມປະລິມານຂອງຢາ Levemir ® FlexPen ®ເພື່ອການປິ່ນປົວດ້ວຍການຮັກສາທາດແຫຼວ, ຜົນໄດ້ຮັບສຸດທ້າຍໄດ້ຮັກສາຄຸນປະໂຫຍດທີ່ກ່ຽວຂ້ອງກັບການຫຼຸດຜ່ອນນ້ ຳ ໜັກ ຮ່າງກາຍໃນຄົນເຈັບທີ່ມີສະຖິຕິ, ເບິ່ງຕາຕະລາງ 2.
ຕາຕະລາງ 2 ຂໍ້ມູນການທົດລອງທາງດ້ານການຊ່ວຍ - ການປິ່ນປົວດ້ວຍ Levemir ®, ຖືກ ກຳ ນົດນອກ ເໜືອ ຈາກລະບອບການປິ່ນປົວແບບປະສົມປະສານກັບ liraglutide ກັບ metformin
| ອາທິດຂອງການຮັກສາ | ຜູ້ປ່ວຍໄດ້ຮັບການສຸ່ມເພື່ອຮັບການປິ່ນປົວດ້ວຍ Levemir ® FlexPen ®ນອກເຫນືອຈາກ liraglutide + metformin N = 160 | ຄົນເຈັບໄດ້ຮັບການສຸ່ມເພື່ອຮັບການປິ່ນປົວດ້ວຍທາດແຫຼວ liraglutide + ການປິ່ນປົວດ້ວຍ metformin N = 149 | ຕົວຄູນຄວາມ ໜ້າ ເຊື່ອຖືຂອງການປ່ຽນແປງ P-value | |
| ການປ່ຽນແປງສະເລ່ຍຂອງມູນຄ່າຂອງຕົວຊີ້ວັດ HbA1 ຄ ເມື່ອທຽບກັບຈຸດເລີ່ມຕົ້ນຂອງການທົດສອບ (%) | 0–26 | - 0,51 | + 0,02 | |
| 0–52 | - 0,50 | 0,01 | ||
| ອັດຕາສ່ວນຂອງຄົນເຈັບທີ່ບັນລຸມູນຄ່າເປົ້າ ໝາຍ ຂອງ HbA1 ຄ0–26 | 43,1 | 16,8 | ||
| 0–52 | 51,9 | 21,5 | ||
| ການປ່ຽນແປງນ້ ຳ ໜັກ ໃນຮ່າງກາຍຂອງຄົນເຈັບເມື່ອທຽບໃສ່ກັບຕົວຊີ້ວັດໃນຈຸດເລີ່ມຕົ້ນຂອງການທົດສອບ (ກິໂລ) | 0–26 | - 0,16 | - 0,95 | 0,0283 |
| 0–52 | - 0,05 | - 1,02 | 0,0416 | |
| ພະຍາດເບົາຫວານໃນລະດັບອ່ອນໆ (ໃນປະລິມານຂອງ 0 ຄົນເຈັບປີຂອງການ ສຳ ຜັດກັບຢາທົດລອງ) | 0–26 | 0,286 | 0,029 | 0,0037 |
| 0–52 | 0,228 | 0,034 | 0,0011 |
ໃນການສຶກສາໄລຍະຍາວ (months 6 ເດືອນ) ທີ່ກ່ຽວຂ້ອງກັບຄົນເຈັບທີ່ເປັນໂຣກເບົາຫວານປະເພດ 1, ຄວາມເຂັ້ມຂົ້ນຂອງ plasma glucose ແມ່ນດີກວ່າເມື່ອທຽບໃສ່ກັບການຮັກສາດ້ວຍ Levemir ® FlexPen ®ເມື່ອທຽບກັບ isofan-insulin ທີ່ຖືກ ກຳ ນົດໃນການປິ່ນປົວພື້ນຖານ / bolus. ການຄວບຄຸມ Glycemic (HbA1 ຄ) ໃນໄລຍະການຮັກສາດ້ວຍ Levemir ® FlexPen ®ທຽບກັບກັບ isofan-insulin, ແຕ່ມີຄວາມສ່ຽງຕ່ ຳ ໃນການເປັນໂລກເບົາຫວານໃນຕອນກາງຄືນແລະບໍ່ມີການເພີ່ມນ້ ຳ ໜັກ ໃນຮ່າງກາຍກັບ Levemir ® FlexPen ®.
ຜົນໄດ້ຮັບຂອງການສຶກສາທາງດ້ານການຊ່ວຍປະເມີນລະບົບການປິ່ນປົວອິນຊູລິນເຊິ່ງເປັນຕົວຊີ້ບອກໃຫ້ເຫັນການເກີດຂື້ນຂອງໂລກເອດສໃນເລືອດໂດຍທົ່ວໄປໃນໄລຍະການປິ່ນປົວດ້ວຍ Levemir ® FlexPen ®ແລະ isofan-insulin. ການວິເຄາະກ່ຽວກັບການພັດທະນາຂອງການເປັນໂລກເບົາຫວານໃນກະດູກສັນຫຼັງໃນຄົນເຈັບທີ່ເປັນໂລກເບົາຫວານປະເພດ 1 ໄດ້ສະແດງໃຫ້ເຫັນວ່າມີການຂາດນ້ ຳ ຕານໃນເລືອດຕໍ່າໂດຍການ ນຳ ໃຊ້ Levemir ® FlexPen independently (ໃນເວລາທີ່ຄົນເຈັບສາມາດ ກຳ ຈັດຄວາມດັນເລືອດໃນເລືອດ ໜ້ອຍ ລົງ). , 8 mmol / L ຫຼືຜົນຂອງການວັດແທກຄວາມເຂັ້ມຂົ້ນຂອງນ້ ຳ ຕານໃນ plasma ໃນເລືອດຕ່ ຳ ກ່ວາ 3,1 mmol / L), ທຽບໃສ່ກັບວ່າເມື່ອໃຊ້ isofan-insulin, ໃນຂະນະທີ່ ລະຫວ່າງກິນຢາສອງສຶກສາບໍ່ໄດ້ເປີດເຜີຍໃຫ້ເຫັນຄວາມແຕກຕ່າງໃນຄວາມຖີ່ຂອງການປະກົດຕົວຂອງ episodes ຂອງປອດ hypoglycemia nocturnal ໃນຄົນເຈັບທີ່ມີພະຍາດເບົາຫວານປະເພດ 2.
ຂໍ້ມູນຂອງ glycemia ໃນຕອນກາງຄືນແມ່ນ flatter ແລະຍິ່ງໄປກວ່ານັ້ນກັບ Levemir ® FlexPen ®ເມື່ອທຽບກັບ isofan-insulin, ເຊິ່ງສະທ້ອນໃຫ້ເຫັນເຖິງຄວາມສ່ຽງຕ່ ຳ ໃນການພັດທະນາການເປັນໂລກເບົາຫວານໃນຕອນກາງຄືນ.
ໃນເວລາທີ່ໃຊ້ Levemir P FlexPen ®, ການຜະລິດພູມຕ້ານທານໄດ້ຖືກສັງເກດເຫັນ. ເຖິງຢ່າງໃດກໍ່ຕາມ, ຄວາມຈິງນີ້ບໍ່ມີຜົນຕໍ່ການຄວບຄຸມ glycemic.
ການຖືພາ
ໃນການທົດລອງທາງດ້ານຄລີນິກແບບຄວບຄຸມແບບສຸ່ມ, ເຊິ່ງລວມມີແມ່ຍິງຖືພາ 310 ຄົນທີ່ເປັນໂລກເບົາຫວານປະເພດ 1, ປະສິດທິພາບແລະຄວາມປອດໄພຂອງ Levemir ® FlexPen ®ໃນລະດັບພື້ນຖານ (ຄົນເຈັບ 152 ຄົນ) ໄດ້ຖືກປຽບທຽບກັບທາດ isofan-insulin (158 ຄົນເຈັບ) ໃນ ປະສົມປະສານກັບ insulin aspart, ຖືກນໍາໃຊ້ເປັນ insulin prandial.
ຜົນຂອງການສຶກສາໄດ້ສະແດງໃຫ້ເຫັນວ່າໃນຄົນເຈັບທີ່ໄດ້ຮັບຢາ Levemir ® FlexPen ®, ການຫຼຸດລົງທີ່ຄ້າຍຄືກັນໄດ້ຖືກສັງເກດເຫັນເມື່ອປຽບທຽບກັບກຸ່ມທີ່ໄດ້ຮັບສານ isofan-insulin HbA1 ຄ ໃນ 36 ອາທິດຂອງການ gestation. ກຸ່ມຄົນເຈັບທີ່ໄດ້ຮັບການປິ່ນປົວດ້ວຍ Levemir ® FlexPen ®, ແລະກຸ່ມທີ່ໄດ້ຮັບການປິ່ນປົວດ້ວຍ isofan-insulin, ຕະຫຼອດໄລຍະເວລາການສະແດງອອກ, ໄດ້ສະແດງໃຫ້ເຫັນຄວາມຄ້າຍຄືກັນໃນຂໍ້ມູນລວມຂອງ HbA1 ຄ.
ລະດັບ HbA ເປົ້າ ໝາຍ1 ຄ .0 6.0% ໃນອາທິດທີ່ 24 ແລະ 36 ຂອງການຖືພາບັນລຸໄດ້ 41% ຂອງຄົນເຈັບໃນກຸ່ມການປິ່ນປົວດ້ວຍ Levemir ® FlexPen and ແລະໃນ 32% ຂອງຄົນເຈັບໃນກຸ່ມການປິ່ນປົວດ້ວຍ isofan-insulin.
ຄວາມເຂັ້ມຂົ້ນຂອງລະດັບນ້ ຳ ຕານໃນເວລາ 24 ແລະ 36 ອາທິດຂອງການມີເພດ ສຳ ພັນແມ່ນມີສະຖິຕິຕ່ ຳ ຫຼາຍໃນກຸ່ມແມ່ຍິງທີ່ກິນຢາ Levemir-FlexPen ®ເມື່ອທຽບກັບກຸ່ມທີ່ໄດ້ຮັບການປິ່ນປົວດ້ວຍ isofan-insulin.
ໃນຊ່ວງໄລຍະເວລາທັງ ໝົດ ຂອງການຖືພາ, ບໍ່ມີຄວາມແຕກຕ່າງທີ່ມີຄວາມ ໝາຍ ທາງສະຖິຕິລະຫວ່າງຄົນເຈັບທີ່ໄດ້ຮັບສານ Levemir ® FlexPen ®ແລະ isofan-insulin ໃນເຫດການທີ່ເກີດຂື້ນໃນລະດັບໂລກເອດສໃນເລືອດ.
ທັງສອງກຸ່ມຂອງແມ່ຍິງຖືພາທີ່ໄດ້ຮັບການປິ່ນປົວດ້ວຍ Levemir ® FlexPen ®ແລະ isofan-insulin ໄດ້ສະແດງໃຫ້ເຫັນຜົນໄດ້ຮັບທີ່ຄ້າຍຄືກັນໃນການເກີດເຫດການທີ່ບໍ່ດີໃນລະຫວ່າງການຖືພາທັງ ໝົດ ຂອງພວກເຂົາ, ເຖິງຢ່າງໃດກໍ່ຕາມ, ມັນພົບວ່າໃນແງ່ປະລິມານການເກີດຂອງເຫດການທີ່ຮ້າຍແຮງໃນຄົນເຈັບ ອາຍຸການຖືພາທັງ ໝົດ (61 (40%) ທຽບກັບ 49 (31%)), ໃນເດັກນ້ອຍໃນຊ່ວງໄລຍະການພັດທະນາພາຍໃນແລະຫຼັງເກີດ (36 (24%) ທຽບກັບ 32 (20%)) ແມ່ນສູງກວ່າກຸ່ມການປິ່ນປົວດ້ວຍ Levemir ir Fle Spenny ®ເມື່ອທຽບກັບກຸ່ມການປິ່ນປົວດ້ວຍ isophane insulin ໄດ້.
ຈຳ ນວນເດັກທີ່ມີຊີວິດຈາກແມ່ທີ່ຖືພາຫລັງຈາກຖືກສຸ່ມເຂົ້າໄປໃນກຸ່ມປິ່ນປົວເພື່ອຮັບການປິ່ນປົວດ້ວຍ ໜຶ່ງ ໃນຢາທີ່ໄດ້ຮັບການທົດສອບແມ່ນ 50 (83%) ໃນກຸ່ມການປິ່ນປົວ Levemir ® FlexPen and ແລະ 55 (89%) ໃນກຸ່ມປິ່ນປົວ isofan ອິນຊູລິນ. ຈຳ ນວນເດັກນ້ອຍທີ່ເກີດມາເປັນໂຣກຜິດປົກກະຕິໃນການເກີດແມ່ນ 4 (5%) ໃນກຸ່ມປິ່ນປົວ Levemir-FlexPen and ແລະ 11 (7%) ໃນກຸ່ມປິ່ນປົວ isofan-insulin. ໃນ ຈຳ ນວນດັ່ງກ່າວ, ໂຣກຜິດປົກກະຕິໃນທ້ອງເກີດຂື້ນຢ່າງຮ້າຍແຮງໄດ້ຖືກສັງເກດເຫັນໃນເດັກນ້ອຍ 3 (4%) ໃນກຸ່ມປິ່ນປົວ Levemir-FlexPen and ແລະ 3 (2%) ໃນກຸ່ມປິ່ນປົວ isofan-insulin.
ເດັກນ້ອຍແລະໄວລຸ້ນ
ປະສິດທິພາບແລະຄວາມປອດໄພຂອງການໃຊ້ Levemir ® FlexPen ®ໃນເດັກນ້ອຍໄດ້ຖືກສຶກສາໃນການທົດລອງທາງຄລີນິກທີ່ຄວບຄຸມເປັນເວລາ 12 ເດືອນໂດຍມີໄວລຸ້ນແລະເດັກນ້ອຍອາຍຸສອງປີທີ່ທົນທຸກຈາກໂຣກເບົາຫວານປະເພດ 1 (ຄົນເຈັບທັງ ໝົດ 694 ຄົນ), ໜຶ່ງ ໃນການສຶກສານີ້ ຈຳ ນວນເດັກນ້ອຍທັງ ໝົດ 82 ຄົນທີ່ເປັນໂລກເບົາຫວານປະເພດ 1 ໃນກຸ່ມອາຍຸສອງຫາຫ້າປີ. ຜົນໄດ້ຮັບຂອງການສຶກສາເຫຼົ່ານີ້ໄດ້ສະແດງໃຫ້ເຫັນວ່າການຄວບຄຸມ glycemic (HbA1 ຄ) ຕໍ່ກັບຄວາມເປັນມາຂອງການປິ່ນປົວດ້ວຍ Levemir ® FlexPen ®ທຽບເທົ່າກັບການປິ່ນປົວທີ່ມີ isofan-insulin, ໂດຍການນັດພົບຂອງພວກເຂົາໃນພື້ນຖານຂອງການປິ່ນປົວດ້ວຍ bolus. ນອກຈາກນັ້ນ, ຍັງມີຄວາມສ່ຽງຕ່ ຳ ໃນການພັດທະນາການລະລາຍນ້ ຳ ຕານໃນເລືອດ (ອີງຕາມຄຸນຄ່າຂອງ plasma glucose ທີ່ຖືກວັດແທກໂດຍຄົນເຈັບດ້ວຍຕົວເອງ) ແລະການຂາດນ້ ຳ ໜັກ ຂອງຮ່າງກາຍ (ການບ່ຽງເບນມາດຕະຖານ ສຳ ລັບນ້ ຳ ໜັກ ຂອງຮ່າງກາຍໄດ້ຖືກປັບຕາມເພດແລະອາຍຸຂອງຄົນເຈັບ) ໃນລະຫວ່າງການຮັກສາດ້ວຍ Levemir ® Flexpen®, ໃນການສົມທຽບກັບ isofan-insulin.
ໜຶ່ງ ໃນການສຶກສາທາງຄລີນິກໄດ້ຖືກຂະຫຍາຍໄປອີກ 12 ເດືອນ (ຂໍ້ມູນທາງຄລີນິກໄດ້ຮັບທັງ ໝົດ 24 ເດືອນ) ເພື່ອໃຫ້ໄດ້ຖານຂໍ້ມູນທີ່ສົມບູນກວ່າເກົ່າ ສຳ ລັບການປະເມີນການສ້າງຕັ້ງພູມຕ້ານທານໃນຄົນເຈັບຕໍ່ກັບການປິ່ນປົວໄລຍະຍາວກັບ Levemir ® FlexPen ®.
ຜົນໄດ້ຮັບທີ່ໄດ້ຮັບໃນລະຫວ່າງການສຶກສາຊີ້ໃຫ້ເຫັນວ່າໃນໄລຍະປີ ທຳ ອິດຂອງການຮັກສາໃນຂະນະທີ່ກິນຢາ Levemir ® FlexPen was, ມີການເພີ່ມຂື້ນຂອງລະດັບຂອງພູມຕ້ານທານຕໍ່ສານລະລາຍອິນຊູລິນ, ເຖິງຢ່າງໃດກໍ່ຕາມ, ໃນທ້າຍປີທີ 2 ຂອງການປິ່ນປົວ, ລະດັບຂອງການສ້າງພູມຕ້ານທານຕໍ່ Levemir ® FlexPen ®ຫຼຸດລົງໃນຄົນເຈັບ ລະດັບທີ່ເກີນຂັ້ນ ໜຶ່ງ ເລັກນ້ອຍໃນເວລາເລີ່ມຕົ້ນການປິ່ນປົວດ້ວຍ Levemir ir FlexPen ®. ດັ່ງນັ້ນ, ມັນໄດ້ຖືກພິສູດວ່າການສ້າງຕັ້ງພູມຕ້ານທານໃນຄົນເຈັບທີ່ເປັນໂຣກເບົາຫວານໃນເວລາປິ່ນປົວກັບ Levemir ® FlexPen ®ບໍ່ມີຜົນກະທົບຕໍ່ລະດັບການຄວບຄຸມ glycemic ແລະປະລິມານຂອງ insulin detemir.
ແພດການຢາ
ການດູດຊືມ
ຄວາມເຂັ້ມຂົ້ນຂອງ plasma ສູງສຸດແມ່ນບັນລຸ 6-8 ຊົ່ວໂມງຫຼັງຈາກການບໍລິຫານ.
ດ້ວຍລະບຽບການບໍລິຫານປະ ຈຳ ວັນສອງຄັ້ງ, ຄວາມເຂັ້ມຂຸ້ນຂອງຢາທີ່ມີຄວາມສົມດຸນໃນ plasma ໃນເລືອດແມ່ນບັນລຸໄດ້ຫຼັງຈາກສັກ 2-3 ຄັ້ງ.
ຕົວປ່ຽນແປງຂອງການດູດຊືມໃນລະດັບຕໍ່າແມ່ນຕໍ່າກວ່າ ສຳ ລັບ Levemir-FlexPen ®ເມື່ອທຽບກັບການກະກຽມອິນຊູລິນອື່ນໆ. ບໍ່ມີຄວາມແຕກຕ່າງລະຫວ່າງຍິງ - ຊາຍທີ່ມີຄວາມແຕກຕ່າງທາງດ້ານການແພດໃນຮ້ານຂາຍຢາຂອງ Levemir ® FlexPen ®.
ການແຈກຢາຍ
ການແຈກຢາຍໂດຍສະເລ່ຍຂອງ Levemir ® FlexPen ® (ປະມານ 0.1 L / kg) ສະແດງໃຫ້ເຫັນວ່າອັດຕາສ່ວນຂອງ insulin ສູງທີ່ໄຫລວຽນຢູ່ໃນເລືອດ.
ການເຜົາຜານອາຫານ
ການບໍ່ມີປະສິດຕິຜົນຂອງຢາ Levemir ® FlexPen similar ແມ່ນຄ້າຍຄືກັບການກະກຽມອິນຊູລິນຂອງມະນຸດ, ທາດແປ້ງທັງ ໝົດ ທີ່ສ້າງຂຶ້ນແມ່ນບໍ່ມີປະໂຫຍດ. ການສຶກສາຜູກມັດໂປຣຕີນ ໃນ vitro ແລະ ໃນ vivo ສະແດງໃຫ້ເຫັນການບໍ່ມີປະຕິກິລິຍາທີ່ ສຳ ຄັນທາງຄລີນິກລະຫວ່າງ insulin detemir ແລະກົດໄຂມັນຫຼືຢາອື່ນໆທີ່ຜູກພັນກັບໂປຣຕີນ.
ການປັບປຸງພັນ
ໄລຍະເວລາເຄິ່ງຊີວິດຫຼັງຈາກການສັກຢາ subcutaneous ແມ່ນຖືກ ກຳ ນົດໂດຍລະດັບຂອງການດູດຊຶມຈາກເນື້ອເຍື່ອ subcutaneous ແລະແມ່ນ 5-7 ຊົ່ວໂມງ, ຂື້ນກັບປະລິມານ.
Linearity
ດ້ວຍການບໍລິຫານ subcutaneous, ຄວາມເຂັ້ມຂຸ້ນຂອງ plasma ແມ່ນອັດຕາສ່ວນກັບປະລິມານທີ່ໃຫ້ບໍລິຫານ (ຄວາມເຂັ້ມຂົ້ນສູງສຸດ, ລະດັບຂອງການດູດຊຶມ).
ບໍ່ມີການພົວພັນທາງດ້ານ pharmacokinetic ຫຼື pharmacodynamic ລະຫວ່າງ liraglutide ແລະຢາ Levemir ® FlexPen in, ໃນຄວາມສົມດຸນ, ໂດຍມີການບໍລິຫານພ້ອມໆກັນກັບຄົນເຈັບທີ່ມີຢາເສບຕິດໂລກເບົາຫວານຊະນິດ 2 Levemir ® FlexPen dose ໃນປະລິມານດຽວ 0.5 U / kg ແລະ liraglutide 1.8 ມລກ.
ກຸ່ມຄົນເຈັບພິເສດ
ຄຸນລັກສະນະທາງດ້ານ pharmacokinetic ຂອງ Levemir ® FlexPen ®ໄດ້ຖືກສຶກສາໃນເດັກນ້ອຍ (ເດັກອາຍຸ 6 and12 ປີ) ແລະໄວລຸ້ນ (ອາຍຸ 13-17 ປີ) ແລະສົມທຽບກັບຄຸນສົມບັດທາງ pharmacokinetic ໃນຜູ້ໃຫຍ່ທີ່ເປັນໂລກເບົາຫວານປະເພດ 1. ບໍ່ພົບຄວາມແຕກຕ່າງ. ມັນບໍ່ມີຄວາມແຕກຕ່າງທີ່ ສຳ ຄັນທາງຄລີນິກຂອງຢາ ບຳ ລຸງຮັກສາຂອງ Levemir-FlexPen ®ລະຫວ່າງຄົນເຈັບຜູ້ເຖົ້າແລະຄົນ ໜຸ່ມ, ຫລືລະຫວ່າງຄົນເຈັບທີ່ມີຄວາມບົກຜ່ອງໃນການເຮັດວຽກຂອງເນື້ອງອກແລະຕັບອັກເສບແລະຄົນເຈັບທີ່ມີສຸຂະພາບແຂງແຮງ.
ການສຶກສາຄວາມປອດໄພ Preclinical
ການຄົ້ນຄ້ວາ ໃນ vitro, ໃນສາຍເຊວຂອງມະນຸດ, ລວມທັງການສຶກສາກ່ຽວກັບການຜູກກັບຕົວຮັບອິນຊູລິນແລະ IGF-1 (ປັດໄຈການຈະເລີນເຕີບໂຕທີ່ຄ້າຍຄືກັບອິນຊູລິນ), ໄດ້ສະແດງໃຫ້ເຫັນວ່າສານອິນຊູລິນມີຄວາມ ສຳ ພັນຕໍ່າຕໍ່ທັງສອງຕົວຮັບແລະມີຜົນກະທົບ ໜ້ອຍ ຕໍ່ການຈະເລີນເຕີບໂຕຂອງເຊນທຽບກັບອິນຊູລິນ. ຂໍ້ມູນ Preclinical ໂດຍອີງໃສ່ການສຶກສາປົກກະຕິກ່ຽວກັບຄວາມປອດໄພທາງດ້ານ pharmacological, ຄວາມເປັນພິດຂອງຢາຊ້ ຳ ໆ , ເຊື້ອໂຣກ genotoxicity, ຄວາມເປັນໄປໄດ້ຂອງມະເລັງ, ຜົນກະທົບທີ່ເປັນພິດຕໍ່ ໜ້າ ທີ່ການຈະເລີນພັນ, ບໍ່ໄດ້ເປີດເຜີຍອັນຕະລາຍໃດໆຕໍ່ມະນຸດ.
ວິທີການປິ່ນປົວນີ້ແມ່ນຫຍັງ?

ການ ນຳ ໃຊ້ເຕັກໂນໂລຢີການແນະ ນຳ DNA ແບບທັນສະ ໄໝ ໄດ້ຊ່ວຍນັກວິທະຍາສາດຫຼາຍຄັ້ງໃນການເພີ່ມປະສິດທິພາບຂອງຕົວແທນທີ່ມີອິນຊູລິນປົກກະຕິ.
ການແກ້ໄຂການສີດແບບ Detemir ຖືກສ້າງຂື້ນໂດຍໃຊ້ວິທີການໃນການປຸງແຕ່ງທາງຊີວະວິທະຍາຂອງຕ່ອງໂສ້ DNA ທີ່ໃຊ້ແລ້ວ.
ສາຍພັນຂອງ Saccharomyces cerevisiae ຖືກ ນຳ ໃຊ້ - ນີ້ແມ່ນຕົວຢ່າງພື້ນຖານຂອງທາດອິນຊູລິນຍາວຂອງມະນຸດ, ເຊິ່ງບໍ່ມີກິດຈະ ກຳ ສູງສຸດໃນຮູບແບບການກະ ທຳ.
Detemir ແມ່ນການແກ້ໄຂທີ່ມີ pH ທີ່ເປັນກາງ, ມັນມີຄວາມໂປ່ງໃສແລະບໍ່ມີສີ. ຕົວແທນຕ້ານໂຣກເບົາຫວານນີ້ເປັນຂອງ insulins ທີ່ໃຊ້ໄດ້ດົນນານ. ໃນຕະຫຼາດ, insemir insulin ແມ່ນຖືກຂາຍພາຍໃຕ້ຊື່ Levimir.
ການຫຸ້ມຫໍ່ເບິ່ງຄືວ່ານີ້: ໃນຮ້ານຂາຍຢາ, ມັນຖືກຂາຍໃນຮູບແບບຂອງຕະຫລັບຫມຶກ, ໃນແຕ່ລະຜະລິດຕະພັນຂອງພວກມັນ 0,4242 ມລກຂອງ detemir. ໂດຍສະເລ່ຍ, ການຫຸ້ມຫໍ່ມີລາຄາປະມານ 3,000 ຮູເບີນ. ຢາຊະນິດນີ້ມີຂາຍຄືກັນກັບປະເພດຢາອິນຊູລິນຊະນິດອື່ນໆ.
ເນື້ອແທ້ຂອງການກະ ທຳ ຂອງ Detemir
Detemir ເຮັດໄດ້ກວ້າງກວ່າ insulin glargine ແລະ isofan. ຜົນກະທົບໃນໄລຍະຍາວຂອງຕົວແທນນີ້ແມ່ນເນື່ອງມາຈາກການມີສ່ວນຮ່ວມໃນຕົວເອງທີ່ສົດໃສຂອງໂຄງສ້າງໂມເລກຸນແລະການສົມທົບຂອງພວກມັນກັບລະບົບຕ່ອງໂສ້ອາຊິດໄຂມັນຂ້າງກັບໂມເລກຸນ albumin. ເມື່ອທຽບໃສ່ກັບ insulins ອື່ນໆ, detemir ກະແຈກກະຈາຍຊ້າລົງທົ່ວຮ່າງກາຍ. ກົນໄກການເຮັດວຽກດັ່ງກ່າວຍືດເຍື້ອການເຄື່ອນໄຫວຂອງຢາ, ແລະຊ່ວຍເພີ່ມການດູດຊືມຂອງມັນ.
ນອກຈາກນີ້, ບໍ່ຄືກັບວິທີອື່ນ, insulin ນີ້ສາມາດຄາດເດົາໄດ້ຫຼາຍ, ສະນັ້ນມັນງ່າຍຕໍ່ການຄວບຄຸມຜົນຂອງມັນ.
ນີ້ແມ່ນຍ້ອນປັດໃຈຫຼາຍຢ່າງ:
- Detemir ຍັງຄົງຢູ່ໃນສະພາບຄ່ອງຈາກການຢູ່ໃນ ampoule ຈົນເຖິງເວລາທີ່ຕົວແທນຖືກ ນຳ ເຂົ້າສູ່ຮ່າງກາຍ,
- ອະນຸພາກຂອງມັນຖືກຜູກມັດກັບໂມເລກຸນຂອງແບນໃນລະດັບເລືອດໂດຍວິທີການປ້ອງກັນ.
ເຄື່ອງມືດັ່ງກ່າວພົວພັນກັບເຄື່ອງຮັບພາຍນອກທີ່ຕັ້ງຢູ່ເຍື່ອຫ້ອງ cytoplasmic. ສະລັບສັບຊ້ອນ insulin-receptor ໄດ້ຖືກສ້າງຂື້ນເຊິ່ງກະຕຸ້ນຫຼັກສູດຂອງຂະບວນການ intracellular. ມີການສັງເຄາະ glycogen synthetase, hexokinase ແລະ pyruvate kinase.
ຄວາມເຂັ້ມຂົ້ນຂອງທາດປະລິມານນ້ ຳ ຕານຫຼຸດລົງເນື່ອງຈາກການຂົນສົ່ງນ້ ຳ ຕານເພີ່ມຂື້ນພາຍໃນຈຸລັງ, ມັນເລີ່ມດູດຊືມເຂົ້າໄປໃນເນື້ອເຍື່ອຕ່າງໆໄດ້ດີຂື້ນ. Glycogenogenesis ແລະ lipogenesis ກໍ່ໄດ້ຮັບການປັບປຸງ. ຕັບເລີ່ມຜະລິດນ້ ຳ ຕານຫຼາຍຊ້າ.
ຕົວແທນນີ້ມີຜົນກະທົບ ໜ້ອຍ ຕໍ່ອັດຕາການຈະເລີນເຕີບໂຕຂອງເຊນກ່ວາ insulins ອື່ນໆ. ມັນບໍ່ມີຜົນກະທົບທີ່ເປັນມະເລັງ, ສານພິດແລະຢາ genotoxic ໃນ ໜ້າ ທີ່ຂອງຮ່າງກາຍທັງ ໝົດ, ລວມທັງເພດ.
ຄຸນສົມບັດ Kinetic ຂອງຕົວແທນ
ຫຼັງຈາກການແນະ ນຳ ສານ detemir ເຂົ້າສູ່ຮ່າງກາຍ, ມັນຈະເຂັ້ມຂຸ້ນຫຼາຍທີ່ສຸດໃນທາດແຫຼວ plasma ພາຍຫຼັງ 7 ຊົ່ວໂມງ. ຖ້າຄົນເຈັບໄດ້ຮັບການສັກຢາສອງຄັ້ງຕໍ່ມື້, ຫຼັງຈາກນັ້ນ, ສະພາບ glycemic ຄົງຕົວພາຍຫຼັງການປິ່ນປົວດ້ວຍສອງສາມມື້. ໃນເວລາທີ່ຫຼາຍກ່ວາ 3 ມລກຖືກສັກເຂົ້າໄປໃນຮ່າງກາຍ, prologue ຂອງການປະຕິບັດແມ່ນປະມານ 15 ຊົ່ວໂມງແລະປະສິດທິພາບສູງສຸດແມ່ນບັນລຸໄດ້ຫຼັງຈາກ 2 ຊົ່ວໂມງ.
ເນື່ອງຈາກວ່າ detemir ມີການແຈກຢາຍທີ່ດີ, ມັນໄຫຼວຽນຢູ່ໃນເລືອດໃນປະລິມານທີ່ ສຳ ຄັນ.

ມັນແມ່ນ metabolized ເກືອບທັງຫມົດ, ແລະ metabolites ທັງຫມົດແມ່ນປອດໄພສໍາລັບຮ່າງກາຍ. ເຄິ່ງຊີວິດຂອງຢາແຕກຕ່າງກັນໄປຕາມປະລິມານທີ່ໃຊ້ກັບຄົນເຈັບ. ໂດຍສະເລ່ຍ, ມັນແມ່ນ 6 ຊົ່ວໂມງ.
ຄຳ ແນະ ນຳ ສຳ ລັບການ ນຳ ໃຊ້
ປະລິມານທີ່ ຈຳ ເປັນ ສຳ ລັບຄົນເຈັບແມ່ນຖືກເລືອກເປັນສ່ວນບຸກຄົນ. Detemir ສາມາດປະຕິບັດໄດ້ 1-2 ຄັ້ງຕໍ່ມື້. ຖ້າ detemir ໄດ້ຖືກກໍານົດເພື່ອເພີ່ມປະສິດທິພາບການຄວບຄຸມ glycemia, ຢາດັ່ງກ່າວແມ່ນໃຊ້ສອງຄັ້ງ. ປະລິມານ 1 ຄັ້ງແມ່ນໃຫ້ກິນໃນຕອນເຊົ້າ, ແລະ 2 ຕອນແລງກ່ອນເຂົ້ານອນຫຼືຫຼັງ 12 ຊົ່ວໂມງຫຼັງຈາກສັກຕອນເຊົ້າ.
ຄົນເຈັບທີ່ມີອາຍຸຕ່ ຳ ກວ່າ 50 ປີແລະທຸກທໍລະມານຈາກໂຣກຕັບຫລື ໝາກ ໄຂ່ຫຼັງທີ່ບໍ່ ຈຳ ເປັນຕ້ອງເລືອກຢ່າງລະມັດລະວັງ. ນອກຈາກນັ້ນ, ພວກເຂົາຕ້ອງໄດ້ຮັບການຕິດຕາມກວດກາຢ່າງບໍ່ຢຸດຢັ້ງກ່ຽວກັບນ້ ຳ ຕານໃນເລືອດ.
ການສັກຢາອິນຊູລິນ (Detemir) ການສັກຢາອິນຊູລິນແມ່ນຖືກຈັດໃສ່ໃນບໍລິເວນບ່າ, ຂາ, ຫຼືພື້ນທີ່ຂອງບໍລິເວນ ໜ້າ ທ້ອງ. ຄວາມເຂັ້ມຂອງການກະ ທຳ (ການດູດຊຶມ) ຂອງຢາຈະຂື້ນກັບສະຖານທີ່ສັກຢາ. ຖ້າການສັກຢາຢູ່ໃນພື້ນທີ່ ໜຶ່ງ, ສະຖານທີ່ສັກເຂັມຕ້ອງມີການປ່ຽນແປງໃນແຕ່ລະພາກ. ນີ້ແມ່ນເນື່ອງມາຈາກຄວາມຈິງທີ່ວ່າ lipodystrophy ສາມາດເກີດຂື້ນໄດ້ - ເຫຼົ່ານີ້ແມ່ນໂກນດອກທີ່ມີຄ່າ, ເຊິ່ງຫຼັງຈາກນັ້ນມັນຍາກທີ່ຈະກໍາຈັດ.
ກະລຸນາສັງເກດ: ຖ້າ insulin ຖືກສັກເຂົ້າໄປໃນກະເພາະອາຫານ, ຫຼັງຈາກນັ້ນທ່ານຈໍາເປັນຕ້ອງຖອກ 5 ຊມຈາກສາຍບືແລະ stab ໃນວົງມົນ.
ມັນມີຄວາມ ສຳ ຄັນຫຼາຍທີ່ຈະສັກຢາໃຫ້ຖືກຕ້ອງ. ສຳ ລັບສິ່ງນີ້ທ່ານຈະຕ້ອງການ: insulin ອຸນຫະພູມໃນຫ້ອງ (ເອົາລົງໃນເວລາເຄິ່ງຊົ່ວໂມງ), ເຂັມສັກຢາ (ຖ້າ ຈຳ ເປັນ), ຢາຕ້ານເຊື້ອແລະຝ້າຍຝ້າຍ.
ຍິ່ງໄປກວ່ານັ້ນ, ທຸກສິ່ງທຸກຢ່າງແມ່ນເຮັດໄດ້ໂດຍອີງຕາມລະບົບ:
- ສະຖານທີ່ໄດ້ຮັບການຮັກສາດ້ວຍຢາຕ້ານເຊື້ອ, ສ່ວນທີ່ເຫຼືອຂອງມັນຕ້ອງແຫ້ງໃນຜິວ,
- ຜິວຫນັງໄດ້ຖືກຈັບໃນເພີ່ມທະວີຂຶ້ນ
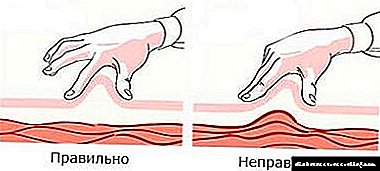
- ເຂັມຖືກໃສ່ຢູ່ໃນມຸມ. ບໍ່ແມ່ນແຮງຊຸກດັນທີ່ແຂງແຮງ, ຫຼັງຈາກນັ້ນ, ກະບອກສູບຍືດອອກໄປ ໜ້ອຍ ໜຶ່ງ. ຖ້າທ່ານຕີເຮືອ, ຫຼັງຈາກນັ້ນທ່ານຈໍາເປັນຕ້ອງປ່ຽນສະຖານທີ່ສັກຢາ.
- ທາດແຫຼວຖືກແນະ ນຳ ເທື່ອລະກ້າວແລະວັດແທກ. ຖ້າຫາກວ່າ piston ບໍ່ເຄື່ອນທີ່ດີ, ຜິວ ໜັງ ທີ່ຢູ່ເທິງເຂັມຈະໃຄ່ບວມແລະເຈັບ - ທ່ານ ຈຳ ເປັນຕ້ອງຍູ້ເຂັມເລິກກວ່າ.
- ຫຼັງຈາກສັກຢາອິນຊູລິນ, ທ່ານ ຈຳ ເປັນຕ້ອງປ່ອຍເຂັມພາຍໃຕ້ຜິວ ໜັງ ປະມານ 4-6 ວິນາທີ. ຫຼັງຈາກນີ້, ເຂັມຖືກຖອດອອກດ້ວຍການເຄື່ອນໄຫວທີ່ແຫຼມ, ສະຖານທີ່ສີດກໍ່ຖືກຖູອີກເທື່ອ ໜຶ່ງ ດ້ວຍຢາຂ້າເຊື້ອ.
ເພື່ອເຮັດໃຫ້ການສີດບໍ່ເຈັບປວດເທົ່າທີ່ຈະເປັນໄປໄດ້, ຄວນເລືອກເຂັມທີ່ສັ້ນແລະອ່ອນກວ່າ, ເມື່ອມີຮອຍຫ່ຽວ, ຢ່າບີບຜິວໃຫ້ ແໜ້ນ, ປາດດ້ວຍມືທີ່ ໝັ້ນ ໃຈ.
ທີ່ ສຳ ຄັນ! ຖ້າຄົນເຈັບສັກຢາອິນຊູລິນຫຼາຍໆຊະນິດ, ທ່ານຕ້ອງກົດສັ້ນ, ແລະຫຼັງຈາກນັ້ນກໍ່ຍາວ.
ສິ່ງທີ່ຕ້ອງຊອກຫາກ່ອນເຂົ້າກອງທຶນ?
ກ່ອນທີ່ທ່ານຈະສັກຢາ, ທ່ານຕ້ອງ:
- ກວດຄືນປະເພດສິນຄ້າ
- ຂ້າເຊື້ອເຍື່ອຢາງໂດຍໃຊ້ເຫຼົ້າຫຼືຢາຂ້າເຊື້ອໂລກອີກຊະນິດ ໜຶ່ງ,
- ກວດຄືນຄວາມສົມບູນຂອງລົດເຂັນ. ຖ້າມັນຖືກ ທຳ ລາຍພາຍນອກຫຼືສ່ວນທີ່ເບິ່ງເຫັນຂອງເຍື່ອເກີນຄວາມກວ້າງຂອງແຖບສີຂາວ, ມັນບໍ່ສາມາດໃຊ້ໄດ້ແລະຕ້ອງຖືກສົ່ງກັບໄປຮ້ານຂາຍຢາ.
ກະລຸນາຮັບຊາບວ່າສານອິນຊູລິນທີ່ເກັບໄວ້ໃນເມື່ອກ່ອນຫຼືຖືກເກັບຮັກສາໄວ້ບໍ່ຖືກຕ້ອງ, ເຄື່ອງຕອງທີ່ມີທາດແຫຼວທີ່ມີເມກແລະສີພາຍໃນບໍ່ຄວນໃຊ້. ຢາ Detemir ບໍ່ຄວນໃຊ້ໃນຈັກສູບນ້ ຳ ອິນຊູລິນ.
ເມື່ອສັກ, ທ່ານຕ້ອງປະຕິບັດຕາມກົດລະບຽບເຫຼົ່ານີ້:
- ຢາເສບຕິດໄດ້ຖືກປະຕິບັດພຽງແຕ່ subcutaneously.
- ຫຼັງຈາກສັກແຕ່ລະຄັ້ງ, ປ່ຽນເຂັມ (ຖ້າໃຊ້ອິນຊູລິນໃນ ampoule), ເພາະວ່າຜະລິດຕະພັນດັ່ງກ່າວອາດຈະຮົ່ວໄຫຼຍ້ອນການເພີ່ມຂື້ນຂອງອຸນຫະພູມ.
- ໄສ້ຕອງບໍ່ສາມາດເຕີມເງິນໄດ້. ຂັ້ນຕອນນີ້ແມ່ນເປັນໄປໄດ້ພຽງແຕ່ໃຊ້ເຂັມທີ່ໃຊ້ແລ້ວ.
ຢາເກີນປະລິມານ
ໃນຢາ, ແນວຄວາມຄິດຂອງການກິນຢາອິນຊູລິນຫຼາຍເກີນໄປແມ່ນບໍ່ໄດ້ສ້າງຕັ້ງຂື້ນ. ໃນເວລາດຽວກັນ, ໃນເວລາທີ່ຄົນເຈັບກິນປະລິມານທີ່ສູງກ່ວາທີ່ລາວຖືກເກັບ, ລາວພັດທະນາຮູບພາບທາງຄລີນິກທີ່ມີທາດ ນຳ ້ຕານໃນເລືອດ (ຄວາມເຂັ້ມຂົ້ນຂອງນ້ ຳ ຕານ ໜ້ອຍ ເກີນໄປ).
ຄົນເຈັບມີອາການດັ່ງຕໍ່ໄປນີ້:
- Pallor

- ເຕົ່າ
- Tinnitus
- ການສູນເສຍຄວາມເຂັ້ມຂົ້ນ
- ຄວາມຮູ້ສຶກຂອງອາການປວດຮາກ
- ຄຸນນະພາບຂອງການເບິ່ງເຫັນຫຼຸດລົງຢ່າງຫຼວງຫຼາຍ,
- ຄວາມກັງວົນໃຈແລະຄວາມບໍ່ມີໃຈ.
ໂດຍປົກກະຕິຄົນເຈັບຈະເຈັບປ່ວຍຢ່າງກະທັນຫັນ. ການສະແດງທີ່ບໍ່ດີຂອງສະພາບການນີ້ສາມາດລົບລ້າງໄດ້ໂດຍການກິນນ້ ຳ ຕານ ໜ້ອຍ ໜຶ່ງ ຫຼືຜະລິດຕະພັນນ້ ຳ ຕານອື່ນໆ. ມີຢາຄຸມ ກຳ ເນີດຊະນິດພິເສດທີ່ຊ່ວຍແກ້ໄຂບັນຫາໂລກເບົາຫວານບໍ່ໄດ້.
ໃນກໍລະນີທີ່ຮຸນແຮງ, ປະລິມານນ້ ຳ ຕານຫຼຸດລົງເປັນສິ່ງ ສຳ ຄັນທີ່ຄົນເຈັບອາດຈະຕົກຢູ່ໃນສະພາບ glycemic.
ສະພາບການນີ້ແມ່ນປະກອບດ້ວຍສັນຍານ:
- ສະຕິເສີຍ
- ວິນຫົວ
- ຄວາມບົກຜ່ອງດ້ານການປາກເວົ້າ
- ການປະສານງານທີ່ບໍ່ດີ
- ຄວາມຮູ້ສຶກທີ່ເຂັ້ມແຂງຂອງຄວາມຢ້ານກົວພາຍໃນ.
ການລະບາດໃນເລືອດຕ່ ຳ ຢ່າງຮຸນແຮງແມ່ນໄດ້ຮັບການຮັກສາດ້ວຍການສັກຢາ intramuscular ຫຼື subcutaneous 1 mg ຂອງ glucagon. ຖ້າຮ່າງກາຍຂອງມະນຸດບໍ່ຕອບສະ ໜອງ ກັບການສີດດັ່ງກ່າວໃນທາງໃດກໍ່ຕາມພາຍໃນ 20 ນາທີ, ວິທີແກ້ໄຂທາດນ້ ຳ ຕານຈະຖືກປະຕິບັດໃນເສັ້ນເລືອດ. ໃນກໍລະນີທີ່ຮຸນແຮງທີ່ສຸດ, ຄົນເຈັບອາດຈະເສຍຊີວິດຫຼືເປັນໂຣກສະ ໝອງ.
ຜົນຂ້າງຄຽງ
ຮູບລັກສະນະຂອງພວກມັນໂດຍກົງແມ່ນຂື້ນກັບປະລິມານຂອງອິນຊູລິນ. ບຸກຄົນໃດ ໜຶ່ງ ອາດຈະປະສົບກັບປະຕິກິລິຍາດັ່ງກ່າວຕໍ່ Detemir:
- ການລະເມີດຂະບວນການ E -book. ຄົນເຈັບອາດຈະເປັນໂຣກກະເພາະ ລຳ ໄສ້ແລະຄວາມບໍ່ສົມດຸນຂອງສານຕ່າງໆໃນເລືອດ.
- ປະຕິກິລິຍາທົ່ວໄປແລະທ້ອງຖິ່ນຂອງຮ່າງກາຍ. ອາດຈະພໍເຫັນເທື່ອ, ຄັນ, ແລະໃຄ່ບວມ. ບາງທີການພັດທະນາຂອງ lipodystrophy ແລະ edema ໃນສ່ວນຕ່າງໆຂອງຮ່າງກາຍ.
- ລະບົບພູມຕ້ານທານ. ຄົນເຈັບບາງຄົນມີອາການແພ້, ປັດສະວະ. ປະຕິກິລິຍາແພ້ຢ່າງຮຸນແຮງສາມາດເຮັດໃຫ້ເກີດອາການປວດຫລັງຂອງ Quincke ແລະອາການແພ້ອື່ນໆທີ່ພາໃຫ້ເສຍຊີວິດ.
- ຄວາມຜິດປົກກະຕິກ່ຽວກັບການສະກັດ. ຄີຫຼັງຂອງແສງແມ່ນມີການສະທ້ອນແສງໃນທັດສະນະທີ່ບໍ່ຖືກຕ້ອງ, ເນື່ອງຈາກວ່າມີການລະເມີດທົ່ວໄປຂອງການເບິ່ງເຫັນແລະຄວາມຮັບຮູ້ຂອງສີ.
- ພະຍາດ Rhinopathic.
- ຄວາມເສຍຫາຍຕໍ່ລະບົບປະສາດສ່ວນປະກອບ, ເນື່ອງຈາກວ່າມັນມີການລະເມີດຂອງຄວາມອ່ອນໄຫວຂອງຜິວຫນັງ, ກ້າມເນື້ອຈະອ່ອນເພຍແລະບໍ່ຟັງ. ໂຣກ neuropathy ຍັງສາມາດເຈັບປວດໄດ້.

ຖ້າບຸກຄົນໃດ ໜື່ງ ມີຄວາມກົດດັນຕໍ່ບາງສ່ວນຂອງສ່ວນປະກອບຂອງ Detemir, ປະຕິກິລິຍາເຫຼົ່ານີ້ສາມາດເກີດຂື້ນໄດ້ເຖິງແມ່ນວ່າຫຼັງຈາກກິນຢານ້ອຍໆ. ພວກເຂົາຈະແຂງແຮງກວ່າຄົນເຈັບຄົນອື່ນໆ.
ດັ່ງທີ່ໄດ້ກ່າວມາແລ້ວ, detemir ສາມາດເຮັດໃຫ້ເກີດໂລກນ້ ຳ ຕານໃນເລືອດເຊິ່ງສົ່ງຜົນກະທົບຕໍ່ຄວາມເຂັ້ມຂົ້ນ. ດ້ວຍຄວາມຜິດປົກກະຕິດັ່ງກ່າວ, ແນະ ນຳ ໃຫ້ ຈຳ ກັດການຂັບຂີ່ລົດ, ຄວບຄຸມກົນໄກທີ່ສັບສົນແລະວຽກບາງປະເພດ, ເພາະວ່າມັນອາດຈະເປັນອັນຕະລາຍຕໍ່ມະນຸດ.
ໃນຜູ້ປ່ວຍບາງຄົນ, ໂຣກຕ່ ຳ ໃນເລືອດສາມາດພັດທະນາໄດ້ໂດຍບໍ່ມີອາການຫລືດ້ວຍອາການທີ່ບໍ່ສະແດງອອກ.. ຖ້າວ່າມີຄວາມສ່ຽງທີ່ຄົນເຈັບອາດຈະພັດທະນາປະກົດການນີ້ບໍ່ສະ ໝໍ່າ ສະ ເໝີ, ຄວນມີມາດຕະການເພື່ອປ້ອງກັນການຫຼຸດລົງຂອງນ້ ຳ ຕານແລະຍັງພິຈາລະນາເຖິງການແນະ ນຳ ໃຫ້ຂັບລົດແລະປະຕິບັດວຽກທີ່ເປັນອັນຕະລາຍ ສຳ ລັບໄລຍະການປິ່ນປົວ.
ມັນເປັນໄປໄດ້ ສຳ ລັບການພະຍາບານ, ແມ່ຍິງຖືພາແລະເດັກນ້ອຍບໍ?
ບໍ່ມີຄວາມແຕກຕ່າງ teratogenic ຫຼື embryotoxic ໃນເວລາທີ່ໃຊ້ insulin Detemir ແລະມະນຸດ ທຳ ມະດາ. ໃນກໍລະນີນີ້, ແມ່ຍິງຖືພາແລະຜູ້ທີ່ຢູ່ໃນໄລຍະເວລາ lactation, ໃນເວລາທີ່ດໍາເນີນການປິ່ນປົວ, ຈໍາເປັນຕ້ອງຢູ່ພາຍໃຕ້ການຊີ້ນໍາຂອງທ່ານຫມໍຢ່າງຕໍ່ເນື່ອງແລະຕິດຕາມປະລິມານນໍ້າຕານ.
ໃນແມ່ຍິງທີ່ເປັນໂຣກເບົາຫວານ, ລະດັບນ້ ຳ ຕານໃນເລືອດຂອງພວກເຂົາຈະສະຖຽນລະພາບເລັກນ້ອຍໃນ 2-3 ລຳ, ສະນັ້ນຄວາມຕ້ອງການຂອງອິນຊູລິນຫຼຸດລົງ. ເມື່ອແມ່ຍິງເກີດລູກແລະຢຸດການລ້ຽງລູກດ້ວຍນົມແມ່, ຮ່າງກາຍກໍ່ເລີ່ມຂາດອິນຊູລິນ. ສະນັ້ນທ່ານບໍ່ສາມາດປ່ອຍຢາໄດ້ຄືກັນກັບສະພາບການດັ່ງກ່າວ, ທ່ານ ຈຳ ເປັນຕ້ອງປັບຂະ ໜາດ ຢາ.
ມີຂໍ້ ຈຳ ກັດໃນການ ນຳ ໃຊ້ຢາຄຸມ ກຳ ເນີດ ສຳ ລັບຄົນເຈັບນ້ອຍໆ. ເດັກນ້ອຍທີ່ມີອາຍຸຕໍ່າກວ່າ 6 ປີບໍ່ຄວນໃຊ້ມັນ.
ສຳ ລັບເດັກທີ່ມີອາຍຸຫຼາຍກວ່າ, ການປິ່ນປົວດ້ວຍອິນຊູລິນແມ່ນເປັນໄປໄດ້, ໃນຂະນະທີ່ຖ້າເດັກມີຕັບ, ໝາກ ໄຂ່ຫຼັງແລະອະໄວຍະວະທີ່ຜິດປົກກະຕິ, ຄວາມເຂັ້ມຂຸ້ນຂອງນ້ ຳ ຕານແລະສະພາບຂອງລະບົບທີ່ຖືກກະທົບຄວນໄດ້ຮັບການຕິດຕາມເປັນປະ ຈຳ.
ຄວາມເຂົ້າກັນໄດ້ກັບຢາອື່ນໆ
ຢາບາງຊະນິດສາມາດເສີມຂະຫຍາຍຜົນກະທົບຂອງ Detemir:
- ຢາຮັກສານ້ ຳ ຕານໃນການຫຼຸດນ້ ຳ ຕານ
- Monoamine oxidase ແລະ angiotensin ປ່ຽນທາດ enzyme ຍັບຍັ້ງຢາ,
- ຕົວເລືອກ b-adrenergic ທີ່ບໍ່ແມ່ນເລືອກກຸ່ມ b.
ເຄື່ອງດື່ມທີ່ມີທາດເຫຼົ້າກໍ່ມີຜົນກະທົບຕໍ່ອິນຊູລິນໃນວິທີດຽວກັນ. ພວກເຂົາຍັງຊ່ວຍກະຕຸ້ນໄລຍະເວລາຂອງຜົນກະທົບຂອງ hypoglycemic.
ສານຕໍ່ໄປນີ້ຍັບຍັ້ງການກະ ທຳ ຂອງສານນີ້:
- ຮໍໂມນການຈະເລີນເຕີບໂຕທີ່ແຕກຕ່າງກັນ,
- Glucocorticoids,
- Sympathomimetics ຂອງກຸ່ມຂ,
- ຮໍໂມນ thyroid,
- ຢາທີ່ມີຢາ danazol.
Lancreotides ແລະ octreodites ສາມາດສົ່ງຜົນກະທົບຕໍ່ສອງຝ່າຍ. ໃນສະຖານະການທີ່ແຕກຕ່າງກັນ, ພວກເຂົາກະຕຸ້ນຫຼືຈົມມັນ. Sulfites ແລະ thiols ບໍ່ສາມາດໃຊ້ກັບ insulin detemir ໄດ້, ເພາະວ່າມັນ ທຳ ລາຍໂຄງສ້າງຂອງອິນຊູລິນແລະຫຼຸດຜ່ອນຜົນກະທົບຂອງມັນ. ເຄື່ອງມືນີ້ບໍ່ສາມາດຖືກເພີ່ມເຂົ້າໃນວິທີແກ້ໄຂບັນຫາກ່ຽວກັບການຕົ້ມນ້ ຳ ຕົ້ມ.
ການປ່ຽນໄປໃຊ້ Detemir ກັບ insulin ຊະນິດອື່ນ
ຂັ້ນຕອນດັ່ງກ່າວຄວນ ດຳ ເນີນພາຍໃຕ້ການຊີ້ ນຳ ຂອງຜູ້ຊ່ຽວຊານ. ການປ່ຽນແປງໃນຄວາມເຂັ້ມຂົ້ນ, ການປ່ຽນແປງຂອງຕົວແທນຕົວແທນ (ຈາກມະນຸດໄປສູ່ສັດ / ສັດຄ້າຍຄືກັນກັບອິນຊູລິນແລະໃນທາງກັບກັນ) ແລະປັດໃຈອື່ນໆອາດຈະຕ້ອງມີການປ່ຽນແປງໃນຈັງຫວະຂອງການປິ່ນປົວດ້ວຍອິນຊູລິນ.
ເມື່ອລ້ານຊ້າງ
ເມື່ອໄປເມືອງ Detemir, ທ່ານ ຈຳ ເປັນຕ້ອງຕິດຕາມລະດັບນ້ ຳ ຕານໃນເລືອດຂອງຄົນເຈັບຢ່າງຕໍ່ເນື່ອງ. ການຄວບຄຸມດັ່ງກ່າວແມ່ນຖືກປະຕິບັດໃນສອງສາມອາທິດ ທຳ ອິດ.
ເມື່ອ ດຳ ເນີນການປິ່ນປົວໂຣກເບົາຫວານທີ່ສັບສົນ, ທ່ານ ຈຳ ເປັນຕ້ອງໄດ້ພັກຜ່ອນລະຫວ່າງການໃຊ້ຢາຊະນິດຕ່າງໆ. ພວກມັນສາມາດສົ່ງຜົນກະທົບຕໍ່ການດູດຊືມແລະການດູດຊືມເຊິ່ງກັນແລະກັນ.
ອິນຊູລິນຄ້າຍຄືກັນ
Insemir insulin ມີສອງຕົວຄ້າຍຄືກັນເຊິ່ງສ່ວນປະກອບຫຼັກ (insulin detemir) ກໍ່ຄືກັນ.
ນີ້ແມ່ນຊື່ແລະລາຄາທີ່ຄາດຄະເນ:
- Levemir Flekspen ໃນຮູບແບບຂອງການສັກຢາ - ລາຄາຕໍ່ຊຸດຕໍ່ 100 ມລແມ່ນ 4500 ຮູເບີນ.
- Levemir Penfil ຍັງຢູ່ໃນຮູບແບບຂອງການແກ້ໄຂ - ຈໍານວນດຽວກັນມີຄ່າໃຊ້ຈ່າຍ 5,000 ຮູເບີນ.

ກຸ່ມການຢາດຽວກັນນີ້ປະກອບມີເງິນທຶນທີ່ມີ insulin glargine. ຊື່ການຄ້າແລະລາຄາການຫຸ້ມຫໍ່:
- ການແກ້ໄຂສີດ Aylar - ສູງເຖິງ 3500 ຮູເບີນ,
- ມາດຕະຖານ Latus Optiset ແລະ Latus - 2900 ຮູເບີນ,
- Latus Solostar - 3000 ຮູເບີນ,
- Tozheo Solostar ຈາກ 1000 ຫາ 2700 ຮູເບີນ.

ຕົວຢ່າງປຽບທຽບອື່ນໆຂອງ detemir:
- Monodar Ultralong (ການລະງັບການສີດ) - ເປັນສ່ວນ ໜຶ່ງ ຂອງອິນຊູລິນ.
- Tresiba Flekstach - ການແກ້ໄຂດ້ວຍ insulin degludec, ມີລາຄາປະມານ 5000 ຮູເບີນ.
ກ່ອນທີ່ຈະປ່ຽນປະເພດຢາອິນຊູລິນທີ່ໃຊ້, ທ່ານ ຈຳ ເປັນຕ້ອງໄດ້ປຶກສາທ່ານ ໝໍ, ເພາະວ່າກອງທຶນ ຈຳ ນວນ ໜຶ່ງ ທີ່ລະບຸໄວ້ອາດຈະມີຄວາມ ໝາຍ ຕໍ່ຄົນເຈັບ.
Detemir ແມ່ນ ໜຶ່ງ ໃນຢາອິນຊູລິນທີ່ດີທີ່ສຸດໃນແງ່ຂອງການ ກຳ ນົດທາງກາຍະພາບແລະສານເຄມີ. ມັນມີຄວາມໃກ້ຊິດທີ່ສຸດເທົ່າທີ່ຈະເຮັດໄດ້ກັບອິນຊູລິນຂອງມະນຸດ. ຜະລິດຕະພັນບໍ່ປ່ອຍໃຫ້ສານທີ່ມີການເຄື່ອນໄຫວຢູ່ໃນຮ່າງກາຍທີ່ສົ່ງຜົນກະທົບທາງລົບຕໍ່ຮ່າງກາຍ. ລາຄາຂອງມັນບໍ່ສູງກວ່າປະລິມານອິນຊູລິນອື່ນໆ.
ເພາະສະນັ້ນ, ຄ່າໃຊ້ຈ່າຍສະເລ່ຍຂອງວິທີການນີ້ແລະ versatility ເຮັດໃຫ້ມັນສາມາດນໍາໃຊ້ມັນສໍາລັບຊະນິດຂອງປະເພດຂອງຄົນເຈັບ.
ຂໍ້ມູນຄວບຄຸມ:
ໃຊ້ໃນໄລຍະຖືພາແລະລ້ຽງລູກດ້ວຍນົມແມ່
ການຖືພາ
ເມື່ອໃຊ້ Levemir m FlexPen ®ໃນລະຫວ່າງການຖືພາ, ມັນ ຈຳ ເປັນຕ້ອງພິຈາລະນາວ່າຜົນປະໂຫຍດຂອງການ ນຳ ໃຊ້ຂອງມັນຈະດີກວ່າຄວາມສ່ຽງທີ່ອາດຈະເກີດຂື້ນໄດ້ແນວໃດ.
ໜຶ່ງ ໃນການທົດລອງທາງຄລີນິກແບບຄວບຄຸມແບບບັງຄັບທີ່ກ່ຽວຂ້ອງກັບແມ່ຍິງຖືພາທີ່ມີໂລກເບົາຫວານປະເພດ 1, ໃນໄລຍະທີ່ມີປະສິດທິພາບແລະຄວາມປອດໄພຂອງການປິ່ນປົວດ້ວຍການປະສົມປະສານກັບ Levemir ® FlexPen ®ກັບ insulin aspart (152 ແມ່ຍິງຖືພາ) ໄດ້ຖືກປຽບທຽບກັບ isofan-insulin ໃນການສົມທົບກັບ insulin aspart. (ແມ່ຍິງຖືພາ 158 ຄົນ), ບໍ່ໄດ້ເປີດເຜີຍຄວາມແຕກຕ່າງຂອງຂໍ້ມູນຄວາມປອດໄພໂດຍລວມໃນລະຫວ່າງການຖືພາ, ໃນຜົນໄດ້ຮັບຂອງການຖືພາ, ຫຼືສຸຂະພາບຂອງເດັກໃນທ້ອງແລະເດັກເກີດ ໃໝ່ (ເບິ່ງພາກ“
ວິທີໃຊ້ແລະການບໍລິຫານ:
| ຄ່າສະເລ່ຍຂອງ Plasma glucose ໄດ້ວັດແທກຢ່າງອິດສະຫຼະກ່ອນອາຫານເຊົ້າ | ການປັບຕົວຂອງຢາ Levemir ® FlexPen ®, ED |
| > ຂະ ໜາດ 10.0 mmol / L (180 mg / dL) | + 8 |
| ຂະ ໜາດ 9.1-10.0 mmol / L (163-180 mg / dl) | + 6 |
| 8.1–9.0 mmol / L (145–162 mg / dL) | + 4 |
| ຂະ ໜາດ 7.1–8.0 mmol / L (127–144 mg / dl) | + 2 |
| ຂະ ໜາດ 6.1–7.0 mmol / L (109–126 mg / dl) | + 2 |
| 4.1-6.0 mmol / L | ບໍ່ມີການປ່ຽນແປງ (ມູນຄ່າເປົ້າ ໝາຍ) |
| ຖ້າມີມູນຄ່ານ້ ຳ ຕານໃນເລືອດດຽວ: | |
| 3.1–4.0 mmol / L (56–72 mg / dl) | - 2 |
| - 4 | |
ຖ້າວ່າຢາ Levemir ® FlexPen ®ຖືກ ນຳ ໃຊ້ເປັນສ່ວນ ໜຶ່ງ ຂອງລະບົບການ ບຳ ລຸງພື້ນຖານ, ມັນຄວນຈະຖືກ ກຳ ນົດ 1 ຫຼື 2 ຄັ້ງຕໍ່ມື້ໂດຍອີງໃສ່ຄວາມຕ້ອງການຂອງຄົນເຈັບ. ປະລິມານຂອງ Levemir-FlexPen ®ແມ່ນຖືກ ກຳ ນົດເປັນສ່ວນບຸກຄົນໃນແຕ່ລະກໍລະນີ.
ຄົນເຈັບທີ່ຕ້ອງການໃຊ້ຢາ 2 ຄັ້ງຕໍ່ມື້ເພື່ອຄວບຄຸມລະດັບ glycemia ຂອງພວກເຂົາໃຫ້ດີທີ່ສຸດສາມາດກິນຕອນແລງບໍ່ວ່າຈະເປັນຕອນຄ່ ຳ ຫລືຕອນນອນ. ການປັບຕົວໃຫ້ສູງຂື້ນອາດຈະມີຄວາມ ຈຳ ເປັນກັບການເພີ່ມກິດຈະ ກຳ ທາງດ້ານຮ່າງກາຍຂອງຄົນເຈັບ, ການປ່ຽນອາຫານ ທຳ ມະດາຂອງລາວຫຼືກັບພະຍາດຕິດຕໍ່.
ຢາ Levemir ® FlexPen ®ສາມາດໃຊ້ໄດ້ທັງການ ບຳ ບັດດ້ວຍ monotherapy ແລະສົມທົບກັບອິນຊູລິນ. ມັນຍັງສາມາດຖືກນໍາໃຊ້ໃນການປະສົມປະສານກັບຢາ hypoglycemic ທາງປາກ, ເຊັ່ນດຽວກັນກັບນອກເຫນືອຈາກການປິ່ນປົວທີ່ມີຢູ່ກັບ liraglutide.
ໃນການປະສົມປະສານກັບຢາທີ່ມີທາດໂລຫິດຕະຫລອດເລືອດຫຼືນອກ ເໜືອ ໄປຈາກ liraglutide, ແນະ ນຳ ໃຫ້ໃຊ້ຢາ Levemir ® FlexPen ® 1 ເທື່ອຕໍ່ມື້, ເລີ່ມຕົ້ນດ້ວຍຂະ ໜາດ 10 PIECES ຫຼື 0.1-0.2 PIECES / kg. ຢາ Levemir ® FlexPen ®ສາມາດປະຕິບັດໄດ້ທຸກເວລາທີ່ສະດວກ ສຳ ລັບຄົນເຈັບໃນເວລາກາງເວັນ, ເຖິງຢ່າງໃດກໍ່ຕາມ, ເມື່ອ ກຳ ນົດເວລາຂອງການສີດຢາທຸກໆມື້, ທ່ານຄວນຍຶດ ໝັ້ນ ກັບລະບຽບການສັກຢາທີ່ຖືກສ້າງຕັ້ງຂຶ້ນ.
Levemir ® FlexPen ®ມີຈຸດປະສົງ ສຳ ລັບການບໍລິຫານ subcutaneous ເທົ່ານັ້ນ.
Levemir ® FlexPen ®ບໍ່ຄວນຈະຖືກຄຸ້ມຄອງຢ່າງເຂັ້ມຂຸ້ນ, ເຊັ່ນດຽວກັນ ນີ້ສາມາດນໍາໄປສູ່ການ hypoglycemia ຮ້າຍແຮງ. ການບໍລິຫານຢາ Intramuscular ກໍ່ຄວນຫຼີກລ້ຽງ. Levemir ® FlexPen ®ບໍ່ໄດ້ມີຈຸດປະສົງໃນການໃຊ້ເຄື່ອງຈັກອິນຊູລິນ.
Levemir ® FlexPen ®ຖືກສີດເຂົ້າໄປໃນບໍລິເວນຂາ, ທາງ ໜ້າ ທ້ອງ, ບ່າໄຫລ່, ບໍລິເວນທ້ອງ. ສະຖານທີ່ສັກຢາຄວນໄດ້ຮັບການປ່ຽນແປງເປັນປົກກະຕິເຖິງແມ່ນວ່າຈະຖືກປະຕິບັດໃນບໍລິເວນດຽວກັນເພື່ອຫຼຸດຜ່ອນຄວາມສ່ຽງຕໍ່ການເປັນໂຣກຜີວ ໜັງ. ເຊັ່ນດຽວກັບການກະກຽມອິນຊູລິນອື່ນໆ, ໄລຍະເວລາຂອງການປະຕິບັດແມ່ນຂື້ນກັບປະລິມານ, ສະຖານທີ່ບໍລິຫານ, ຄວາມເຂັ້ມຂອງການໄຫຼວຽນຂອງເລືອດ, ອຸນຫະພູມແລະລະດັບຂອງການອອກ ກຳ ລັງກາຍ.
ກຸ່ມຄົນເຈັບພິເສດ
ເຊັ່ນດຽວກັນກັບການກະກຽມອິນຊູລິນອື່ນໆ, ໃນຜູ້ປ່ວຍຜູ້ສູງອາຍຸແລະຜູ້ປ່ວຍທີ່ມີຄວາມບໍ່ພຽງພໍກ່ຽວກັບ ໝາກ ໄຂ່ຫຼັງແລະຕັບ, ຄວາມເຂັ້ມຂຸ້ນຂອງທາດນ້ ຳ ຕານໃນເລືອດຄວນໄດ້ຮັບການຕິດຕາມຢ່າງໃກ້ຊິດແລະປະລິມານຂອງການກວດພົບໂດຍສ່ວນບຸກຄົນ.
ເດັກນ້ອຍແລະໄວລຸ້ນ
ປະສິດທິຜົນແລະຄວາມປອດໄພຂອງ Levemir ® FlexPen ®ໃນໄວລຸ້ນແລະເດັກອາຍຸຫຼາຍກວ່າ 2 ປີໄດ້ຖືກຢືນຢັນໃນການທົດລອງທາງຄລີນິກທີ່ແກ່ຍາວເຖິງ 12 ເດືອນ.
ໂອນຈາກການກະກຽມອິນຊູລິນອື່ນໆ:
ການໂອນຍ້າຍຈາກການກະກຽມອິນຊູລິນຂະ ໜາດ ກາງແລະຈາກການກະກຽມອິນຊູລິນຕໍ່ໄປເປັນເວລາດົນນານກັບ Levemir ® FlexPen ®ອາດຈະຕ້ອງການການປັບປະລິມານແລະເວລາ.
ເຊັ່ນດຽວກັບການກະກຽມອິນຊູລິນອື່ນໆ, ການຕິດຕາມກວດກາຢ່າງລະມັດລະວັງກ່ຽວກັບຄວາມເຂັ້ມຂຸ້ນຂອງທາດນ້ ຳ ຕານໃນເລືອດໃນລະຫວ່າງການໂອນຍ້າຍແລະໃນອາທິດ ທຳ ອິດຂອງການອອກຢາ ໃໝ່ ແມ່ນແນະ ນຳ ໃຫ້ໃຊ້.
ຕ້ອງມີການແກ້ໄຂການປິ່ນປົວດ້ວຍທາດ hypoglycemic (ປະລິມານແລະເວລາຂອງການບໍລິຫານຂອງການກະກຽມອິນຊູລິນສັ້ນຫຼືປະລິມານຂອງຢາ hypoglycemic ທາງປາກ).
ຜົນຂ້າງຄຽງ:
ປະຕິກິລິຍາທາງລົບທີ່ສັງເກດເຫັນໃນຄົນເຈັບທີ່ໃຊ້ Levemir ® FlexPen mainly ສ່ວນໃຫຍ່ແມ່ນຂື້ນກັບປະລິມານຢາແລະພັດທະນາຍ້ອນຜົນກະທົບດ້ານການຢາຂອງອິນຊູລິນ. ໂລກຕ່ ຳ ໃນເລືອດມັກຈະເປັນຜົນຂ້າງຄຽງທີ່ສຸດ. ການມີລະດັບຕ່ ຳ ໃນເລືອດກໍ່ຈະເກີດຂື້ນຖ້າປະລິມານທີ່ໃຊ້ເກີນປະລິມານຂອງຢາແມ່ນພົວພັນກັບຄວາມຕ້ອງການຂອງຮ່າງກາຍໃນການໃຊ້ອິນຊູລິນ. ຈາກການສຶກສາທາງດ້ານຄລີນິກມັນແມ່ນເປັນທີ່ຮູ້ກັນວ່າການລະລາຍເລືອດໃນເລືອດທີ່ຮຸນແຮງທີ່ຕ້ອງການການແຊກແຊງຂອງບຸກຄົນທີສາມພັດທະນາໃນປະມານ 6% ຂອງຄົນເຈັບທີ່ໄດ້ຮັບ Levemir ® FlexPen ®.
ປະຕິກິລິຍາຢູ່ບ່ອນສັກຢາສາມາດສັງເກດເຫັນເລື້ອຍໆກັບ Levemir-FlexPen ®ຫຼາຍກ່ວາການແນະ ນຳ ຂອງອິນຊູລິນ. ປະຕິກິລິຍາເຫຼົ່ານີ້ປະກອບມີອາການແດງ, ການອັກເສບ, ການກັດ, ການໃຄ່ບວມແລະອາການຄັນຢູ່ບ່ອນສັກຢາ. ປະຕິກິລິຍາສ່ວນໃຫຍ່ຢູ່ສະຖານທີ່ສັກຢາແມ່ນມີ ໜ້ອຍ ແລະຊົ່ວຄາວຕາມ ທຳ ມະຊາດ, i.e. ຫາຍໄປດ້ວຍການຮັກສາຕໍ່ເນື່ອງເປັນເວລາສອງສາມມື້ຫາຫລາຍອາທິດ.
ອັດຕາສ່ວນຂອງຄົນເຈັບທີ່ໄດ້ຮັບການປິ່ນປົວແລະຜູ້ທີ່ຄາດວ່າຈະພັດທະນາຜົນຂ້າງຄຽງຄາດວ່າຈະເປັນ 12%. ການເກີດຂອງຜົນຂ້າງຄຽງ, ເຊິ່ງໂດຍທົ່ວໄປຄາດຄະເນວ່າມັນກ່ຽວຂ້ອງກັບ Levemir ® FlexPen ®ໃນລະຫວ່າງການທົດລອງທາງຄລີນິກ, ແມ່ນ ນຳ ສະ ເໜີ ຢູ່ລຸ່ມນີ້.
ຄວາມຜິດປົກກະຕິຂອງເມຕິນແລະສານອາຫານ
ເລື້ອຍໆ (> 1/100, 1/100, 1/1 000, 1/1 000, 1/1 000, 1/10 000, ® FlexPen ®, ສາມາດກໍ່ໃຫ້ເກີດການ ທຳ ລາຍຂອງ insulin detemir ໄດ້. ວິທີແກ້ໄຂ.
ເງື່ອນໄຂການເກັບຮັກສາ:
ຢ່າເກັບຮັກສາປາກກາ syringe ທີ່ໃຊ້ແລ້ວໄວ້ໃນຕູ້ເຢັນ. ໃຊ້ຫລືໂອນເປັນປາກກາ syringe spare ກັບຢາ, ເກັບໄວ້ 6 ອາທິດໃນອຸນຫະພູມບໍ່ເກີນ 30 ° C.
ຫຼັງຈາກໃຊ້ແລ້ວ, ໃຫ້ປິດປາກກາ syringe ດ້ວຍ ໝວກ ເພື່ອປ້ອງກັນມັນຈາກແສງ.
ຮັກສາໃຫ້ໄກຈາກເດັກນ້ອຍ.
ຜູ້ຜະລິດ:
Novo Nordisk A / S
Novo Alle,
DK-2880 Baggswerd, ເດນມາກ
ຫ້ອງການຜູ້ຕາງ ໜ້າ "Novo Nordisk A / S"
119330, ມອດໂກ, ສ.
Lomonosovsky Prospekt 38, ຫ້ອງການ 11
Levemir ®, FlexPen ®, NovoFayn ®, NovoTvist ® - ເຄື່ອງ ໝາຍ ການຄ້າທີ່ເປັນເຈົ້າຂອງ Novo Nordisk A / S, ເດນມາກ
ຄຳ ແນະ ນຳ ສຳ ລັບຄົນເຈັບກ່ຽວກັບການ ນຳ ໃຊ້ Levemir ® FlexPen ®
ອ່ານ ຄຳ ແນະ ນຳ ເຫຼົ່ານີ້ຢ່າງລະມັດລະວັງກ່ອນທີ່ຈະໃຊ້ levemir. ® ເບື່ອ ®
Levemir ® FlexPen pen ແມ່ນປາກກາອິນຊູລິນທີ່ມີເອກະລັກສະເພາະດ້ວຍຕົວແຈກ. ຂະ ໜາດ ປະລິມານຂອງອິນຊູລິນ, ຕັ້ງແຕ່ 1 ເຖິງ 60 ໜ່ວຍ ສາມາດປ່ຽນເປັນ 1 ໜ່ວຍ ຂື້ນໄປ. Levemir ® FlexPen ®ຖືກອອກແບບມາເພື່ອໃຊ້ກັບ NovoFine ®ແລະ NovoTvist ®ເຂັມຍາວເຖິງ 8 ມມ. ໃນຖານະເປັນຂໍ້ຄວນລະວັງ, ຄວນ ນຳ ໃຊ້ລະບົບການຈັດສົ່ງອິນຊູລິນປ່ຽນແທນໃນກໍລະນີທີ່ທ່ານສູນເສຍຫຼື ທຳ ລາຍ Levemir ® FlexPen your.
ສີຂອງປາກກາ syringe ທີ່ສະແດງຢູ່ໃນຕົວຢ່າງອາດຈະແຕກຕ່າງຈາກສີຂອງ Levemir-FlexPen your. 

ເລີ່ມຕົ້ນ
ກວດເບິ່ງປ້າຍເພື່ອຮັບປະກັນວ່າ Levemir ® FlexPen ®ປະກອບດ້ວຍ insulin ຊະນິດທີ່ຖືກຕ້ອງ.
 | ກ
ເອົາຝາອອກຈາກປາກກາ syringe. ຂ້າເຊື້ອຈຸລິນຊີທີ່ເຮັດດ້ວຍຜ້າຝ້າຍ. |
 | ຂ
ຖອດສະຕິກເກີປ້ອງກັນອອກຈາກເຂັມທີ່ຖືກຖິ້ມ. ສຽບເຂັມເຂັມຄ່ອຍໆແລະແຫນ້ນໃສ່ Levemir ® FlexPen Le. |
 | ກັບ
ຖອດຝາປິດທາງນອກຂະ ໜາດ ໃຫຍ່ອອກຈາກເຂັມ, ແຕ່ຢ່າປະຖິ້ມມັນ. |
 | ດ
ຖອດແລະເອົາຝາປິດຂອງເຂັມອອກ. |
 | ການໂຍກຍ້າຍທາງອາກາດເບື້ອງຕົ້ນຈາກລົດເຂັນ
ເຖິງແມ່ນວ່າມີການໃຊ້ປາກກາຢ່າງຖືກຕ້ອງກໍ່ຕາມ, ອາກາດນ້ອຍໆກໍ່ສາມາດສະສົມຢູ່ໃນກະຕ່າກ່ອນການສີດແຕ່ລະຄັ້ງ. ເພື່ອປ້ອງກັນການເຂົ້າສູ່ຟອງອາກາດແລະຮັບປະກັນປະລິມານຢາທີ່ຖືກຕ້ອງ: ອີ ກົດ 2 ໜ່ວຍ ຂອງຢາ. |
 | ສ
ໃນຂະນະທີ່ຖື Levemir ® FlexPen ®ດ້ວຍເຂັມຂຶ້ນ, ແຕະກະຕ່າສອງສາມຄັ້ງດ້ວຍນິ້ວມືຂອງທ່ານເພື່ອໃຫ້ຟອງອາກາດເຄື່ອນຍ້າຍໄປທາງເທິງຂອງໄສ້ຕອງ. |
 | ຈ
ໃນຂະນະທີ່ຈັບປາກກາ syringe ດ້ວຍເຂັມຂຶ້ນ, ກົດປຸ່ມເລີ່ມຕົ້ນ. ຕົວເລືອກຂະ ໜາດ ຢາຈະກັບມາສູນ. ການຫຼຸດລົງຂອງ insulin ຄວນຈະປາກົດຢູ່ໃນຕອນທ້າຍຂອງເຂັມ. ຖ້າສິ່ງນີ້ບໍ່ເກີດຂື້ນ, ທົດແທນເຂັມແລະເຮັດຊ້ ຳ ອີກຂັ້ນຕອນ, ແຕ່ບໍ່ເກີນ 6 ເທື່ອ. ຖ້າຫາກວ່າອິນຊູລິນບໍ່ໄດ້ມາຈາກເຂັມ, ນີ້ສະແດງໃຫ້ເຫັນວ່າປາກກາ syringe ແມ່ນຂາດຕົກບົກຜ່ອງແລະບໍ່ຄວນໃຊ້ອີກເທື່ອ ໜຶ່ງ. |
 | ການຕັ້ງຄ່າຢາ
ໃຫ້ແນ່ໃຈວ່າຕົວເລືອກຂະ ໜາດ ຖືກຕັ້ງໃຫ້ເປັນ“ 0”. ນ ໂທຫາ ຈຳ ນວນຫົວ ໜ່ວຍ ທີ່ ຈຳ ເປັນ ສຳ ລັບການສີດ. ປະລິມານສາມາດປັບໄດ້ໂດຍການ ໝູນ ຕົວເລືອກຂະ ໜາດ ໃນທິດທາງໃດ ໜຶ່ງ ຈົນກ່ວາປະລິມານທີ່ຖືກຕ້ອງຖືກຕັ້ງຢູ່ຕໍ່ ໜ້າ ຕົວຊີ້ວັດປະລິມານຢາ. ເມື່ອ ໝຸນ ເຄື່ອງເລືອກຂະ ໜາດ ໃຫ້ລະມັດລະວັງຢ່າລະວັງກົດປຸ່ມເລີ່ມຕົ້ນເພື່ອປ້ອງກັນການປ່ອຍຂອງອິນຊູລິນ. ບໍ່ສາມາດ ກຳ ນົດປະລິມານທີ່ເກີນ ຈຳ ນວນ ໜ່ວຍ ທີ່ຍັງເຫຼືອຢູ່ໃນໄສ້ຕອງ. •ຢ່າໃຊ້ຂະ ໜາດ ທີ່ເຫຼືອເພື່ອວັດແທກລະດັບປະລິມານອິນຊູລິນ. |
 | ການບໍລິຫານອິນຊູລິນ
ໃສ່ເຂັມພາຍໃຕ້ຜິວ ໜັງ. ໃຊ້ເຕັກນິກການສີດທີ່ທ່ານ ໝໍ ແນະ ນຳ. ເພື່ອສັກ, ໃຫ້ກົດປຸ່ມເລີ່ມຕົ້ນຈົນກ່ວາ "0" ປາກົດຢູ່ຕໍ່ ໜ້າ ຕົວຊີ້ວັດປະລິມານຢາ. ຈົ່ງລະມັດລະວັງ: ເມື່ອປະຕິບັດຢາ, ພຽງແຕ່ກົດປຸ່ມເລີ່ມຕົ້ນເທົ່ານັ້ນ. ເມື່ອຕົວເລືອກຢາຂະ ໜາດ ໝູນ ວຽນ, ການບໍລິຫານປະລິມານຈະບໍ່ເກີດຂື້ນ. |
 | ເຈ
ເມື່ອຖອດເຂັມອອກຈາກໃຕ້ຜິວ ໜັງ, ກົດປຸ່ມເລີ່ມຕົ້ນທີ່ມີອາການຊຶມເສົ້າເຕັມທີ່. |
 | ເຖິງ
ຊີ້ເຂັມເຂັມໄປທາງຫລວງດ້ານນອກຂອງເຂັມໂດຍບໍ່ແຕະໃສ່ຫົວ. ເມື່ອເຂັມເຂັມເຂົ້າໄປ, ໃຫ້ໃສ່ ໝວກ ແລະປັກເຂັມ. ການເກັບຮັກສາແລະເບິ່ງແຍງ Levemir ® FlexPen ®ຖືກອອກແບບມາເພື່ອການ ນຳ ໃຊ້ທີ່ມີປະສິດຕິພາບແລະປອດໄພແລະຕ້ອງການການຈັດການຢ່າງລະມັດລະວັງ. ໃນກໍລະນີທີ່ມີການຫຼຸດລົງຫຼືຄວາມກົດດັນດ້ານກົນຈັກທີ່ແຂງແຮງ, ປາກກາ syringe ອາດຈະເສຍຫາຍແລະ insulin ອາດຈະຮົ່ວໄຫຼ. ພື້ນຜິວຂອງ Levemir ® FlexPen ®ສາມາດເຮັດຄວາມສະອາດດ້ວຍຜ້າຝ້າຍຈຸ່ມໃສ່ເຫຼົ້າ. ຢ່າຖອກໃສ່ເຂັມສັກຢາໃນເຫຼົ້າ, ຢ່າລ້າງຫລືລ້າງມັນ, ຄືກັບ ນີ້ອາດຈະ ທຳ ລາຍກົນໄກ. ຢ່າເຕີມເງິນ Levemir ® FlexPen ®. |