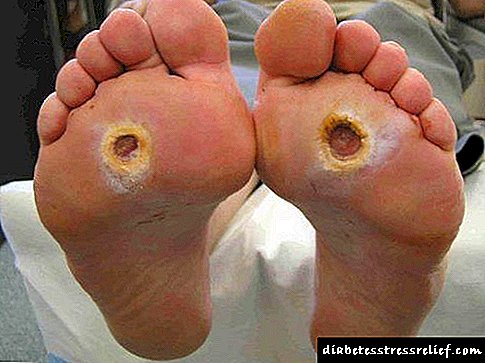
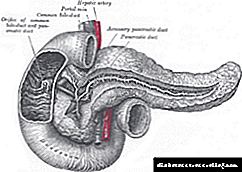
ລໍາດັບຂອງການສັງເຄາະ cholesterol ໃນຕັບ
ການຫັນປ່ຽນຂອງ lanosterol ເຂົ້າໄປໃນ cholesterol ແມ່ນປະຕິບັດຢູ່ໃນເຍື່ອຂອງ endicpatasmic hepatocyte reticulum. ຄວາມຜູກພັນຄູ່ໃນຮູບແບບໂມເລກຸນຂອງທາດປະສົມ ທຳ ອິດ. ປະຕິກິລິຍານີ້ໃຊ້ພະລັງງານຫຼາຍໂດຍໃຊ້ NADPH ເປັນຜູ້ໃຫ້ທຶນ. ຫຼັງຈາກອິດທິພົນຂອງ enzymes ຫັນປ່ຽນຕ່າງໆໃນໄລຍະ lanosterol, cholesterol ຈະປາກົດ.
ການຂົນສົ່ງ Q10
ຫນ້າທີ່ທີ່ສໍາຄັນຂອງ cholesterol ແມ່ນການໂອນຍ້າຍ Q10. ສານປະສົມນີ້ແມ່ນຮັບຜິດຊອບໃນການປົກປ້ອງເຍື່ອຈາກຜົນກະທົບທາງລົບຂອງເອນໄຊ. ຈໍານວນຂອງທາດປະສົມນີ້ແມ່ນຜະລິດອອກໃນບາງໂຄງສ້າງ, ແລະຫຼັງຈາກນັ້ນກໍ່ເຂົ້າສູ່ກະແສເລືອດ. ລາວບໍ່ມີຄວາມສາມາດທີ່ຈະເຈາະເຂົ້າໄປໃນຈຸລັງສ່ວນທີ່ເຫຼືອ, ສະນັ້ນເພື່ອຈຸດປະສົງນີ້ລາວຕ້ອງການຜູ້ໃຫ້ບໍລິການ. Cholesterol ປະສົບຜົນ ສຳ ເລັດໃນວຽກນີ້.
ຟັງຊັນການເຊື່ອມຕໍ່ພື້ນຖານ
ດັ່ງທີ່ໄດ້ກ່າວມາຂ້າງເທິງ, ສານນີ້ສາມາດເປັນປະໂຫຍດ ສຳ ລັບມະນຸດ, ແນ່ນອນ, ຖ້າພວກເຮົາ ກຳ ລັງເວົ້າເຖິງ HDL.
ອີງໃສ່ສິ່ງນີ້, ມັນຈະກາຍເປັນທີ່ຈະແຈ້ງວ່າການຢືນຢັນວ່າຄໍເລສເຕີໂຣນແມ່ນເປັນອັນຕະລາຍແທ້ໆຕໍ່ມະນຸດແມ່ນຄວາມຜິດພາດ.
Cholesterol ແມ່ນສ່ວນປະກອບທີ່ເຮັດວຽກທາງຊີວະພາບ:
- ມີສ່ວນຮ່ວມໃນການສັງເຄາະຮໍໂມນເພດຊາຍ,
- ຮັບປະກັນການເຮັດວຽກປົກກະຕິຂອງ receptors serotonin ໃນສະ ໝອງ,
- ແມ່ນສ່ວນປະກອບຫຼັກຂອງ ໜິ້ວ ນໍ້າບີ, ເຊັ່ນດຽວກັນກັບວິຕາມິນ D, ເຊິ່ງຮັບຜິດຊອບຕໍ່ການດູດຊຶມຂອງໄຂມັນ,
- ປ້ອງກັນບໍ່ໃຫ້ຂະບວນການ ທຳ ລາຍໂຄງສ້າງພາຍໃຕ້ອິດທິພົນຂອງອິດສະຫຼະອິດສະຫຼະ.
ແຕ່ຄຽງຄູ່ກັບຄຸນລັກສະນະໃນທາງບວກ, ສານດັ່ງກ່າວສາມາດມີຜົນກະທົບບາງຢ່າງຕໍ່ສຸຂະພາບຂອງມະນຸດ. ຍົກຕົວຢ່າງ, LDL ສາມາດເຮັດໃຫ້ເກີດການພັດທະນາຂອງພະຍາດຮ້າຍແຮງ, ປະກອບສ່ວນຕົ້ນຕໍເຂົ້າໃນການພັດທະນາຂອງໂລກ atherosclerosis.
ຢູ່ໃນຕັບ, ສານເຄມີຊີວະພາບຖືກສັງເຄາະພາຍໃຕ້ອິດທິພົນຂອງ HMG ທີ່ຖືກປັບ ໃໝ່. ນີ້ແມ່ນເອນໄຊຕົ້ນຕໍທີ່ກ່ຽວຂ້ອງກັບການໃຊ້ຊີວະວິທະຍາ. ການຍັບຍັ້ງການສັງເຄາະເກີດຂື້ນພາຍໃຕ້ອິດທິພົນຂອງຄວາມຄິດເຫັນໃນແງ່ລົບ.
ຂະບວນການຂອງການສັງເຄາະສານໃນຕັບມີການພົວພັນກັນກັບປະລິມານຂອງສານປະສົມທີ່ເຂົ້າສູ່ຮ່າງກາຍຂອງມະນຸດກັບອາຫານ.
ເຖິງແມ່ນວ່າງ່າຍດາຍ, ຂະບວນການນີ້ຖືກອະທິບາຍດ້ວຍວິທີນີ້. ຕັບຄວບຄຸມລະດັບ cholesterol ເປັນອິດສະຫຼະ. ຄົນເຮົາບໍລິໂພກອາຫານທີ່ມີສ່ວນປະກອບນີ້ຫຼາຍເທົ່າໃດ, ສານກໍ່ຈະຖືກຜະລິດ ໜ້ອຍ ລົງໃນຈຸລັງຂອງອະໄວຍະວະແລະຖ້າເຮົາ ຄຳ ນຶງເຖິງວ່າໄຂມັນບໍລິໂພກຮ່ວມກັນກັບຜະລິດຕະພັນທີ່ບັນຈຸມັນ, ຂະບວນການກົດລະບຽບນີ້ມີຄວາມ ສຳ ຄັນຫຼາຍ.
ລັກສະນະຂອງການສັງເຄາະສານ
ຜູ້ໃຫຍ່ທີ່ມີສຸຂະພາບດີປົກກະຕິສັງເຄາະ HDL ໃນອັດຕາປະມານ 1 g / ມື້ແລະບໍລິໂພກປະມານ 0.3 g / ມື້.
 ລະດັບທີ່ຂ້ອນຂ້າງຂອງ cholesterol ໃນເລືອດມີຄຸນຄ່າດັ່ງກ່າວ - 150-200 mg / dl. ຮັກສາໄວ້ເປັນສ່ວນໃຫຍ່ໂດຍຄວບຄຸມລະດັບການສັງເຄາະຂອງໂດໂຊໂວ.
ລະດັບທີ່ຂ້ອນຂ້າງຂອງ cholesterol ໃນເລືອດມີຄຸນຄ່າດັ່ງກ່າວ - 150-200 mg / dl. ຮັກສາໄວ້ເປັນສ່ວນໃຫຍ່ໂດຍຄວບຄຸມລະດັບການສັງເຄາະຂອງໂດໂຊໂວ.
ມັນເປັນສິ່ງສໍາຄັນທີ່ຈະສັງເກດວ່າການສັງເຄາະຂອງ HDL ແລະ LDL ຂອງຕົ້ນກໍາເນີດທີ່ເປັນສານ endogenous ແມ່ນຖືກຄວບຄຸມໂດຍບາງສ່ວນໂດຍອາຫານ.
Cholesterol ທັງຈາກອາຫານແລະສັງເຄາະໃນຕັບແມ່ນໃຊ້ໃນການສ້າງເຍື່ອ, ໃນການສັງເຄາະຮໍໂມນສະເຕີຣອຍແລະກົດອາຊິດບີ. ອັດຕາສ່ວນທີ່ໃຫຍ່ທີ່ສຸດຂອງສານແມ່ນໃຊ້ໃນການສັງເຄາະອາຊິດບີ.
ການໄດ້ຮັບສານ HDL ແລະ LDL ໂດຍຈຸລັງຖືກຮັກສາໄວ້ໃນລະດັບທີ່ ໝັ້ນ ຄົງໂດຍ 3 ກົນໄກທີ່ແຕກຕ່າງກັນ:
- ລະບຽບການຂອງກິດຈະ ກຳ HMGR
- ກົດລະບຽບຂອງລະດັບຄໍເລດສະເຕີຣອຍຟຣີເກີນໂດຍຜ່ານກິດຈະ ກຳ ຂອງ O-acyltransferase sterol, SOAT1 ແລະ SOAT2 ກັບ SOAT2, ເຊິ່ງເປັນສ່ວນປະກອບທີ່ມີສ່ວນ ສຳ ຄັນໃນຕັບ. ການອອກແບບເບື້ອງຕົ້ນ ສຳ ລັບເອນໄຊເຫຼົ່ານີ້ແມ່ນ ACAT ສຳ ລັບ acyl-CoA: acyltransferase cholesterol. Enzymes ACAT, ACAT1, ແລະ ACAT2 ແມ່ນ acetyl CoA acetyltransferases 1 ແລະ 2.
- ໂດຍການຄວບຄຸມລະດັບ cholesterol ຂອງ plasma ຜ່ານ LDL-mediated receptor ແລະການຂົນສົ່ງດ້ານ HDL-mediated.
ລະບຽບການຂອງກິດຈະ ກຳ HMGR ແມ່ນວິທີການຕົ້ນຕໍໃນການຄວບຄຸມລະດັບການຜະລິດຊີວະພາບຂອງ LDL ແລະ HDL.
ເອນໄຊໄດ້ຖືກຄວບຄຸມໂດຍ 4 ກົນໄກທີ່ແຕກຕ່າງກັນ:
- ຂໍ້ສະ ເໜີ ແນະ,
- ການຄວບຄຸມການສະແດງອອກຂອງເຊື້ອສາຍ,
- ອັດຕາການເຊື່ອມໂຊມຂອງ enzyme,
- phosphorylation-dephosphorylation.
ກົນໄກຄວບຄຸມສາມຢ່າງ ທຳ ອິດແມ່ນປະຕິບັດໂດຍກົງຕໍ່ສານດັ່ງກ່າວ. Cholesterol ເຮັດ ໜ້າ ທີ່ເປັນຕົວຍັບຍັ້ງການປະຕິກິລິຍາຈາກ HMGR ທີ່ມີມາກ່ອນ, ແລະຍັງເຮັດໃຫ້ມີການເຊື່ອມໂຊມຂອງເອນໄຊຢ່າງໄວວາ. ສຸດທ້າຍແມ່ນຜົນມາຈາກການ polyubiquitination ຂອງ HMGR ແລະການເຊື່ອມໂຊມຂອງມັນໃນໂປຣຕີນ. ຄວາມສາມາດນີ້ແມ່ນຜົນຂອງໂດເມນທີ່ລະອຽດອ່ອນຂອງ HMGR SSD.
ນອກຈາກນັ້ນ, ໃນເວລາທີ່ຄໍເລດສະເຕີຣອນເກີນ, ປະລິມານຂອງ mRNA ສຳ ລັບ HMGR ຫຼຸດລົງເນື່ອງຈາກການສະແດງອອກຂອງເຊື້ອສາຍ.
Enzymes ມີສ່ວນຮ່ວມໃນການສັງເຄາະ
 ຖ້າສ່ວນປະກອບ exogenous ຖືກຄວບຄຸມໂດຍຜ່ານການດັດແກ້ covalent, ຂະບວນການນີ້ຈະຖືກປະຕິບັດເປັນຜົນມາຈາກ phosphorylation ແລະ dephosphorylation.
ຖ້າສ່ວນປະກອບ exogenous ຖືກຄວບຄຸມໂດຍຜ່ານການດັດແກ້ covalent, ຂະບວນການນີ້ຈະຖືກປະຕິບັດເປັນຜົນມາຈາກ phosphorylation ແລະ dephosphorylation.
ເອນໄຊແມ່ນມີການເຄື່ອນໄຫວຫຼາຍທີ່ສຸດໃນຮູບແບບທີ່ບໍ່ມີການປ່ຽນແປງ. Phosphorylation ຂອງ enzyme ຫຼຸດຜ່ອນກິດຈະກໍາຂອງມັນ.
HMGR ແມ່ນ phosphorylated ໂດຍ kinase ທາດໂປຼຕີນຈາກ AMP, AMPK. AMPK ຕົວມັນເອງຖືກກະຕຸ້ນໂດຍ phosphorylation.
phosphorylation AMPK ແມ່ນຖືກລະລາຍໂດຍຢ່າງຫນ້ອຍສອງ enzymes, ຄື:
- kinase ຕົ້ນຕໍທີ່ຮັບຜິດຊອບໃນການເປີດໃຊ້ AMPK ແມ່ນ LKB1 (ຕັບ kinase B1). LKB1 ໄດ້ຖືກລະບຸຕົວ ທຳ ອິດວ່າເປັນເຊື້ອສາຍໃນມະນຸດທີ່ມີການປ່ຽນແປງທີ່ໂດດເດັ່ນໃນອັດຕະໂນມັດໃນໂຣກ Putz-Jegers, PJS. LKB1 ຍັງພົບວ່າມີເຊື້ອໂຣກໃນໂຣກ adenocarcinoma ປອດ.
- ທາດໂປຼຕີນຈາກ phosphorylating ທີສອງ AMPK ແມ່ນທາດໂປຼຕີນຈາກ kinase kinase beta-calmodulin-dependant (CaMKK Ca). CaMKKβເຮັດໃຫ້ເກີດ phosphorylation AMPK ໃນການຕອບສະ ໜອງ ຕໍ່ການເພີ່ມຂື້ນຂອງ Ca2 + ໃນກ້າມເຊິ່ງເປັນຜົນມາຈາກການຫົດຕົວຂອງກ້າມເນື້ອ.
ກົດລະບຽບຂອງ HMGR ໂດຍການດັດແກ້ covalent ຊ່ວຍໃຫ້ຜະລິດ HDL. HMGR ແມ່ນມີການເຄື່ອນໄຫວຫຼາຍທີ່ສຸດໃນລັດ dephosphorylated. Phosphorylation (Ser872) ແມ່ນຖືກລະລາຍໂດຍທາດໂປຼຕີນຈາກທາດໂປຼຕີນຈາກ kinase (AMPK) ທີ່ມີການເຄື່ອນໄຫວຂອງ AMP, ກິດຈະກໍາທີ່ຍັງຖືກຄວບຄຸມໂດຍ phosphorylation.
phosphorylation AMPK ສາມາດເກີດຂື້ນໄດ້ເນື່ອງຈາກມີຢ່າງ ໜ້ອຍ ສອງ enzymes:
Dephosphorylation ຂອງ HMGR, ການສົ່ງມັນກັບຄືນສູ່ສະຖານະທີ່ມີການເຄື່ອນໄຫວຫຼາຍຂຶ້ນ, ແມ່ນຖືກປະຕິບັດໂດຍຜ່ານກິດຈະ ກຳ ຂອງໂປຼຕີນໂປຼຕີນຂອງຄອບຄົວ 2A. ລໍາດັບນີ້ຊ່ວຍໃຫ້ທ່ານສາມາດຄວບຄຸມການຜະລິດ HDL.
ຜົນກະທົບຕໍ່ປະເພດຂອງ cholesterol ແມ່ນຫຍັງ?
 PP2A ທີ່ມີການເຮັດວຽກມີຢູ່ໃນສອງ isoform catalytic ທີ່ແຕກຕ່າງກັນທີ່ຖືກເຂົ້າລະຫັດໂດຍສອງ ກຳ ມະພັນທີ່ຖືກລະບຸວ່າ PPP2CA ແລະ PPP2CB. ສອງ isoforms ຕົ້ນຕໍຂອງ PP2A ແມ່ນ enzyme ຫຼັກ heterodimeric ແລະ holoenzyme heterotrimeric.
PP2A ທີ່ມີການເຮັດວຽກມີຢູ່ໃນສອງ isoform catalytic ທີ່ແຕກຕ່າງກັນທີ່ຖືກເຂົ້າລະຫັດໂດຍສອງ ກຳ ມະພັນທີ່ຖືກລະບຸວ່າ PPP2CA ແລະ PPP2CB. ສອງ isoforms ຕົ້ນຕໍຂອງ PP2A ແມ່ນ enzyme ຫຼັກ heterodimeric ແລະ holoenzyme heterotrimeric.
ທາດ enzyme ຕົ້ນຕໍຂອງ PP2A ປະກອບດ້ວຍອະນຸພາກ scaffold (ເດີມເອີ້ນວ່າ A subunit) ແລະທາດຍ່ອຍຍ່ອຍ (C subunit). ສານອະນຸມູນອິຕາລີໄດ້ຖືກເຂົ້າລະຫັດໂດຍ gene PPP2CA, ແລະທາດຍ່ອຍຍ່ອຍໄດ້ຖືກລະຫັດໂດຍ gene PPP2CB.
ພື້ນຖານໂຄງລ່າງຂອງ scaffold ແມ່ນຖືກເຂົ້າລະຫັດໂດຍ gene PPP2R1A ແລະສ່ວນຍ່ອຍຂອງ gene PPP2R1B. ທາດ enzyme ຕົ້ນຕໍ, PP2A, ພົວພັນກັບ subunit ລະບຽບການທີ່ມີຕົວປ່ຽນແປງເພື່ອປະກອບເຂົ້າໃນ holoenzyme.
ລະບົບຍ່ອຍຂອງ PP2A ລວມມີ 4 ຄອບຄົວ (ແຕ່ເດີມເອີ້ນວ່າ B-subunits), ເຊິ່ງແຕ່ລະປະກອບດ້ວຍ isoforms ຫຼາຍທີ່ຖືກເຂົ້າລະຫັດໂດຍພັນທຸ ກຳ ທີ່ແຕກຕ່າງກັນ.
ໃນປະຈຸບັນ, ມີ 15 ເຊື້ອພັນທຸ ກຳ ທີ່ແຕກຕ່າງກັນ ສຳ ລັບລະບົບຍ່ອຍຂອງ PP2A B. ໜ້າ ທີ່ຕົ້ນຕໍຂອງລະບົບຍ່ອຍຂອງລະບຽບ PP2A ແມ່ນເພື່ອແນໃສ່ໂປຣຕີນຍ່ອຍ phosphorylated ເພື່ອກິດຈະ ກຳ phosphatase ຂອງທາດຍ່ອຍຍ່ອຍຂອງ PP2A.
PPP2R ແມ່ນ ໜຶ່ງ ໃນ 15 ອະນຸ ກຳ ມະການທີ່ແຕກຕ່າງກັນຂອງ PP2A. ຮໍໂມນເຊັ່ນ: glucagon ແລະ adrenaline ສົ່ງຜົນກະທົບຕໍ່ biosynthesis cholesterol ໂດຍການເພີ່ມກິດຈະ ກຳ ຂອງລະບົບຍ່ອຍຂອງລະບຽບການສະເພາະຂອງ enzymes ຂອງ PP2A.
PKA-mediated phosphorylation ຂອງລະບຽບການຍ່ອຍຂອງ PP2A (PPP2R) ເຮັດໃຫ້ການປ່ອຍ PP2A ອອກຈາກ HMGR, ປ້ອງກັນການລະລາຍຂອງມັນ. ໂດຍການຕ້ານກັບຜົນກະທົບຂອງ glucagon ແລະ adrenaline, insulin ກະຕຸ້ນການຂັບຖ່າຍຂອງຟອສເຟດແລະເຮັດໃຫ້ກິດຈະ ກຳ ຂອງ HMGR ເພີ່ມຂື້ນ.
ລະບຽບການເພີ່ມເຕີມຂອງ HMGR ເກີດຂື້ນໂດຍການສະກັດກັ້ນການຕອບສະ ໜອງ ກັບຄໍເລດເຕີລອນ, ພ້ອມທັງກົດລະບຽບຂອງການສັງເຄາະຂອງມັນໂດຍການເພີ່ມລະດັບຂອງຄໍເລດສະເຕີຣອຍແລະສະເຕີຣອຍ.
ປະກົດການສຸດທ້າຍນີ້ແມ່ນພົວພັນກັບປັດໄຈການໂອນຍ້າຍ SREBP.
ຂັ້ນຕອນໃນຮ່າງກາຍຂອງມະນຸດມີຄືແນວໃດ?
 ກິດຈະ ກຳ HMGR ຍັງຖືກຕິດຕາມກວດກາໂດຍການເຊັນສັນຍາກັບ AMP. ການເພີ່ມຂື້ນຂອງ cAMP ກະຕຸ້ນ kinase ທາດໂປຼຕີນຈາກ cAMP, PKA. ໃນແງ່ຂອງລະບຽບການຂອງ HMGR, PKA phosphorylates ລະບຽບຍ່ອຍ, ເຊິ່ງນໍາໄປສູ່ການເພີ່ມຂື້ນຂອງການປ່ອຍ PP2A ຈາກ HMGR. ນີ້ປ້ອງກັນ PP2A ຈາກການຖອດ phosphates ອອກຈາກ HMGR, ປ້ອງກັນການເຄື່ອນໄຫວຂອງມັນ.
ກິດຈະ ກຳ HMGR ຍັງຖືກຕິດຕາມກວດກາໂດຍການເຊັນສັນຍາກັບ AMP. ການເພີ່ມຂື້ນຂອງ cAMP ກະຕຸ້ນ kinase ທາດໂປຼຕີນຈາກ cAMP, PKA. ໃນແງ່ຂອງລະບຽບການຂອງ HMGR, PKA phosphorylates ລະບຽບຍ່ອຍ, ເຊິ່ງນໍາໄປສູ່ການເພີ່ມຂື້ນຂອງການປ່ອຍ PP2A ຈາກ HMGR. ນີ້ປ້ອງກັນ PP2A ຈາກການຖອດ phosphates ອອກຈາກ HMGR, ປ້ອງກັນການເຄື່ອນໄຫວຂອງມັນ.
ຄອບຄົວໃຫຍ່ຂອງທາດໂປຼຕີນຈາກໂປຼຕີນ phosphatase ທີ່ມີກົດລະບຽບຄວບຄຸມແລະ / ຫຼືຍັບຍັ້ງການເຄື່ອນໄຫວຂອງ phosphatases ຫຼາຍ, ລວມທັງສະມາຊິກຂອງຄອບຄົວ PP1, PP2A, ແລະ PP2C. ນອກເຫນືອໄປຈາກ phosphatases PP2A, ເຊິ່ງເອົາ phosphates ຈາກ AMPK ແລະ HMGR, phosphatases ຂອງຄອບຄົວໂປຕີນ phosphatase 2C (PP2C) ຍັງເອົາ phosphates ຈາກ AMPK.
ໃນເວລາທີ່ລະບຽບການເຫຼົ່ານີ້ຍ່ອຍ phosphorylate PKA, ກິດຈະກໍາຂອງ phosphatases ຜູກພັນຫຼຸດລົງ, ເຊິ່ງເຮັດໃຫ້ AMPK ຍັງຄົງຢູ່ໃນສະພາບ phosphorylated ແລະເຄື່ອນໄຫວ, ແລະ HMGR ໃນສະພາບ phosphorylated ແລະບໍ່ມີການເຄື່ອນໄຫວ. ເມື່ອການກະຕຸ້ນຖືກຍ້າຍອອກ, ເຮັດໃຫ້ການຜະລິດ cAMP ເພີ່ມຂຶ້ນ, ລະດັບ phosphorylation ຫຼຸດລົງ, ແລະລະດັບ dephosphorylation ເພີ່ມຂື້ນ. ຜົນສຸດທ້າຍແມ່ນການກັບຄືນສູ່ລະດັບສູງຂອງກິດຈະ ກຳ HMGR. ໃນທາງກົງກັນຂ້າມ, insulin ເຮັດໃຫ້ການຫຼຸດລົງຂອງ cAMP, ເຊິ່ງ, ໃນທາງກັບກັນ, ກະຕຸ້ນການສັງເຄາະ. ຜົນສຸດທ້າຍແມ່ນການກັບຄືນສູ່ລະດັບສູງຂອງກິດຈະ ກຳ HMGR.
ໃນທາງກົງກັນຂ້າມ, insulin ເຮັດໃຫ້ການຫຼຸດລົງຂອງ cAMP, ເຊິ່ງ, ໃນທາງກັບກັນ, ກະຕຸ້ນການສັງເຄາະ cholesterol. ຜົນສຸດທ້າຍແມ່ນການກັບຄືນສູ່ລະດັບສູງຂອງກິດຈະ ກຳ HMGR. Insulin ເຮັດໃຫ້ການຫຼຸດລົງຂອງ cAMP, ເຊິ່ງໃນທາງກັບກັນ, ສາມາດຖືກນໍາໃຊ້ເພື່ອເສີມຂະຫຍາຍຂະບວນການສັງເຄາະ.
ຄວາມສາມາດໃນການກະຕຸ້ນ insulin ແລະຍັບຍັ້ງ glucagon, ກິດຈະກໍາ HMGR ແມ່ນສອດຄ່ອງກັບອິດທິພົນຂອງຮໍໂມນເຫຼົ່ານີ້ຕໍ່ກັບຂະບວນການເຜົາຜານອາຫານອື່ນໆ. ຫນ້າທີ່ຕົ້ນຕໍຂອງຮໍໂມນທັງສອງນີ້ແມ່ນເພື່ອຄວບຄຸມການເຂົ້າເຖິງແລະການຂົນສົ່ງພະລັງງານໄປຍັງຈຸລັງທັງ ໝົດ.
ການຕິດຕາມກວດກາໄລຍະຍາວຂອງກິດຈະ ກຳ HMGR ແມ່ນ ດຳ ເນີນເປັນສ່ວນໃຫຍ່ໂດຍການຄວບຄຸມການສັງເຄາະແລະການເສື່ອມສະພາບຂອງເອນໄຊ. ເມື່ອລະດັບໄຂມັນສູງ, ລະດັບຂອງການສະແດງອອກ gene ຂອງ HMGR ຫຼຸດລົງ, ແລະໃນທາງກັບກັນ, ລະດັບຕ່ ຳ ຈະກະຕຸ້ນການສະແດງອອກຂອງ gene.
ຂໍ້ມູນກ່ຽວກັບ cholesterol ແມ່ນມີໃຫ້ໃນວີດີໂອໃນບົດຄວາມນີ້.
ເນື້ອໃນ ສຳ ຄັນຂອງຂັ້ນຕອນການຜະລິດໂມເລກຸນທາດໄຂມັນແມ່ນຫຍັງ?
ອາຫານຫຼາຍຊະນິດເຮັດໃຫ້ຮ່າງກາຍມີຄໍເລດເຕີຣອນ - ເຫຼົ່ານີ້ແມ່ນຜະລິດຕະພັນທີ່ມາຈາກສັດເຊັ່ນດຽວກັນກັບໄຂມັນ trans ເຊິ່ງພົບໃນປະລິມານຫຼາຍໃນອາຫານທີ່ປຸງແຕ່ງພ້ອມທັງອາຫານໄວ (ອາຫານໄວ).
ຖ້າທ່ານໃຊ້ຜະລິດຕະພັນດັ່ງກ່າວຢ່າງມະຫາສານ, ຫຼັງຈາກນັ້ນ, ຄວາມເຂັ້ມຂົ້ນຂອງໂມເລກຸນໂມເລກຸນໃນເລືອດຈະສູງຂື້ນແລະທ່ານຈະຕ້ອງໄດ້ໃຊ້ວິທີແກ້ໄຂທາງການແພດຕໍ່ hypercholesterolemia.
ທາດ Cholesterol ເຊິ່ງເຂົ້າສູ່ຮ່າງກາຍກັບອາຫານມີຄວາມ ໜາ ແໜ້ນ ໂມເລກຸນຕ່ ຳ ເຊິ່ງ ນຳ ໄປສູ່ການວາງຕົວຂອງຄໍເລສເຕີຣອນດັ່ງກ່າວໃສ່ໃນຫອຍພາຍໃນຂອງເສັ້ນເລືອດ, ເຊິ່ງເປັນການກະຕຸ້ນການພັດທະນາຂອງຄໍເລສເຕີໂຣນແລະພະຍາດເສັ້ນເລືອດຂອງໂລກ atherosclerosis.
ການເພີ່ມຂື້ນຂອງດັດສະນີ cholesterol ໃນເລືອດເກີດຂື້ນບໍ່ພຽງແຕ່ຍ້ອນວ່າມັນໄດ້ຮັບຈາກພາຍນອກ, ແຕ່ກໍ່ຍັງເປັນການລະເມີດໃນຂະບວນການການສັງເຄາະໂມເລກຸນ lipoprotein ໂດຍຈຸລັງຕັບ.
 ການສັງເຄາະ Cholesterol ເນື້ອຫາ↑
ການສັງເຄາະ Cholesterol ເນື້ອຫາ↑
ການສັງເຄາະໄຂມັນໃນຕັບ
ການສັງເຄາະໄຂມັນໃນຮ່າງກາຍແມ່ນປະມານ 0.50-0,80 ກຼາມຕໍ່ມື້.
ການສັງເຄາະໂມເລກຸນໄຂມັນໃນຮ່າງກາຍແມ່ນແຈກຢາຍ:
- 50.0% ແມ່ນຜະລິດໂດຍຈຸລັງຕັບ,
- 15.0% - 20.0% - ໂດຍພະແນກຂອງ ລຳ ໄສ້ນ້ອຍ,
- 10.0% - ຖືກສັງເຄາະໂດຍ adrenal cortex ແລະຈຸລັງຜິວ ໜັງ.
ຈຸລັງທັງ ໝົດ ໃນຮ່າງກາຍຂອງຄົນເຮົາມີຄວາມສາມາດໃນການສັງເຄາະ lipoproteins.
ດ້ວຍອາຫານ, ເຖິງ 20.0% ຂອງໂມເລກຸນໄຂມັນທັງ ໝົດ ເຂົ້າສູ່ຮ່າງກາຍ - ປະມານ 0.40 ກຣາມຕໍ່ມື້.
Lipoproteins ຖືກໄລ່ອອກນອກຮ່າງກາຍໂດຍການຊ່ວຍເຫຼືອຂອງກົດບີ, ແລະຕໍ່ມື້ການໃຊ້ໂມເລກຸນ cholesterol ໂດຍນໍ້າບີບໍ່ເກີນ 1.0 ກຣາມ.
ຊີວະວິທະຍາຂອງ lipoproteins ໃນຮ່າງກາຍ
ຊີວະວິທະຍາຂອງໂມເລກຸນ lipid ເກີດຂື້ນໃນພະແນກ endoplasmic - reticulum. ພື້ນຖານ ສຳ ລັບອະຕອມຂອງໂມເລກຸນກາກບອນແມ່ນສານ acetyl-SCoA, ເຊິ່ງເຂົ້າໄປໃນ endoplasm ຈາກ mitochondria ໃນໂມເລກຸນທາດໂປຼຕີນ.
ໃນໄລຍະຊີວະເຄມີສາດຂອງໂມເລກຸນ lipoprotein, ໂມເລກຸນ 18 ATP ມີສ່ວນ, ແລະໂມເລກຸນ NADPH 13 ກາຍເປັນຜູ້ເຂົ້າຮ່ວມໃນການສັງເຄາະ.
ຂະບວນການຂອງການສ້າງຄໍເລສເຕີຣອນຈະຜ່ານຢ່າງ ໜ້ອຍ 30 ໄລຍະແລະປະຕິກິລິຍາຕ່າງໆໃນຮ່າງກາຍ.
ການສັງເຄາະໄລຍະຂອງ lipoproteins ສາມາດແບ່ງອອກເປັນກຸ່ມ:
ໃສ່ການກະຕຸ້ນທີ່ກະຕຸ້ນ - ລະດັບນໍ້າຕານ
- ການສັງເຄາະຂອງອາຊິດ mevalonic ເກີດຂື້ນໃນໄລຍະ ketogenesis ຂອງສອງປະຕິກິລິຍາ ທຳ ອິດ, ແລະຫລັງຈາກຂັ້ນຕອນທີສາມ, hydroxy-3-methylglutaryl-ScoA ປະຕິກິລິຍາກັບໂມເລກຸນ HMG-ScoA reductase. ຈາກປະຕິກິລິຍານີ້, Mevalonate ຖືກສັງເຄາະ. ປະຕິກິລິຍານີ້ຮຽກຮ້ອງໃຫ້ມີປະລິມານ glucose ໃນເລືອດຢ່າງພຽງພໍ. ທ່ານສາມາດແຕ່ງກິນໄດ້ໂດຍການຊ່ວຍເຫຼືອຂອງອາຫານຫວານແລະທັນຍາພືດ,
- ການສັງເຄາະສານ isopentenyl diphosphate ເກີດຂື້ນຫຼັງຈາກການເພີ່ມຟອສເຟດໄປຫາໂມເລກຸນອາຊິດ mevalonic ແລະການສູນເສຍນ້ ຳ ຂອງພວກມັນ,
- ການສັງເຄາະຂອງ farnesyl diphosphate ເກີດຂື້ນຫຼັງຈາກການປະສົມຂອງໂມເລກຸນ 3 isopentenyl diphosphate,
- ການສັງເຄາະ Squalene ແມ່ນການຜູກມັດ 2 ໂມເລກຸນຂອງ farnesyl diphosphate,
- ປະຕິກິລິຍາຂອງການຫັນປ່ຽນຂອງ squalene ກັບໂມເລກຸນ lanosterol ເກີດຂື້ນ,
- ຫຼັງຈາກການ ກຳ ຈັດກຸ່ມ methyl ທີ່ບໍ່ ຈຳ ເປັນ, cholesterol ກໍ່ຈະປ່ຽນໄປ.


ລະບຽບການຂອງການສັງເຄາະ lipoproteins
ອົງປະກອບກົດລະບຽບໃນຂະບວນການສັງເຄາະແມ່ນທາດອີໂຊນ hydroxymethylglutaryl-ScoA reductase. ຄວາມສາມາດຂອງເອນໄຊນີ້ໃນການປ່ຽນກິດຈະ ກຳ ແມ່ນຫຼາຍກ່ວາ 100 ເທົ່າ.
ລະບຽບການຂອງກິດຈະ ກຳ enzyme ເກີດຂື້ນຕາມຫຼັກການຫຼາຍຢ່າງ:
- ລະບຽບການຂອງການສັງເຄາະຢູ່ໃນລະດັບການເຜົາຜານອາຫານ. ຫຼັກການນີ້ເຮັດວຽກ "ຈາກກົງກັນຂ້າມ", ເອນໄຊໄດ້ຖືກຍັບຍັ້ງໂດຍ cholesterol, ເຊິ່ງເຮັດໃຫ້ມັນສາມາດຮັກສາເນື້ອໃນທີ່ຄົງທີ່ໄດ້,
- ກົດລະບຽບຂອງຮໍໂມນ Covalent.
ລະບຽບໃນລະດັບຮໍໂມນເກີດຂື້ນໃນໄລຍະດັ່ງຕໍ່ໄປນີ້:
- ການເພີ່ມຂື້ນຂອງ insulin ຮໍໂມນໃນຮ່າງກາຍເຮັດໃຫ້ phosphatase ທາດໂປຼຕີນ, ເຊິ່ງກະຕຸ້ນການເພີ່ມຂື້ນຂອງກິດຈະກໍາຂອງ enzyme ຕົ້ນຕໍ HMG-ScoA reductase,
- ຮໍໂມນ glucagon ແລະຮໍໂມນ adrenaline ມີຄວາມສາມາດໃນການກະຕຸ້ນອົງປະກອບຂອງທາດໂປຼຕີນ kinase A, ເຊິ່ງ phosphorylates enzyme HMG-ScoA reductase ແລະຫຼຸດຜ່ອນກິດຈະ ກຳ ຂອງມັນ,
- ກິດຈະ ກຳ ຂອງການສັງເຄາະຄໍເລສເຕີຣອນແມ່ນຂື້ນກັບຄວາມເຂັ້ມຂົ້ນຂອງໂປຕີນສົ່ງໃນເລືອດ, ເຊິ່ງຈະເຮັດໃຫ້ເກີດປະຕິກິລິຍາໃນລະດັບປານກາງຂອງທາດແປ້ງ.
ໄຂມັນໃນຮ່າງກາຍ
cholesterol ທີ່ຖືກສັງເຄາະຢູ່ໃນຈຸລັງຕັບແມ່ນມີຄວາມ ຈຳ ເປັນ ສຳ ລັບຮ່າງກາຍ ສຳ ລັບຂະບວນການ ສຳ ຄັນຕ່າງໆ:
- ຕັ້ງຢູ່ໃນແຕ່ລະເຍື່ອຂອງຈຸລັງ, ໂມເລກຸນໄຂມັນທີ່ເຮັດໃຫ້ມັນແຂງແຮງແລະເຮັດໃຫ້ມັນຍືດເຍື້ອ,
- ດ້ວຍການຊ່ວຍເຫຼືອຂອງ lipoproteins, ຈຸລັງ choroid ເພີ່ມຄວາມຕ້ານທານຂອງມັນ, ເຊິ່ງປົກປ້ອງພວກເຂົາຈາກອິດທິພົນຈາກພາຍນອກ,
- ຖ້າບໍ່ມີການຊ່ວຍເຫຼືອຂອງ lipoproteins, ຕ່ອມ adrenal ບໍ່ໄດ້ຜະລິດປະເພດຮໍໂມນເພດຊາຍ,
- ການໃຊ້ລິບສະຕິກ, ການຜະລິດອາຊິດບີນໍ້າບີເກີດຂື້ນແລະປ້ອງກັນການພົກຍ່ຽວຕ່ອມຂົມຈາກການສ້າງກ້ອນຫີນໃນນັ້ນ,
- Lipoproteins ຜູກກັນຈຸລັງ neuron ໃນກະດູກສັນຫຼັງແລະໃນສະຫມອງ,
- ດ້ວຍການຊ່ວຍເຫຼືອຂອງ lipoproteins, ກາບຂອງເສັ້ນໃຍເສັ້ນປະສາດໄດ້ຖືກສ້າງຄວາມເຂັ້ມແຂງ,
- ດ້ວຍການຊ່ວຍເຫຼືອຂອງຄໍເລສເຕີໂຣນ, ການຜະລິດວິຕາມິນດີເກີດຂື້ນ, ເຊິ່ງຊ່ວຍດູດຊຶມທາດແຄວຊ້ຽມແລະປ້ອງກັນການ ທຳ ລາຍເນື້ອເຍື່ອກະດູກ.
Cholesterol ຊ່ວຍໃຫ້ຕ່ອມ adrenal ເຮັດການສັງເຄາະຮໍໂມນກຸ່ມເຫຼົ່ານີ້:
- ກຸ່ມ Corticosteroid
- ກຸ່ມຮໍໂມນ Glucocorticoid,
- ກຸ່ມຂອງ mineralocorticoids.
 Cholesterol ຊ່ວຍຜະລິດ adrenal ການສັງເຄາະກຸ່ມຮໍໂມນ
Cholesterol ຊ່ວຍຜະລິດ adrenal ການສັງເຄາະກຸ່ມຮໍໂມນຮໍໂມນເຫຼົ່ານີ້ໃຫ້ຂະບວນການຂອງລະບຽບການຮໍໂມນຂອງອະໄວຍະວະສືບພັນຂອງມະນຸດ.
ໂມເລກຸນຂອງ cholesterol ຫຼັງຈາກການສັງເຄາະໃນຈຸລັງຕັບເຂົ້າໄປໃນອະໄວຍະວະ endocrine ຂອງຕ່ອມ adrenal ແລະປະກອບສ່ວນໃນການຜະລິດຮໍໂມນແລະຮັກສາຄວາມສົມດຸນໃນຂອບເຂດຮໍໂມນ.
ການລະລາຍຂອງໂມເລກຸນຂອງວິຕາມິນ D ໃນຮ່າງກາຍ
ການຜະລິດໂມເລກຸນວິຕາມິນດີແມ່ນມາຈາກແສງແດດເຊິ່ງມັນຈະເຂົ້າໄປໃນຄໍເລສເຕີຣອນທີ່ຢູ່ໃຕ້ຜິວ ໜັງ. ໃນຈຸດນີ້, ການສັງເຄາະວິຕາມິນດີເກີດຂື້ນ, ເຊິ່ງມັນມີຄວາມ ສຳ ຄັນຫຼາຍຕໍ່ຮ່າງກາຍໃນການດູດຊຶມແຮ່ທາດແຄວຊ້ຽມ.
lipoproteins ທຸກຊະນິດ, ຫຼັງຈາກການສັງເຄາະ, ຖືກຂົນສົ່ງຜ່ານຮ່າງກາຍໂດຍລະບົບສາຍເລືອດ.
ວິຕາມິນ D ສາມາດປ່ຽນເປັນພຽງແຕ່ lipoproteins ທີ່ມີໂມເລກຸນທີ່ມີຄວາມຫນາແຫນ້ນສູງ, ແລະ lipids ນ້ ຳ ໜັກ ໂມເລກຸນຕ່ ຳ ກໍ່ໃຫ້ເກີດການພັດທະນາຂອງພະຍາດເສັ້ນເລືອດ atherosclerosis, ເພາະວ່າພວກມັນມີຄວາມສາມາດທີ່ຈະຕົກລົງຢູ່ໃນເຍື່ອພາຍໃນຂອງເສັ້ນເລືອດໃນຮູບແບບຂອງຄໍເລດເຕີລໍໂຕ, ເຊິ່ງຈະເລີນເຕີບໂຕແລະເຮັດໃຫ້ເກີດພະຍາດທາງເສັ້ນເລືອດນີ້.
ບາງຄັ້ງແຜງ cholesterol ສາມາດສັງເກດເຫັນຢູ່ໃນມະນຸດພາຍໃຕ້ຜິວ ໜັງ ຢູ່ໃນມື.
 ການລະລາຍຂອງວິຕາມິນ D ເນື້ອຫາ↑
ການລະລາຍຂອງວິຕາມິນ D ເນື້ອຫາ↑
ການລົບກວນໃນການສັງເຄາະ lipoproteins
ໃນຫຼາຍຂະບວນການທາງເດີນອາຫານໃນຮ່າງກາຍ, ຄວາມລົ້ມເຫຼວແລະການລົບກວນສາມາດເກີດຂື້ນໄດ້. ຄວາມຜິດປົກກະຕິດັ່ງກ່າວສາມາດເກີດຂື້ນໃນການເຜົາຜານໄຂມັນ lipid. ມີຫຼາຍເຫດຜົນແລະພວກມັນມີລະບົບນິເວດວິທະຍາທີ່ມີປະສິດທິພາບສູງ.
ສາເຫດ endogenous ຂອງຜິດປົກກະຕິການສັງເຄາະ lipoprotein ປະກອບມີ:
- ອາຍຸຂອງຄົນ. ພາຍຫຼັງ 40 ປີໃນຮ່າງກາຍຂອງມະນຸດ, ການຜະລິດຮໍໂມນເພດ ສຳ ພັນແລະຄວາມເປັນມາຂອງຮໍໂມນແມ່ນຖືກລົບກວນ, ແລະເມື່ອຮອດອາຍຸ 45 - 50 ປີ, ຂະບວນການເຜົາຜານອາຫານທັງ ໝົດ ຊ້າລົງ, ເຊິ່ງຍັງສາມາດ ນຳ ໄປສູ່ການ ທຳ ລາຍລະບົບເຜົາຜານໄຂມັນ lipid,
- ບົດບາດຍິງ - ຊາຍແມ່ນມີຄວາມສ່ຽງຕໍ່ການສະສົມຂອງ cholesterol ຫຼາຍກວ່າແມ່ຍິງ. ແມ່ຍິງກ່ອນການ ໝົດ ປະ ຈຳ ເດືອນແລະປະ ຈຳ ເດືອນແມ່ນປ້ອງກັນໂດຍການຜະລິດຮໍໂມນເພດຊາຍ, ຈາກການສະສົມຂອງ lipoproteins,
- predisposition ພັນທຸກໍາພັນທຸກໍາ. ການພັດທະນາຂອງ hypercholesterolemia ຄອບຄົວ.
ສາເຫດທີ່ເຮັດໃຫ້ເກີດຄວາມຜິດປົກກະຕິຂອງ lipid ປະກອບມີປັດໃຈຕ່າງໆທີ່ຂື້ນກັບວິຖີຊີວິດຂອງຄົນເຈັບ, ເຊັ່ນດຽວກັນກັບບັນດາພະຍາດທີ່ກ່ຽວຂ້ອງເຊິ່ງກໍ່ໃຫ້ເກີດການລະເມີດໃນການສັງເຄາະໂມເລກຸນ cholesterol:
- ສິ່ງເສບຕິດນິໂກຕິນ,
- ສິ່ງເສບຕິດເຫຼົ້າເຮື້ອຮັງ,
- ໂພຊະນາການທີ່ບໍ່ຖືກຕ້ອງສາມາດນໍາໄປສູ່ການເພີ່ມຂື້ນຂອງ cholesterol ໃນຮ່າງກາຍແລະການສະສົມຂອງມັນບໍ່ພຽງແຕ່ຢູ່ໃນເລືອດ,
- ຊີວິດ sedentary ເປັນສາເຫດຂອງຂະບວນການ E -book ທີ່ຊັກຊ້າແລະການສັງເຄາະ lipoprotein,
- ຄວາມດັນໂລຫິດ - ຄວາມດັນເລືອດສູງໃນກະແສເລືອດເຮັດໃຫ້ມີຄວາມຕ້ອງການລ່ວງ ໜ້າ ສຳ ລັບເຍື່ອຫລອດເລືອດໃນເລືອດທີ່ຈະອີ່ມຕົວດ້ວຍໄຂມັນທີ່ເປັນໄຂມັນ, ເຊິ່ງຕໍ່ມາປະກອບເປັນຄໍເລດເຕີລໍໄຂມັນ.
- Dyslipidemia ແມ່ນຄວາມຜິດປົກກະຕິໃນການລະລາຍໄຂມັນ lipid. ດ້ວຍພະຍາດທາງດ້ານເຊື້ອພະຍາດ, ຄວາມບໍ່ສົມດຸນເກີດຂື້ນລະຫວ່າງ VP lipoproteins, lipids NP, ເຊັ່ນດຽວກັນກັບລະດັບຂອງ triglycerides ໃນເລືອດ,
- ໂລກອ້ວນພະຍາດ,
- ໂຣກເບົາຫວານ mellitus. ມີ hyperglycemia, ການເຜົາຜະຫລານແລະ metabolism lipid ແມ່ນຖືກລົບກວນ.
 ໂລກອ້ວນພະຍາດເນື້ອຫາ↑
ໂລກອ້ວນພະຍາດເນື້ອຫາ↑ການຂາດໃນຮ່າງກາຍຂອງໂມເລກຸນໄຂມັນທີ່ເປັນປະໂຫຍດ
ມີພະຍາດວິທະຍາທີ່ຊ່ວຍຫຼຸດຜ່ອນຄວາມເຂັ້ມຂົ້ນຂອງໄຂມັນໂມເລກຸນໃນເລືອດເນື່ອງຈາກການຫຼຸດລົງຂອງການສັງເຄາະໂມເລກຸນ HDL.
ນີ້ສາມາດນໍາໄປສູ່ການເປັນພະຍາດໃນຕ່ອມ thyroid, ສາມາດສົ່ງຜົນກະທົບຢ່າງຫຼວງຫຼາຍຕໍ່ລະດັບນໍ້າຕານໃນເລືອດແລະເຮັດໃຫ້ເກີດພະຍາດເບົາຫວານ, ພ້ອມທັງເຮັດໃຫ້ເກີດພະຍາດຫຼາຍຢ່າງໃນກະແສເລືອດແລະອະໄວຍະວະຫົວໃຈ.
ຜົນສະທ້ອນຂອງຄວາມເຂັ້ມຂົ້ນຂອງໄຂມັນໂມເລກຸນສູງສາມາດເປັນໄດ້:
- ພະຍາດວິທະຍາຂອງ rickets, ເຊິ່ງພັດທະນາໃນໄວເດັກຍ້ອນການຫຼຸດຜ່ອນການສັງເຄາະຂອງວິຕາມິນ D ແລະການຍ່ອຍອາຫານຂອງໂມເລກຸນທາດການຊຽມ,
- ໄວແກ່ຂອງຈຸລັງຮ່າງກາຍ. ຖ້າບໍ່ມີການສະ ໜອງ ໄຂມັນຂອງຄໍເລສເຕີຣອນໃຫ້ທັນເວລາ, ພວກມັນຈະຖືກ ທຳ ລາຍແລະຂະບວນການຂອງຜູ້ສູງອາຍຸເລີ່ມຕົ້ນ,
- ການຫຼຸດລົງຢ່າງຫນັກຂອງນ້ ຳ ໜັກ ໃນຮ່າງກາຍ, ເຊິ່ງເກີດຂື້ນຈາກການສັງເຄາະໂມເລກຸນໄຂມັນທີ່ບໍ່ພຽງພໍ, ແລະການລະລາຍຂອງໄຂມັນທີ່ເຮັດໃຫ້ໄຂມັນໃນຮ່າງກາຍຫຼຸດລົງ.
- ຄວາມເຈັບປວດໃນເນື້ອເຍື່ອກ້າມເນື້ອຈາກການຂາດຈຸລັງກ້າມເນື້ອໄຂມັນ,
- ຄວາມເຈັບປວດໃນອະໄວຍະວະຫົວໃຈທີ່ສາມາດເຮັດໃຫ້ເກີດການໂຈມຕີຫົວໃຈ.
ເພື່ອແກ້ໄຂດັດສະນີ cholesterol ທີ່ມີນ້ ຳ ໜັກ ໂມເລກຸນສູງ, ທ່ານສາມາດ ນຳ ໃຊ້ອາຫານການກິນເຊິ່ງປະກອບມີປາທະເລ, ນ້ ຳ ມັນພືດຕ່າງໆ, ພ້ອມທັງຜະລິດຕະພັນນົມ.
ແລະຢ່າລືມກ່ຽວກັບຫມາກໄມ້ສົດ, ພືດສະຫມຸນໄພແລະຜັກ - ພວກມັນຄວນຈະຊະນະໃນອາຫານ.