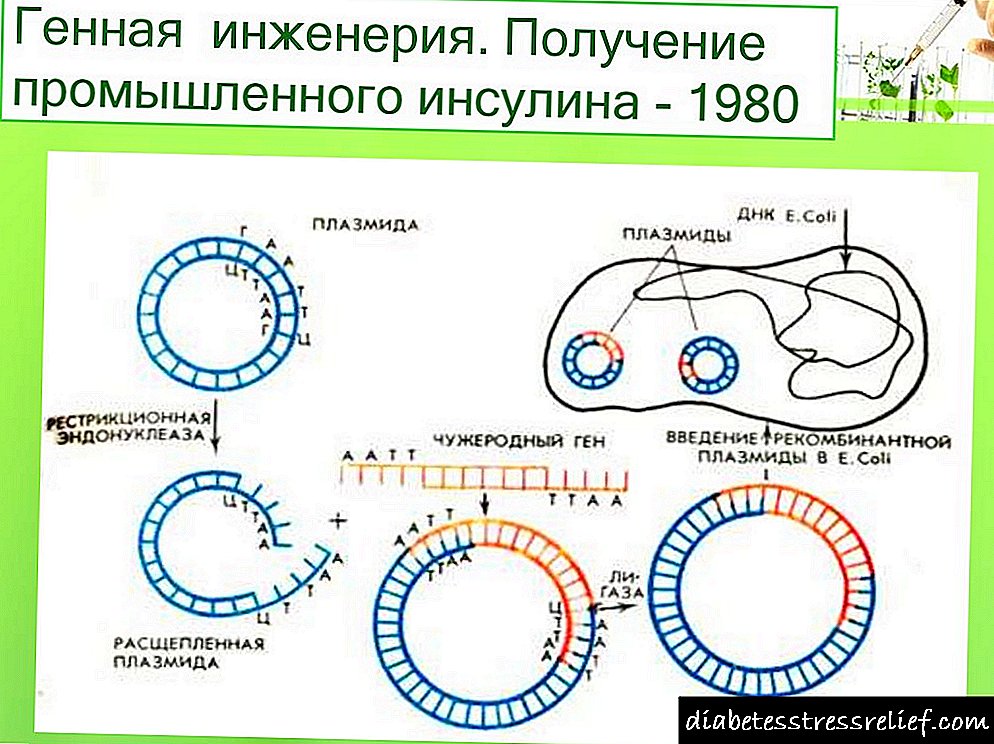
ການຜະລິດອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ
Insulin - ຮໍໂມນເພ້ຍທີ່ຄວບຄຸມ | ທາດແປ້ງທາດແປ້ງແລະຮັກສາລະດັບປົກກະຕິຂອງ cazdpaໃນເລືອດ. ການຂາດຮໍໂມນນີ້ໃນຮ່າງກາຍ ນຳ.) ເປັນ ໜຶ່ງ ໃນພະຍາດທີ່ຮ້າຍແຮງທີ່ສຸດ - ພະຍາດເບົາຫວານເຊິ່ງເປັນສາເຫດຂອງການເສຍຊີວິດແມ່ນຢູ່ໃນອັນດັບ 3 ຫຼັງຈາກພະຍາດຫຼອດເລືອດຫົວໃຈແລະມະເຮັງ. ອິນຊູລິນເປັນໂລກຂະ ໜາດ ນ້ອຍ | ທາດໂປຼຕີນທີ່ບັນຈຸສານອາຊິດ amino ທີ່ມີ 51 ແລະປະກອບດ້ວຍຕ່ອງໂສ້ polypeptide ສອງເຊື່ອມຕໍ່ກັນໂດຍຂົວ disulfide ສອງແຫ່ງ. ມັນໄດ້ຖືກສັງເຄາະໃນຮູບແບບຂອງລະບົບຕ່ອງໂສ້ເສັ້ນດ່າງເບື້ອງຕົ້ນ, preproinsulin, ບັນຈຸ koi peptide ສັນຍານສູນກາງ (ສານຕົກຄ້າງຂອງອາຊິດ amino 23) ແລະ peptide ເຊື່ອມຕໍ່ 35 ເຊື່ອມຕໍ່ (C-peptide). ໃນເວລາທີ່ peptide ສັນຍານໄດ້ຖືກໂຍກຍ້າຍອອກ, proinsulin ຈາກທາດອາຊິດ amino amino 86 ຖືກສ້າງຕັ້ງຂື້ນໃນຫ້ອງ, ເຊິ່ງສາຍໂສ້ A ແລະ B ຂອງ insulin ຖືກເຊື່ອມຕໍ່C-neitweed, ເຊິ່ງໃຫ້ພວກເຂົາມີແນວທາງທີ່ ຈຳ ເປັນໃນລາຄາ 3 ໂດລາ ສຳ ລັບຄວາມຜູກພັນ disulfide. ຫຼັງຈາກການແຍກທາດໂປຼຕີນຈາກ C peptide, ອິນຊູລິນຈະຖືກສ້າງຕັ້ງຂຶ້ນ.
ໂຣກເບົາຫວານຫລາຍຮູບແບບແມ່ນເປັນທີ່ຮູ້ກັນດີ. ຮູບແບບທີ່ຮຸນແຮງທີ່ສຸດ, ສຳ ລັບການປິ່ນປົວທີ່ຄົນເຈັບຕ້ອງການຢາອິນຊູລິນ (ຮູບແບບທີ່ຂື້ນກັບອິນຊູລິນຂອງພະຍາດ), ແມ່ນເກີດມາຈາກການຕາຍຂອງຈຸລັງທີ່ເລືອກເອົາການສັງເຄາະຮໍໂມນນີ້ (ຈຸລັງຂອງ islets of Langerhans ໃນກະຕ່າຍ). ຮູບແບບຂອງໂຣກເບົາຫວານ, ເຊິ່ງການປິ່ນປົວດ້ວຍອິນຊູລິນບໍ່ ຈຳ ເປັນ, ແມ່ນພົບເລື້ອຍກວ່າ, ມັນສາມາດຄວບຄຸມໄດ້ໂດຍການຊ່ວຍເຫຼືອໃນຄາບອາຫານທີ່ ເໝາະ ສົມແລະຖາມຄືນ:> ແມ່. ໂດຍປົກກະຕິແລ້ວ, ຝູງສັດປີກແລະງົວບໍ່ໄດ້ຖືກ ນຳ ໃຊ້ເຂົ້າໃນອຸດສາຫະ ກຳ ຊີ້ນແລະກະປcanອງແລະຖືກ ນຳ ໄປໃສ່ໃນຕູ້ເຢັນ ສຳ ລັບບໍລິສັດການຢາບ່ອນທີ່ການ ນຳ ເອົາຮໍໂມນອອກໄປ. ເພື່ອໃຫ້ໄດ້ 100 g cr! ທາດ insulin Thallic ຕ້ອງການອາຫານສັດ 800-1000 ກິໂລ
ການສັງເຄາະຂອງຕ່ອງໂສ້ທັງສອງແລະການເຊື່ອມຕໍ່ຂອງພັນທະບັດທີ່ບໍ່ເອົາໃຈໃສ່ຂອງພວກເຂົາເພື່ອໃຫ້ໄດ້ຮັບອິນຊູລິນໄດ້ຖືກປະຕິບັດໃນປີ 1963 ແລະປີ 1965. ສາມທີມຄົ້ນຄ້ວາໃນສະຫະລັດອາເມລິກາ, ຈີນແລະເຢຍລະມັນ. ໃນປີ 1980, ບໍລິສັດເດັນມາກ Novo Industri ຂອງເດັນມາກໄດ້ພັດທະນາວິທີການໃນການປ່ຽນອິນຊູລິນຂອງ ໝູ ໃຫ້ເປັນອິນຊູລິນຂອງມະນຸດໂດຍການທົດແທນທາດອາລີນນິນທີ 30 ໃນຕ່ອງໂສ້ B ກັບສານເສດເຫຼືອ threonine. ທັງສອງ insulin ບໍ່ແຕກຕ່າງກັນໃນກິດຈະ ກຳ ແລະໄລຍະເວລາຂອງການປະຕິບັດ.
ການເຮັດວຽກກ່ຽວກັບວິສະວະ ກຳ ທາງພັນທຸ ກຳ ຂອງອິນຊູລິນໄດ້ເລີ່ມຕົ້ນປະມານ 20 ປີກ່ອນ. ໃນປີ 1978, ຂໍ້ຄວາມໄດ້ປາກົດຂື້ນກ່ຽວກັບການຜະລິດສາຍພັນຂອງ Escherichia coli ທີ່ຜະລິດ proinsulin ຫນູ (USA). ໃນປີດຽວກັນ, ຕ່ອງໂສ້ອິນຊູລິນຂອງມະນຸດແຕ່ລະຄົນໄດ້ຖືກສັງເຄາະໂດຍການສະແດງອອກຂອງເຊື້ອສາຍສັງເຄາະຂອງພວກມັນຢູ່ໃນຈຸລັງ.ອີ.coli(ຮູບທີ 5.11). ແຕ່ລະເຊື້ອພັນທຸ ກຳ ທີ່ໄດ້ຮັບມານັ້ນໄດ້ຖືກດັດແປງໄປຫາ 3'-end ຂອງ gene enzyme (3-galactosidase ແລະ ນຳ ສະ ເໜີ ເຂົ້າໄປໃນ plasmid vector)(pBR322).ຈຸລັງອີ.coliຫັນປ່ຽນດ້ວຍ plasmids ທີ່ ຈຳ ເປັນເຊັ່ນນັ້ນ, ທາດໂປຼຕີນປະສົມ (chimeric) ໄດ້ຖືກຜະລິດອອກມາເຊິ່ງປະກອບດ້ວຍສ່ວນປະກອບຂອງ p-galactosidase ແລະ A ຫຼື B insulin peptide ທີ່ຕິດກັບມັນຜ່ານສານຕົກຄ້າງ methionine. ໃນເວລາທີ່ການປຸງແຕ່ງທາດໂປຼຕີນຈາກ chimeric ກັບ cyanogen bromide, peptide ຖືກປ່ອຍອອກມາ. ເຖິງຢ່າງໃດກໍ່ຕາມ, ການປິດຂົວ disulfide ລະຫວ່າງຕ່ອງໂສ້ອິນຊູລິນແມ່ນມີຄວາມຫຍຸ້ງຍາກ.
ໃນປີ 1981, ຕົວຢ່າງການເສີມທາດອິນຊູລິນ, mini-C-pro-insulin, ໄດ້ຖືກສັງເຄາະໃນການທີ່ C-peptide 35 ໜ່ວຍ ຖືກທົດແທນດ້ວຍສ່ວນ ໜຶ່ງ ຂອງອາຊິດ amino 6 ຊະນິດ: arg-arg-gly-ser-lys-arg ແລະການສະແດງອອກຂອງມັນຖືກສະແດງຢູ່ໃນອີ.coli.
ໃນປີ 1980, W. Gilbert ແລະເພື່ອນຮ່ວມງານຂອງລາວໄດ້ແຍກຕົວ insulin mRNA ອອກຈາກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກປອດໄພ. cDNA ຜົນໄດ້ຮັບຖືກໃສ່ເຂົ້າໄປໃນ plasmidpBR322ອີ.coliໃນພາກກາງຂອງເຊື້ອ penicillinase. plasmid ທີ່ສົມບູນແບບມີຂໍ້ມູນກ່ຽວກັບໂຄງສ້າງຂອງ proinsulin.ເປັນຜົນມາຈາກການແປພາສາ mRNA, ທາດໂປຼຕີນປະສົມໄດ້ຖືກສັງເຄາະຢູ່ໃນຈຸລັງທີ່ມີສານເປນີຊີລິນແລະລະດັບ proinsulin, ເຊິ່ງຖືກຍ່ອຍດ້ວຍ trypsin ຈາກທາດໂປຼຕີນດັ່ງກ່າວ.
ໃນປີ 1978, ພະນັກງານຂອງສະຖາບັນວິຊາເຄມີຊີວະພາບພາຍໃຕ້ການຊີ້ ນຳ ຂອງ Acad. A. Ovchinnikov, ສອງໂຄງສ້າງພັນທຸກໍາທີ່ເຂົ້າລະຫັດການສັງເຄາະຂອງ neuropeptides ໄດ້ຖືກສັງເຄາະ:leucine- enkephalin ແລະ bradykinin.ເຊື້ອໂຣກ leucine enkephalin ທີ່ສັງເຄາະມີສອງສົ້ນ“ ໜຽວ”:
ເຊື້ອສາຍສັງເຄາະທີ່ໄດ້ຮັບໄດ້ຖືກລວມເຂົ້າກັບຊິ້ນສ່ວນ DNA ທຳ ມະຊາດທີ່ມີສ່ວນສົ່ງເສີມແລະສ່ວນທີ່ຕັ້ງຢູ່ໃກ້ກັບເຊື້ອສາຍໂປຕີນ E. coli P-galactosidase.ອີ.coliກັບ plasmid ໄດ້
ການໄດ້ຮັບສານອິນຊູລິນ, ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ, ເຕັກໂນໂລຊີຊີວະພາບ - ວຽກວິຊາ

1. ໂຄງສ້າງແລະ ໜ້າ ທີ່ຂອງອິນຊູລິນ 5
1.1. ໂຄງສ້າງຂອງໂມເລກຸນອິນຊູລິນ 5
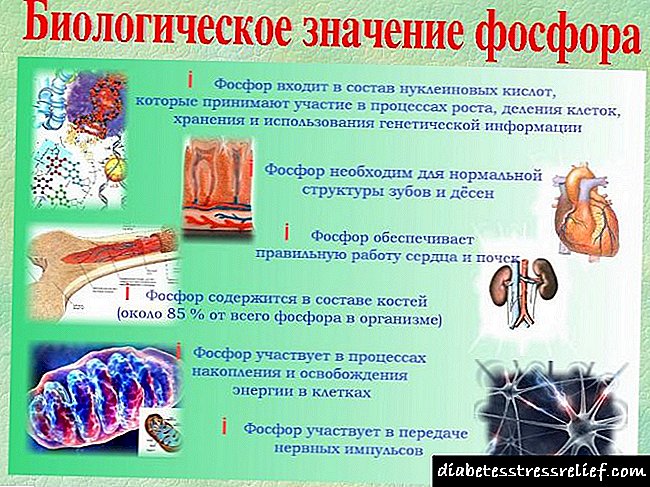
1.2. ຄວາມ ສຳ ຄັນທາງຊີວະພາບຂອງອິນຊູລິນ 7
1.3. ການຍັບຍັ້ງການວິເຄາະທາງອິນຊີ 8
2. ການສັງເຄາະອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ 10
2.1. ການໃຊ້ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ ສຳ ລັບການສັງເຄາະຢາ 10
2.2. ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ 11
2.3. ການຜະລິດອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ 14
ຄັດຈາກຂໍ້ຄວາມ
ຍິ່ງໄປກວ່ານັ້ນ, ທັງສອງສ່ວນປະກອບເຫຼົ່ານີ້ອາດຈະມີຢູ່ພ້ອມໆກັນໃນສ່ວນປະກອບຂອງທາດໂປຼຕີນປະສົມ. ນອກຈາກນັ້ນ, ໃນເວລາທີ່ສ້າງໂປຣຕີນປະສົມ, ຫຼັກການຂອງຫຼາຍຮູບແບບສາມາດ ນຳ ໃຊ້ໄດ້ - ການມີ polypeptide ເປົ້າ ໝາຍ ຫຼາຍຊະນິດໃນໂປຼຕີນປະສົມເຊິ່ງສາມາດເພີ່ມຜົນຜະລິດຂອງຜະລິດຕະພັນເປົ້າ ໝາຍ ໄດ້ຢ່າງຫຼວງຫຼາຍ.
ໃນປະເທດອັງກິດ, ທາດອິນຊູລິນທັງສອງຊະນິດໄດ້ຖືກສັງເຄາະໂດຍໃຊ້ E. coli, ເຊື່ອມຕໍ່ກັບໂມເລກຸນຂອງຮໍໂມນທີ່ໃຊ້ຊີວະວິທະຍາ. ເພື່ອໃຫ້ອົງການທີ່ບໍ່ເປັນເອກະພາບສາມາດສັງເຄາະໂມເລກຸນອິນຊູລິນໃນກະດູກສັນຫຼັງຂອງມັນ, ມັນ ຈຳ ເປັນຕ້ອງສະ ໜອງ ໃຫ້ກັບໂປແກຼມທີ່ ຈຳ ເປັນ, ນັ້ນຄືການແນະ ນຳ ຕົວຮໍໂມນຮໍໂມນ.
ທາດ insulin ທີ່ໄດ້ຮັບຄືນແມ່ນໄດ້ມາຈາກສະຖາບັນວິທະຍາສາດວິທະຍາສາດລັດເຊຍໂດຍໃຊ້ສາຍພັນຂອງເຄື່ອງຈັກອີຍິບ. ທາດໂປຼຕີນຈາກຕົວປະສົມແມ່ນສະແດງອອກຈາກຊີວະມວນທີ່ເຕີບໃຫຍ່, ສະແດງອອກເປັນປະລິມານ
40. ຂອງທາດໂປຼຕີນຈາກຈຸລັງທັງ ໝົດ ປະກອບດ້ວຍ preproinsulin.
ການປ່ຽນໃຈເຫລື້ອມໃສຂອງມັນໃຫ້ອິນຊູລິນໃນ vitro ແມ່ນ ດຳ ເນີນໄປຕາມ ລຳ ດັບຄືກັນກັບໃນ vivo - polypeptide ຊັ້ນ ນຳ ແມ່ນ ກຳ ຈັດ, preproinsulin ຖືກປ່ຽນເປັນອິນຊູລິນໂດຍຜ່ານໄລຍະຂອງ sulfitolysis ຜຸພັງ, ຕາມດ້ວຍການປິດການຜະລິດຂອງພັນທະບັດສາມຫລ່ຽມແລະການໂດດດ່ຽວຂອງ C-peptide. ຫຼັງຈາກໄລຍະຂອງການແລກປ່ຽນທາດ ion, ຊຸດ, ເຈນແລະ HPLC ການເຮັດຄວາມສະອາດ chromatographic, insulin ຂອງມະນຸດຂອງຄວາມບໍລິສຸດສູງແລະກິດຈະ ກຳ ທຳ ມະຊາດແມ່ນໄດ້ຮັບ.
ເພື່ອໃຫ້ໄດ້ຮັບສານອິນຊູລິນ, ສາຍພັນແມ່ນຖືກ ນຳ ໃຊ້ກັບ nucleotide ຕາມ ລຳ ດັບ plasmid ທີ່ສະແດງທາດໂປຼຕີນປະສົມເຊິ່ງປະກອບດ້ວຍທາດໂປຣຕີນເສັ້ນແລະສ່ວນຂອງທາດໂປຼຕີນ Staphylococcus aureus A ຕິດກັບ N-terminus ຂອງມັນຜ່ານທາດເສດ methionine 8, 9, 10.
ການປູກຝັງຂອງເຊື້ອໄຟຊີວະພາບທີ່ອີ່ມຕົວຂອງຈຸລັງຂອງສາຍພັນທີ່ສົມບູນແບບເຮັດໃຫ້ການເລີ່ມຕົ້ນຂອງການຜະລິດໂປຣຕີນປະສົມ, ການໂດດດ່ຽວແລະການຫັນເປັນ ລຳ ດັບເຊິ່ງໃນທໍ່ ນຳ ໄປສູ່ການເຮັດອິນຊູລິນ.
ອີກວິທີ ໜຶ່ງ ກໍ່ຍັງເປັນໄປໄດ້: ການໄດ້ຮັບໃນລະບົບແບັກທີເລຍຂອງການສະແດງອອກຂອງທາດໂປຼຕີນທີ່ປະສົມປະສານກັບໂປຕີນ proinsulin ຂອງມະນຸດແລະຫາງ polyhistidine ຕິດຢູ່ໃນມັນໂດຍຜ່ານສານຕົກຄ້າງ methionine. ມັນຖືກແຍກອອກໄປໂດຍການໃຊ້ຊິບໂຄຣໂປຼແກຼມ chelate ໃສ່ຖັນດ້ວຍ Ni-agarose ແລະ bromine cleavage.
ທາດໂປຼຕີນທີ່ໂດດດ່ຽວແມ່ນ S-sulfonated. ການສ້າງແຜນທີ່ແລະການວິເຄາະສັງເຄາະມະຫາສານກ່ຽວກັບທາດໂປຼຕິນທີ່ໄດ້ຮັບທີ່ບໍລິສຸດໂດຍການແລກປ່ຽນທາດຊິລິໂຄນແລກປ່ຽນ ion ກ່ຽວກັບການແລກປ່ຽນນ້ ຳ ຢາງ anion ແລະ RP (ໄລຍະປີ້ນກັບກັນ) ສະພາບຊິລິໂຄນແຫຼວທີ່ມີປະສິດຕິພາບສູງ.
ບໍ່ດົນມານີ້, ໄດ້ມີການເອົາໃຈໃສ່ຢ່າງໃກ້ຊິດໃນການເຮັດຂັ້ນຕອນງ່າຍໆໃນການຜະລິດອິນຊູລິນໂດຍວິສະວະ ກຳ ທາງພັນທຸ ກຳ.ດັ່ງນັ້ນ, ຕົວຢ່າງ, ທ່ານສາມາດໄດ້ຮັບທາດໂປຼຕີນທີ່ປະກອບດ້ວຍ proinsulin ຕິດກັບ N-terminus ຜ່ານທາດແຫຼວ lysine ຂອງ peleide ຜູ້ ນຳ interleukin.
2. ທາດໂປຼຕີນແມ່ນຖືກສະແດງອອກແລະປະຕິບັດໃນທ້ອງຖິ່ນຢ່າງມີປະສິດຕິຜົນໃນອົງການຈັດຕັ້ງລວມ. ຫຼັງຈາກໂດດດ່ຽວ, ທາດໂປຼຕີນທີ່ຈະຜະລິດອິນຊູລິນແລະ C-peptide ໄດ້ຖືກອະນາໄມດ້ວຍສານ trypsin 5, 8, 10.
ຜົນຂອງ insulin ແລະ C-peptide ຖືກເຮັດໃຫ້ບໍລິສຸດໂດຍ RP-HPLC. ມີຄວາມ ສຳ ຄັນຫຼາຍເມື່ອສ້າງໂຄງສ້າງທີ່ຂົ້ວແມ່ນອັດຕາສ່ວນຂອງມວນສານຂອງທາດໂປຼຕີນຂອງບັນທຸກແລະ polypeptide ເປົ້າ ໝາຍ.
C-peptides ດ້ວຍຄວາມຊ່ວຍເຫຼືອຂອງ spacers ອາຊິດ amino ທີ່ບັນຈຸສະຖານທີ່ ຈຳ ກັດ Sfi I ແລະສານຕົກຄ້າງ arginine ສອງຕົ້ນໃນຕອນເລີ່ມຕົ້ນແລະໃນຕອນທ້າຍຂອງ spacer ສຳ ລັບການຍ່ອຍອາຫານທາດໂປຼຕີນຈາກ trypsin ແມ່ນເຊື່ອມຕໍ່ຕາມຫຼັກການຂອງຫາງ.
HPLC ຂອງຜະລິດຕະພັນການເກັບກູ້ໄດ້ສະແດງໃຫ້ເຫັນວ່າການ ກຳ ຈັດຂອງ C-peptide ໄດ້ຮັບປະລິມານຫຼາຍ, ແລະສິ່ງນີ້ຊ່ວຍໃຫ້ການ ນຳ ໃຊ້ພັນທຸ ກຳ ສັງເຄາະແບບ multimeric ຜະລິດ polypeptides ເປົ້າ ໝາຍ ໃນລະດັບອຸດສາຫະ ກຳ.
ສະຫຼຸບ
ຮາກ, ແລະໃນກໍລະນີຫຼາຍທີ່ສຸດ, ວິທີດຽວທີ່ຈະຮັກສາຊີວິດແລະຄວາມສາມາດໃນການເຮັດວຽກຂອງຄົນເຈັບທີ່ເປັນໂລກເບົາຫວານແມ່ນມາຮອດປະຈຸບັນ, ອິນຊູລິນ.
ກ່ອນທີ່ຈະໄດ້ຮັບແລະແນະ ນຳ ທາດອິນຊູລິນເຂົ້າໃນການປະຕິບັດຕົວຈິງທາງດ້ານການຊ່ວຍ, ຄາດວ່າຜົນໄດ້ຮັບທີ່ເປັນອັນຕະລາຍເຖິງ ໜຶ່ງ ຫຼືສອງປີຈາກການເລີ່ມຕົ້ນຂອງພະຍາດຂອງຄົນເຈັບເບົາຫວານຊະນິດ I, ເຖິງວ່າຈະມີການ ນຳ ໃຊ້ອາຫານທີ່ອ່ອນແອທີ່ສຸດ.
ຜູ້ປ່ວຍເບົາຫວານຊະນິດ I ຕ້ອງການການປິ່ນປົວທົດແທນຕະຫຼອດຊີວິດດ້ວຍການກະກຽມອິນຊູລິນ. ການຢຸດເຊົາຂອງການບໍລິຫານອິນຊູລິນເປັນປົກກະຕິດ້ວຍເຫດຜົນ ໜຶ່ງ ຫຼືອີກຢ່າງ ໜຶ່ງ ເຮັດໃຫ້ການພັດທະນາຂອງອາການແຊກຊ້ອນຢ່າງໄວວາແລະການຕາຍຂອງຄົນເຈັບຢ່າງໄວວາ.
ໃນປະຈຸບັນ, ອັດຕາສ່ວນຂອງໂຣກເບົາຫວານແມ່ນຢູ່ໃນອັນດັບ 3 ຫຼັງຈາກພະຍາດຂອງລະບົບຫຼອດເລືອດຫົວໃຈແລະເນື້ອງອກທີ່ເປັນໂຣກຮ້າຍ. ອັດຕາການເປັນໂຣກເບົາຫວານໃນບັນດາຜູ້ໃຫຍ່, ອີງຕາມອົງການອະນາໄມໂລກ, ໃນພື້ນທີ່ສ່ວນໃຫຍ່ຂອງໂລກແມ່ນ 2-5% ແລະມັກຈະເພີ່ມຂື້ນທຸກໆຄົນ
1. ປີຂອງ ຈຳ ນວນຄົນເຈັບເກືອບສອງເທົ່າ. ຈຳ ນວນຄົນເຈັບທີ່ມີອິນຊູລິນ, ເຖິງວ່າຈະມີຄວາມຄືບ ໜ້າ ຢ່າງຈະແຈ້ງໃນຂົງເຂດການຮັກສາສຸຂະພາບ, ແມ່ນເພີ່ມຂື້ນໃນແຕ່ລະປີ, ແລະປະຈຸບັນຢູ່ປະເທດຣັດເຊຍດຽວມີປະມານ 2 ລ້ານຄົນ.
ວິທີການທີ່ດີທີ່ສຸດໃນການຜະລິດອິນຊູລິນແມ່ນວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ. ອິນຊູລິນທີ່ມີການ ກຳ ເນີດທາງພັນທຸ ກຳ ແມ່ນໄດ້ຮັບໂດຍການຜະລິດສາຍໂສ້ A ແລະ B ແຍກຕ່າງຫາກໂດຍໃຊ້ສາຍພັນຂອງຜູ້ຜະລິດທີ່ແຕກຕ່າງກັນແລະການພັບໂມເລກຸນຕໍ່ມາ, ປະຕິບັດຕາມດ້ວຍການແຍກ isoforms, ແລະການສັງເຄາະຂອງໂປຣຕີນໃນຈຸລັງ E. Coli ດ້ວຍຄວາມສະອາດຂອງມັນດ້ວຍ trypsin ແລະ carboxypeptidase ແລະການຜະລິດອິນຊູລິນ.
ການສ້າງຢາຂອງອິນຊູລິນທີ່ຜະລິດໂດຍເຊື້ອໄວຣັດພາຍໃນປະເທດເຮັດໃຫ້ມີຄວາມເປັນໄປໄດ້ ໃໝ່ ໃນການແກ້ໄຂບັນຫາພະຍາດເບົາຫວານຂອງຣັດເຊຍຫລາຍໆຢ່າງເພື່ອຊ່ວຍຊີວິດຜູ້ເປັນໂລກເບົາຫວານຫລາຍລ້ານຄົນ.
ວັນນະຄະດີ
Balabolkin M.I. , Klebanova E.M. , Kreminskaya V.M. ໂລກເບົາຫວານ: ດ້ານທີ່ທັນສະ ໄໝ ຂອງການບົ່ງມະຕິແລະການຮັກສາ / Doctor, ed. G.L. Vyshkovsky. -2005.- M.: RLS-2005, 2004.- 960 ນ.
Gavrikov, A.V. ການເພີ່ມປະສິດທິພາບການຜະລິດທາງດ້ານເຕັກໂນໂລຢີຊີວະພາບຂອງສານແຊກແຊງຂອງຄົນ: ... ທຽນ. biol. ວິທະຍາສາດ - ມ, 2003
ລະບົບອິນຊູລິນຂອງມະນຸດ. ການເພີ່ມປະສິດທິພາບຂອງການແຍກຕ່າງຫາກແບບຈຸລິນຊີໂດຍໃຊ້ຫຼັກການຂອງຄວາມຫຼາກຫຼາຍ. / Romanchikov A.B. , Yakimov S.A. , Klyushnichenko V.E. , Arutunyan A.M. , Wulfson A.N. // ວິຊາເຄມີຊີວະພາບ, ປີ 1997 - 23, ອັນດັບ 2
Glick B. , Pasternak J. ການຄວບຄຸມການ ນຳ ໃຊ້ວິທີການເຕັກໂນໂລຢີຊີວະພາບ // B. Glick, J. Parsnip / ໂມເລກຸນເຕັກໂນໂລຢີຊີວະພາບ = ໂມເລກຸນເຕັກໂນໂລຢີຊີວະພາບ. - M .: Mir, 2002 .-- S. 517-532. - 589 ນ.
Glick B. , Pasternak J. ໂມເລກຸນເຕັກໂນໂລຢີຊີວະພາບ. ຫຼັກການແລະການ ນຳ ໃຊ້. M.: Mir, ປີ 2002.
Davis R. , Botstein D, Roth J. ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ. ພັນທຸກໍາຂອງເຊື້ອແບັກທີເຣັຍ // R. Davis, D. Botstein, J. Roth / Per. ຈາກພາສາອັງກິດ.-M .: Mir .- 1984.- 176 ໜ້າ.
Ermishin A.P.ອົງການທີ່ມີການປ່ຽນແປງທາງພັນທຸ ກຳ: Myths ແລະຄວາມເປັນຈິງ / A.P. Ermishin // Mn: Tekhnalogaliya.- 2004. - 118 p.
ພື້ນຖານດ້ານເຕັກນິກວິທະຍາສາດການຢາ: ປື້ມແບບຮຽນ / TP Prischep, V.S. Chuchalin, K.L. Zaykov, L.K. ມິຄາລີ. - Rostov-on-Don.: Phoenix, Tomsk: ສຳ ນັກພິມ ຈຳ ໜ່າຍ NTL, 2006.
Patrushev L.I. ລະບົບພັນທຸ ກຳ ທຽມ. // L.I. Patrushev / M. : Nauka.- 2004.
Romanchikov, A.B. ລະບົບອິນຊູລິນຂອງມະນຸດ. ການເພີ່ມປະສິດທິພາບຂອງການແຍກຕ່າງຫາກແບບຈຸລິນຊີໂດຍໃຊ້ຫຼັກການຂອງຄວາມຫຼາກຫຼາຍ. / A.B. Romanchikov ແລະອື່ນໆ.
// ວິຊາເຄມີຊີວະພາບ. ປີ 1997. ສະບັບເລກທີ 2. ປ. . 23
Rybchin V.N. ພື້ນຖານຂອງວິສະວະ ກຳ ພັນທຸ ກຳ // V.N. Rybchin / 2nd ed., ໄດ້ປັບປຸງ ໃໝ່. ແລະເພີ່ມ.: ປື້ມແບບຮຽນ ສຳ ລັບມະຫາວິທະຍາໄລ. SPb: ສຳ ນັກພິມແຫ່ງ SPbSTU. - ປີ 2002 .-- 522 ສ.
Schelkunov S. N. ວິສະວະກໍາພັນທຸກໍາ // Schelkunov S. N. / Novosibirsk: Sib. univ. ສຳ ນັກພິມ ຈຳ ໜ່າຍ ປີ 2008.
Schelkunov, S.N. ວິສະວະ ກຳ ພັນທຸ ກຳ: ປື້ມແບບຮຽນ. ເງິນອຸດ ໜູນ. - ປີທີ 2, ed, Rev. ແລະເພີ່ມ. - Novosibirsk: Sib. univ. ສຳ ນັກພິມ ຈຳ ໜ່າຍ, ປີ 2004 .-- 496 ໜ້າ.
1. ທີ່ຕັ້ງຂອງພັນທະບັດ disulfide ໃນໂມເລກຸນອິນຊູລິນ.
2. ການຈັດການຂອງທາດອາຊິດ amino ໃນການວາງໂມເລກຸນອິນຊູລິນ
ຜົນກະທົບຂອງ insulin ຕໍ່ enzymes ທີ່ ສຳ ຄັນໃນລະບົບຍ່ອຍອາຫານ
ການເຄື່ອນໄຫວຂອງເນື້ອເຍື່ອກ້າມເນື້ອ Adipose 1. Phosphodiesterase 1. Phosphodiesterase 1. LP-lipase
4. ສະລັບສັບຊ້ອນ Pyruvate dehydrogenase
4. ສະລັບສັບຊ້ອນ Pyruvate dehydrogenase
5. Phosphatase glycogen synthase ແລະ glycogen phosphorylase
5. Glycogen synthase phosphatase ຂ. Induction Acetyl-CoA-carboxylase 1. Glucokinase 1. Glyceraldehyde ຟອສເຟດ dehydrogenase
6. ການລະລາຍຂອງທາດ Glucose-6-phosphate dehydrogenase Phosphoenolpyruvate carboxykinase
ຊາວ. 3 ແຜນການຂອງ biosynthesis insulin ໃນຈຸລັງ is ຂອງ islets ຂອງ Langerhans. ER - endicasm reticulum. 1 - ການສ້າງຕັ້ງ peptide ສັນຍານ, 2 - ການສັງລວມຂອງ preproinsulin, 3 - ການ ຊຳ ລະຂອງ peptide ສັນຍານ, 4 - ການຂົນສົ່ງ proinsulin ໄປຍັງເຄື່ອງປະກອບ Golgi, 5 - ການປ່ຽນທາດໂປຼຕີນຈາກ insulin ແລະ C-peptide ແລະການລວມເອົາ insulin ແລະ C-peptide ເຂົ້າໃນເມັດລັບ, 6 - ຄວາມລັບຂອງ insulin ແລະ C peptide.
4. ໂຄງການທົ່ວໄປ ສຳ ລັບການສັງເຄາະອິນຊູລິນຈາກລຸ້ນກ່ອນ
ຊາວ. 5 ການສັງເຄາະອິນຊູລິນໂດຍການສ້າງຕັ້ງສອງຕ່ອງໂສ້ແຍກຕ່າງຫາກ
ວິທີການໃນການໄດ້ຮັບສານອິນຊູລິນຂອງມະນຸດທີ່ຖືກສ້າງຂື້ນໂດຍ ກຳ ມະພັນ

ການປະດິດສ້າງແມ່ນກ່ຽວຂ້ອງກັບຂະ ແໜງ ເຕັກໂນໂລຢີຊີວະພາບ, ແລະໂດຍສະເພາະແມ່ນການຜະລິດອິນຊູລິນຂອງມະນຸດທີ່ໄດ້ຮັບການອອກແບບທາງພັນທຸ ກຳ ສຳ ລັບການຜະລິດຢາທີ່ໃຊ້ໃນການຮັກສາໂລກເບົາຫວານ.
ວິທີການດັ່ງກ່າວແມ່ນປະຕິບັດໂດຍການສ້າງຄວາມເຂັ້ມຂົ້ນຂອງຜູ້ຜະລິດທາດໂປຼຕີນປະສົມທີ່ມີໂປຕີນຂອງມະນຸດ, Escherichia coli BL21 / pPINS07 (BL07) ຫຼື Escherichia coli JM109 / pPINS07, ທຳ ລາຍຈຸລັງໂດຍການແຕກແຍກ, ແຍກຮ່າງກາຍທີ່ປະກອບດ້ວຍທາດໂປຼຕີນປະສົມ.
ຕໍ່ໄປ, ການລ້າງເບື້ອງຕົ້ນຂອງອົງການລວມ, ການລະລາຍຂອງທາດໂປຼຕີນພ້ອມກັນແລະການຟື້ນຟູພັນທະບັດ disulfide ໃນບັຟເຟີທີ່ມີຂະ ໜາດ 5-10 mM dithiothreitol ແລະ 1 mM EDTA ແມ່ນ ດຳ ເນີນ, ການປ່ຽນແປງແລະການ ຊຳ ລະທາດໂປຼຕີນຈາກການແລກປ່ຽນທາດໂປຼຕີນຈາກການແລກປ່ຽນທາດ ion.
ການລ້າງສານສະກັດຈາກທາດໂປຼຕີນປະສົມແມ່ນ ດຳ ເນີນໂດຍການຮ່ວມກັນຂອງ hydrolysis ຂອງ trypsin ແລະ carboxypeptidase B ໃນອັດຕາສ່ວນນ້ ຳ ໜັກ ຂອງໂປຣຕີນປະສົມ, trypsin ແລະ carboxypeptidase B 4000: 0.6: 0.9.
ການເຮັດຄວາມສະອາດຂອງອິນຊູລິນແມ່ນປະຕິບັດໂດຍ chromatography hydrophobic ຫຼືໄລຍະ chromatography ແຫຼວປະສິດທິພາບສູງປະຕິບັດຕາມດ້ວຍການກັ່ນຕອງເຈນ, ແລະການໂດດດ່ຽວຂອງອິນຊູລິນໂດຍການໄປເຊຍກັນໃນການປະກອບດ້ວຍເກືອສັງກະສີ. ການປະດິດສ້າງຊ່ວຍໃຫ້ຫຼຸດຜ່ອນຂັ້ນຕອນໃນການໄດ້ຮັບສານອິນຊູລິນທີ່ໄດ້ຮັບການອອກແບບຈາກມະນຸດແລະເພີ່ມຜົນຜະລິດ
ການປະດິດສ້າງແມ່ນກ່ຽວຂ້ອງກັບຂະ ແໜງ ເຕັກໂນໂລຢີຊີວະພາບ, ໂດຍສະເພາະແມ່ນການຜະລິດອິນຊູລິນຂອງມະນຸດທີ່ມີການ ກຳ ເນີດທາງເຊື້ອພັນ ສຳ ລັບການຜະລິດຢາທີ່ໃຊ້ໃນການຮັກສາໂລກເບົາຫວານ.
ໂດຍ ຄຳ ນຶງເຖິງຜົນ ສຳ ເລັດຕົ້ນຕໍຂອງໂລກເບົາຫວານແລະ ຄຳ ແນະ ນຳ ຂອງອົງການອະນາໄມໂລກ, ບັນດາປະເທດເອີຣົບໃນປີ 2001 ໄດ້ ສຳ ເລັດການຫັນປ່ຽນສູ່ການ ນຳ ໃຊ້ອິນຊູລິນ. ໃນເລື່ອງນີ້, ການພັດທະນາວິທີການຜະລິດອິນຊູລິນໂດຍການ ນຳ ໃຊ້ວິທີການຂອງເຕັກໂນໂລຍີ DNA ທີ່ສົມທົບ ໃໝ່ ແມ່ນວຽກທີ່ເລັ່ງດ່ວນ.
ວິທີການທີ່ມີຊື່ສຽງໃນການຜະລິດອິນຊູລິນຂອງມະນຸດທີ່ມີການ ກຳ ເນີດທາງພັນທຸ ກຳ, ເຊິ່ງປະກອບດ້ວຍການປູກຜູ້ຜະລິດ E. Coli ຜະລິດ proinsulin, ເຊິ່ງບັນຈຸ ລຳ ດັບສອງໂດເມນທີ່ຜູກມັດ IgG ສັງເຄາະຂອງທາດໂປຼຕີນ staphylococcal A.
ວິທີການດັ່ງກ່າວປະກອບດ້ວຍການ ທຳ ລາຍຈຸລັງແບັກທີເລຍ, ການໄດ້ຮັບສານ Taurus ທີ່ປະກອບດ້ວຍ proinsulin, ລະລາຍ Taurus, ທາດ sulfitolysis ຜຸພັງຂອງທາດໂປຼຕີນຊີນ, ການປັບຕົວຂອງມັນ, ການ ຊຳ ລະລ້າງທາດໂປຼຕີນທີ່ລະລາຍໂດຍການສະສົມທາດໂປຼຕິນ, ຄວາມສະອາດຂອງໂປຕີນ Proinsulin ດ້ວຍທາດໂປຣຕີນ proteolytic (trypsin ແລະ carboxypeptidase B) chromatography (Nilson J. , Jonasson P. , Samuelsson E. , Stahl S. , Uhlen M. "ການຜະລິດອິນຊູລິນປະສົມປະສານຂອງມະນຸດແລະ C-peptide ຂອງມັນ", ວາລະສານວິທະຍາສາດເຕັກໂນໂລຢີຊີວະພາບ, ປີ 1996, ຂໍ້ 48, ໜ້າ 241-250) .
ຂໍ້ເສຍປຽບຂອງວິທີການນີ້ແມ່ນຄ່າໃຊ້ຈ່າຍສູງຂອງຜະລິດຕະພັນແລະການ ນຳ ໃຊ້ເຂົ້າໃນການຜະລິດສານສະກັດອິນຊູລິນເຊິ່ງອາດຈະມີຢູ່ໃນຜະລິດຕະພັນເປົ້າ ໝາຍ.
ວິທີການທີ່ເປັນທີ່ຮູ້ຈັກຂອງການຜະລິດອິນຊູລິນໃນການ ກຳ ເນີດທາງພັນທຸ ກຳ, ເຊິ່ງປະກອບດ້ວຍການສ້າງຈຸລັງຂອງຜູ້ຜະລິດສາຍພັນ E.
Coli DN5 a / pVK100, ທຳ ລາຍຈຸລັງແບັກທີເລຍໂດຍການແຍກຕົວຂອງ ultrasonic, ອົງການລວມເຂົ້າແຍກຕ່າງຫາກທີ່ບັນຈຸທາດໂປຼຕີນປະສົມຈາກຄວາມບໍ່ສະອາດໃນການລະລາຍຂອງນ້ ຳ ໂດຍການໃຊ້ສານ centrifugation, ລະລາຍອົງປະກອບທີ່ລວມເຂົ້າໃນ buffer ທີ່ບັນຈຸ 8 M urea, 1 mM dithiothreitol, 0.1 M Tris-HCl, pH 8.0, ເປັນເວລາ 12-16 ຊົ່ວໂມງ.
ຄວາມບໍ່ສະອາດທີ່ລະລາຍແມ່ນຖືກ ກຳ ຈັດໂດຍການສູນກາງ, ຫລັງຈາກນັ້ນຄວາມເຂັ້ມຂົ້ນຂອງ dithiothreitol ແມ່ນເພີ່ມຂື້ນເຖິງ 10 ມມແລະພັນທະບັດ disulfide ຖືກຟື້ນຟູຢູ່ທີ່ 37 ° C ເປັນເວລາ 1 ຊົ່ວໂມງ. ວິທີແກ້ໄຂດັ່ງກ່າວຖືກເຈືອຈາງ 5 ເທື່ອດ້ວຍນ້ ຳ ເຢັນ, ປັບເປັນ pH 4.5 ແລະອົບເປັນເວລາ 2 ຊົ່ວໂມງໃນອຸນຫະພູມ 4 ° C ເພື່ອປະກອບເປັນນ້ ຳ ຝົນ.
precipitate ປະກອບດ້ວຍທາດໂປຼຕີນປະສົມໄດ້ຖືກແຍກອອກໂດຍ centrifugation ແລະ renatured, ຖືກລະລາຍຢ່າງໄວວາໃນນ້ໍາເຢັນໃນລະດັບ pH ຂອງ 10-12, ຫຼັງຈາກນັ້ນມັນຖືກເຈືອຈາງດ້ວຍ 10 mM glycine buffer, pH 10.8, ແລະເກັບຮັກສາໄວ້ໃນອຸນຫະພູມ 4 ° C ໃນຄືນ. ຫຼັງຈາກການລະລາຍຄວາມຮຸນແຮງ, ວິທີແກ້ໄຂແມ່ນຕ້ອງມີການກັ່ນຕອງນ້ ຳ ມັນໃສ່ຖັນ Sephadex G-50 ແລະຖືກລົບລ້າງດ້ວຍຄວາມຍາວ 10 ມມ glycine.
ສ່ວນປະກອບທີ່ມີທາດໂປຼຕີນປະສົມຖືກເກັບ ກຳ, ເຮັດໃຫ້ແຫ້ງ, ແລະແຫ້ງ. ທາດໂປຼຕີນປະສົມທີ່ໄດ້ຮັບແມ່ນລະລາຍໃນ 0.08 M Tris-HCl buffer, pH 7.5, ເຖິງຄວາມເຂັ້ມຂົ້ນຂອງ 10 mg / ml ແລະລ້າງອອກພ້ອມໆກັບ trypsin ແລະ carboxypeptidase B (ອັດຕາສ່ວນຂອງ carboxypeptidase B: trypsin: ທາດໂປຣຕີນ fusion 0.3: 1: 10) ທີ່ 37 ° C ປະມານ 30 ນາທີ.
ຫຼັງຈາກນັ້ນຕື່ມ isopropanol ໃຫ້ 40%. ສ່ວນປະສົມດັ່ງກ່າວແມ່ນໂຄຣມຽມໃນຖັນ DEAE-Sephadex A-25 ແລະປະສົມກັບແບນປ້ອງກັນ 0,55 M Tris-HCl, pH 7.5 ກັບ isopropanol 40% ພ້ອມດ້ວຍເສັ້ນດ່າງເສັ້ນດ່າງ sodium chloride ຈາກ 0 ຫາ 0,1 m, ຫຼັງຈາກເອົາ isopropanol, ຄວາມເຂັ້ມຂົ້ນຂອງ sodium chloride ເພີ່ມຂື້ນເປັນ 25%, ປ່ຽນລະດັບ pH ເປັນ 2.0 ແລະເກັບ ກຳ ຂໍ້ມູນຂອງອິນຊູລິນ.
(Chen J. J.-Q. , Zhang H.-T. , Hu M.-N. , Tang J.-G. , "ການຜະລິດອິນຊູລິນຂອງມະນຸດໃນລະບົບ E. Coli ທີ່ມີທາດໂປຼຕີນຈາກ lys-linsins ຂອງມະນຸດ) ຄາຣະວາກ່ອນ "ການ ນຳ ໃຊ້ຊີວະວິທະຍາແລະເຕັກໂນໂລຊີຊີວະພາບ, ປີ 1995, ຂໍ້ 55, ໜ້າ 5-15).
ຂໍ້ເສຍປຽບຂອງວິທີການນີ້ປະກອບມີການ ນຳ ໃຊ້ການກັ່ນຕອງນ້ ຳ ໃນໄລຍະເລີ່ມຕົ້ນ, ເຊິ່ງຮຽກຮ້ອງໃຫ້ມີປະລິມານທີ່ ໜ້າ ວິຕົກກັງວົນແລະ ຈຳ ນວນຫຼາຍຂອງເອນໄຊທີ່ ນຳ ໃຊ້ໃນການ ທຳ ລາຍທາດໂປຼຕີນປະສົມ.
ວິທີການທີ່ມີຊື່ສຽງໃນການຜະລິດອິນຊູລິນຂອງມະນຸດທີ່ໄດ້ຮັບການ ກຳ ເນີດທາງພັນທຸ ກຳ, ປະກອບດ້ວຍການປູກຝູງຜູ້ຜະລິດ Escherichia coli JM109 / pPINS07, ທຳ ລາຍຈຸລັງແບັກທີເຣຍໂດຍການແຕກແຍກ, ແຍກຮ່າງກາຍທີ່ບັນຈຸທາດໂປຼຕີນປະສົມ, ລະລາຍໃນທາດປ້ອງກັນທີ່ມີທາດຢູເຣນຽມແລະ dithiothreitol, ການປ່ຽນຊື່ແລະການກັ່ນຕອງຂອງທາດໂປຼຕີນປະສົມທີ່ມີຊື່ສຽງ. precipitation ຂອງທາດປະສົມທີ່ບໍ່ສະອາດໃນ isopropanol 40% ປະຕິບັດຕາມໂດຍ chromatography ກ່ຽວກັບ KM-sepharose, ການລ້າງມົນລະພິດຕາມລໍາດັບຂອງມັນກັບ trypsin ແລະ carboxypeptidase B, ໃນຂະນະທີ່ຜະລິດຕະພັນ trypsinolysis ແມ່ນໂຄຣມຽມໃນ SP-Sepharose, ສົມທຽບກັບ 0.03-0.1 M ammonium acetate buffer pH 5.0-6.0 ບັນຈຸທາດຢູເຣນຽມ 6 M, ມີທາດໂປຼຕີນຈາກການຕັດທາດໂປຼຕີນຈາກທາດໂຊດຽມ sodium chloride ຈາກ 0 ຫາ 0.5 M ໃນຕອນເລີ່ມຕົ້ນ buffer, ແລະສ່ວນປະກອບຂອງ insulin ທີ່ໄດ້ຮັບຫຼັງຈາກການຖອກດ້ວຍ carboxypeptidase B ໄດ້ຖືກເຮັດໃຫ້ບໍລິສຸດໂດຍໄລຍະ chromatography ແຫຼວທີ່ມີປະສິດຕິພາບສູງ (RP HPLC) ປະຕິບັດຕາມດ້ວຍການກັ່ນຕອງເຈນ (Pat. RF No. 2141531, MKI C12P 21/02, ເຜີຍແຜ່). ປີ 1999)
ຂໍ້ເສຍປຽບຂອງວິທີການລວມມີການ ນຳ ໃຊ້ສານລະລາຍອູຣິດແລະສານອິນຊີໃນປະລິມານທີ່ ສຳ ຄັນໃນຂັ້ນຕອນຂອງການເຮັດຄວາມສະອາດຂອງທາດໂປຼຕີນປະສົມ.
ຜູ້ຊ່ຽວຊານດ້ານໂລກເບົາຫວານ

ກ່ອນການ ນຳ ໃຊ້ອິນຊູລິນ, ອາຍຸຍືນຂອງຜູ້ປ່ວຍທີ່ເປັນໂຣກເບົາຫວານແມ່ນບໍ່ເກີນ 10 ປີ. ການປະດິດສ້າງຂອງຢານີ້ໄດ້ຊ່ວຍຄົນເຈັບຫຼາຍລ້ານຄົນ. ອິນຊູລິນວິສະວະ ກຳ ພັນທຸ ກຳ ຂອງມະນຸດແມ່ນຄວາມກ້າວ ໜ້າ ໃໝ່ ຫຼ້າສຸດໃນວິທະຍາສາດ.
ຜົນຂອງການເຮັດວຽກ ໜັກ ຫຼາຍປີ
ກ່ອນການປະດິດສ້າງວິສະວະ ກຳ ພັນທຸ ກຳ (ກຳ ລັງຜະລິດ) ກະຕຸ້ນອິນຊູລິນແຍກອອກຈາກຝູງງົວແລະ ໝູ.
ຄວາມແຕກຕ່າງລະຫວ່າງອິນຊູລິນແລະມະນຸດແມ່ນພຽງແຕ່ກົດອາມິໂນພຽງ ໜຶ່ງ ດຽວ
ຂໍ້ເສຍປຽບຂອງວິທີການໃນການຮັບຢາ:
- ຄວາມສັບສົນໃນການເກັບຮັກສາແລະການຂົນສົ່ງວັດຖຸດິບທາງຊີວະພາບ,
- ຂາດສັດລ້ຽງ
- ຄວາມຫຍຸ້ງຍາກຕ່າງໆທີ່ກ່ຽວຂ້ອງກັບການຈັດສັນແລະການ ຊຳ ລະຮໍໂມນຂອງ pancreatic,
- ຄວາມສ່ຽງສູງຂອງອາການແພ້.
ດ້ວຍການສັງເຄາະອິນຊູລິນຂອງມະນຸດ ທຳ ມະຊາດໃນທາດແຫຼວຊີວະພາບໃນປີ 1982, ຍຸກສະ ໄໝ ໃໝ່ ທາງດ້ານເຕັກໂນໂລຢີຊີວະພາບໄດ້ເລີ່ມຕົ້ນ. ຖ້າໃນເວລາອາລຸນຂອງການປິ່ນປົວດ້ວຍອິນຊູລິນ, ເປົ້າ ໝາຍ ຂອງນັກວິທະຍາສາດແມ່ນພຽງແຕ່ການຢູ່ລອດຂອງຄົນເຈັບ, ໃນເວລາຂອງພວກເຮົາການພັດທະນາຢາ ໃໝ່ ແມ່ນແນໃສ່ເພື່ອບັນລຸການຊົດເຊີຍທີ່ຍືນຍົງ ສຳ ລັບພະຍາດ. ເປົ້າ ໝາຍ ຫຼັກຂອງການຄົ້ນຄວ້າວິທະຍາສາດແມ່ນເພື່ອປັບປຸງຄຸນນະພາບຊີວິດຂອງຄົນເຈັບທີ່ເປັນໂລກເບົາຫວານ.
ເຕັກໂນໂລຢີທີ່ທັນສະ ໄໝ
ປະເພດຢາ, ຂື້ນກັບວິທີການກະກຽມ:
| ວິສະວະ ກຳ ທາງພັນທຸ ກຳ Recombinant | ສຳ ລັບການຜະລິດ, E. coli ທີ່ຖືກດັດແປງພັນທຸ ກຳ ແມ່ນຖືກ ນຳ ໃຊ້.
| ຄົນທີ່ມັກທີ່ສຸດຂອງນັກພັນທຸ ກຳ ພັນພັນທຸ ກຳ ແມ່ນ E. coli |
| ດັດແກ້ພັນທຸ ກຳ | ອຸປະກອນການເລີ່ມຕົ້ນແມ່ນອິນຊູລິນ. ມັນຖືກດັດແປງໂດຍວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ. | ໂຄງປະກອບຮໍໂມນ |
| ສັງເຄາະ | ຢາທີ່ຖືກສັງເຄາະແບບປອມ, ໃນສ່ວນປະກອບຂອງມັນແມ່ນຄ້າຍຄືກັນກັບທາດອິນຊູລິນ. | ການຜະລິດຢາ |
ມີຫຍັງເກີດຂື້ນໃນຮ່າງກາຍຫລັງຈາກໃຊ້ຢາ?
ເຊື່ອມຕໍ່ກັບຕົວຮັບຂອງເຍື່ອຫ້ອງ, ອິນຊູລິນປະກອບເປັນສະລັບສັບຊ້ອນທີ່ປະຕິບັດຂັ້ນຕອນຕໍ່ໄປນີ້:
- ປັບປຸງການຂົນສົ່ງນ້ ຳ ຕານເຂົ້າສູ່ລະບົບແລະຊ່ວຍໃນການດູດຊຶມຂອງມັນ.
- ກະຕຸ້ນການປ່ອຍທາດເອນໄຊທີ່ມີສ່ວນຮ່ວມໃນການປຸງແຕ່ງນ້ ຳ ຕານ.
- ມັນຫຼຸດຜ່ອນອັດຕາການສ້າງ glycogen ໃນຕັບ.
- ກະຕຸ້ນການເຜົາຜະຫລານໄຂມັນແລະໂປຕີນ.
ໃນກໍລະນີຂອງການບໍລິຫານ subcutaneous, insulin ເລີ່ມປະຕິບັດໃນ 20-25 ນາທີ. ໄລຍະເວລາຂອງຢາຈາກ 5 ເຖິງ 8 ຊົ່ວໂມງ. ມັນຖືກກັກຂັງຕື່ມອີກໂດຍສານອິນຊູລິນ insulinase ແລະຂັບອອກມາໃນຍ່ຽວ. ຢາບໍ່ໄດ້ຂ້າມແຮ່ແລະບໍ່ຜ່ານເຂົ້າໄປໃນນົມແມ່.
ໃນເວລາທີ່ insulin ແມ່ນເຄື່ອງຈັກກໍາເນີດໂດຍກໍາມະພັນ?
ຖ້າຕ້ອງການຄວາມຊ່ວຍເຫຼືອດ່ວນ
ຢາອິນຊູລິນທີ່ອອກແບບໂດຍ ກຳ ມະພັນແມ່ນໃຊ້ໃນກໍລະນີຕໍ່ໄປນີ້:
- ໂຣກເບົາຫວານປະເພດ 1 ຫລືຊະນິດ 2. ມັນຖືກນໍາໃຊ້ເປັນການປິ່ນປົວເອກະລາດຫຼືປະສົມປະສານກັບຢາອື່ນໆ.
- ດ້ວຍຄວາມຕ້ານທານຕໍ່ຕົວແທນການອັກເສບໃນປາກ.
- ເປັນໂລກເບົາຫວານໃນແມ່ຍິງຖືພາ.
- ໃນກໍລະນີທີ່ມີອາການແຊກຊ້ອນຈາກ ໝາກ ໄຂ່ຫຼັງແລະຕັບ.
- ເມື່ອປ່ຽນໄປໃຊ້ອິນຊູລິນທີ່ເຮັດວຽກເປັນເວລາດົນ.
- ໃນໄລຍະເວລາ preoperative.
- ໃນກໍລະນີທີ່ມີເງື່ອນໄຂອັນຕະລາຍຕໍ່ຊີວິດ (hyperosmolar ຫຼື ketoacidotic coma).
- ໃນສະຖານະການສຸກເສີນ (ກ່ອນເກີດລູກ, ມີການບາດເຈັບ).
- ຖ້າມີໂຣກຜິວ ໜັງ ທີ່ເປັນໂຣກຕັບແຂງ (ເປັນແຜ, ເປັນຕຸ່ມຄັນ).
- ການປິ່ນປົວໂຣກເບົາຫວານຕ້ານກັບພື້ນຫລັງຂອງການຕິດເຊື້ອ.
ອິນຊູລິນວິສະວະ ກຳ ພັນທຸ ກຳ ຂອງມະນຸດມີຄວາມທົນທານໄດ້ດີແລະບໍ່ກໍ່ໃຫ້ເກີດປະຕິກິລິຍາແພ້, ເພາະມັນຄ້າຍຄືກັນກັບຮໍໂມນ ທຳ ມະຊາດ.
ການຕິດຕາມກວດກາຄົງທີ່ແມ່ນ ສຳ ຄັນ!
ມັນຖືກຫ້າມບໍ່ໃຫ້ສັ່ງຢາໃນກໍລະນີ:
- ເຮັດໃຫ້ນ້ ຳ ຕານໃນເລືອດຫຼຸດລົງ
- hypersensitivity ກັບຢາ.
ໃນມື້ ທຳ ອິດຫລັງຈາກນັດພົບຢາ, ຕ້ອງມີການຕິດຕາມຄົນເຈັບຢ່າງລະມັດລະວັງ.
ຜົນຂ້າງຄຽງ
ອັນຕະລາຍ Urticaria! ອາການປວດຫລັງຂອງ Quincke!
ໃນກໍລະນີທີ່ຫາຍາກ, ໃນເວລາທີ່ໃຊ້ insulin, ອາການແຊກຊ້ອນດັ່ງຕໍ່ໄປນີ້ແມ່ນເປັນໄປໄດ້:
- ຕິກິລິຍາແພ້ (urticaria, ໂຣກ edin Quincke, ອາການຄັນຂອງຜິວຫນັງ),
- ການຫຼຸດລົງຢ່າງຫຼວງຫຼາຍຂອງນ້ ຳ ຕານໃນເລືອດ (ມີການພັດທະນາຍ້ອນການປະຕິເສດຂອງຢາໂດຍຮ່າງກາຍຫຼືໃນກໍລະນີທີ່ມີຂໍ້ຂັດແຍ່ງທາງພູມຕ້ານທານ),
- ສະຕິເສີຍ
- ໃນກໍລະນີທີ່ຮຸນແຮງ, ການພັດທະນາຂອງສະມອງເລືອດທີ່ເປັນໄປໄດ້,
- ຫິວ, ປາກແຫ້ງ, ເຫງົານອນ, ການສູນເສຍຄວາມຢາກອາຫານ,
- hyperglycemia (ໃນເວລາທີ່ໃຊ້ຢາຕ້ານກັບພື້ນຫລັງຂອງການຕິດເຊື້ອຫຼືໄຂ້),
- ຜິວ ໜ້າ ແດງ
- ປະຕິກິລິຍາທ້ອງຖິ່ນໃນເຂດບໍລິຫານ (ການເຜົາຜານ, ອາການຄັນ, ການຫົດຕົວຫລືການແຜ່ຂະຫຍາຍຂອງໄຂມັນ subcutaneous).
ບາງຄັ້ງການປັບຕົວເຂົ້າກັບຢາແມ່ນປະກອບດ້ວຍຄວາມຜິດປົກກະຕິເຊັ່ນ: ໃຄ່ບວມແລະພິການທາງສາຍຕາ. ການສະແດງເຫຼົ່ານີ້ມັກຈະຫາຍໄປຫຼັງຈາກສອງສາມອາທິດ.
ວິທີການຊອກຫາອິນຊູລິນທີ່ມີການ ກຳ ເນີດທາງພັນທຸ ກຳ ໃນຮ້ານຂາຍຢາ?
ຢາມີຢູ່ໃນຮູບແບບຂອງການແກ້ໄຂ ສຳ ລັບການບໍລິຫານພໍ່ແມ່:
| "Biosulin" | ໄລຍະເວລາສະເລ່ຍຂອງການປະຕິບັດ |
| Actrapid | ການສະແດງອິນຊູລິນສັ້ນ |
| Gensulin | ການກະກຽມ Biphasic (ປະສົມປະສານຂອງ insulins ໄລຍະສັ້ນແລະກາງ) |
| Rinsulin | ຜົນໄວ |
| ມະນຸດສາດ | ປາກກາ syringe ແມ່ນໃຊ້ໃນການບໍລິຫານຢາ. |
ມັນບໍ່ຍາກທີ່ຈະເລືອກການກະກຽມອິນຊູລິນໂດຍ ຄຳ ນຶງເຖິງຄຸນລັກສະນະສ່ວນຕົວຂອງຄົນເຈັບ.
ເງື່ອນໄຂການ ນຳ ໃຊ້
ສ່ວນຫຼາຍມັກ, ການບໍລິຫານ subulinaneous ຂອງ insulin ແມ່ນຖືກ ນຳ ໃຊ້.
ໃນກໍລະນີທີ່ຮີບດ່ວນ, ຢາດັ່ງກ່າວຈະຖືກຄຸ້ມຄອງຢ່າງເຂັ້ມງວດ.
ໃນສະພາບຮ້າຍແຮງຂອງຄົນເຈັບ
ແມ່ນແຕ່ຜູ້ເປັນໂລກເບົາຫວານທີ່ມີປະສົບການກໍ່ສາມາດເຮັດຜິດໄດ້ໃນເວລາທີ່ໃຊ້ຢາ.
ເພື່ອຫລີກລ້ຽງອາການແຊກຊ້ອນ, ມັນ ຈຳ ເປັນ:
- ກ່ອນການ ນຳ ໃຊ້, ໃຫ້ກວດເບິ່ງວັນ ໝົດ ອາຍຸຂອງຢາ.
- ປະຕິບັດຕາມ ຄຳ ແນະ ນຳ ໃນການເກັບຮັກສາ: ຕູ້ເກັບມ້ຽນທີ່ຄວນມີຄວນເກັບມ້ຽນໄວ້ໃນຕູ້ເຢັນ. ກະປdevelopedອງທີ່ພັດທະນາແລ້ວສາມາດເກັບຮັກສາໄວ້ໃນອຸນຫະພູມຫ້ອງໃນບ່ອນມືດ.
- ໃຫ້ແນ່ໃຈວ່າທ່ານຕ້ອງຈື່ ຈຳ ໄວ້ໃນປະລິມານທີ່ຖືກຕ້ອງ: ອ່ານໃບສັ່ງແພດຂອງທ່ານ ໝໍ ອີກເທື່ອ ໜຶ່ງ.
- ກ່ອນທີ່ຈະສີດ, ມັນຈໍາເປັນຕ້ອງປ່ອຍອາກາດຈາກ syringe.
- ຜິວຫນັງຄວນສະອາດ, ແຕ່ວ່າມັນເປັນສິ່ງທີ່ບໍ່ຕ້ອງການທີ່ຈະໃຊ້ເຫຼົ້າໃນການປຸງແຕ່ງ, ເພາະວ່າມັນຊ່ວຍຫຼຸດປະສິດທິພາບຂອງຢາ.
- ເລືອກສະຖານທີ່ສັກຢາທີ່ດີທີ່ສຸດ. ເມື່ອແນະ ນຳ ພາຍໃຕ້ຜິວ ໜັງ ຂອງທ້ອງ, ຢາຈະເຮັດໄດ້ໄວຂື້ນ. ການດູດຊືມອິນຊູລິນຊ້າລົງເມື່ອແນະ ນຳ ເຂົ້າໄປໃນພັບຫລືບ່າໄຫລ່.
- ໃຊ້ບໍລິເວນພື້ນຜິວທັງ ໝົດ (ປ້ອງກັນອາການແຊກຊ້ອນໃນທ້ອງຖິ່ນ). ໄລຍະຫ່າງລະຫວ່າງການສັກຢາຄວນຈະເປັນຢ່າງ ໜ້ອຍ 2 ຊມ.
- ລອກຜິວ ໜັງ ໃນຈຸດເພີ່ມຂື້ນເພື່ອຫຼຸດຜ່ອນຄວາມສ່ຽງທີ່ຈະເຂົ້າໄປໃນກ້າມເນື້ອ.
- ສັກເຂັມໃສ່ໃຕ້ຜິວ ໜັງ ຢູ່ໃນມຸມເພື່ອບໍ່ໃຫ້ຢາບໍ່ຮົ່ວໄຫຼ.
- ໃນເວລາທີ່ຖືກສັກເຂົ້າໄປໃນກະເພາະອາຫານ, ອິນຊູລິນທີ່ເຮັດສັ້ນໆແມ່ນໃຊ້ 20 ນາທີກ່ອນອາຫານ. ໃນກໍລະນີຂອງການເລືອກບ່າຫລືກົ້ນ - ສາມສິບນາທີກ່ອນອາຫານ.
ການປະສົມປະສານກັບຢາອື່ນໆ
ສ່ວນຫຼາຍມັກເປັນໂລກເບົາຫວານ, ຄົນເຈັບກິນຢາຫຼາຍໆຊະນິດ. ການປະສົມປະສານກັບຢາຊະນິດອື່ນສາມາດສົ່ງຜົນກະທົບຕໍ່ການປິ່ນປົວຂອງອິນຊູລິນທີ່ໄດ້ຮັບການ ກຳ ເນີດທາງພັນທຸ ກຳ.
ເພື່ອປ້ອງກັນອາການແຊກຊ້ອນ, ທ່ານ ຈຳ ເປັນຕ້ອງຮູ້:
| ເພີ່ມຜົນກະທົບຂອງອິນຊູລິນທີ່ຖືກສ້າງຂື້ນໂດຍ ກຳ ມະພັນໂດຍການຫຼຸດນ້ ຳ ຕານໃນເລືອດ |
| ຢາຊະນິດ ໜຶ່ງ ທີ່ນິຍົມໃຊ້ໃນການຮັກສາການຕິດເຊື້ອທາງເດີນປັດສະວະ Doxycycline |
| ຫຼຸດຜ່ອນການກະ ທຳ ຂອງອິນຊູລິນ |
| ເອົາໃຈໃສ່! |
ກິນເພາະຖ້າກິນ
ໃນບາງກໍລະນີ, ການບໍລິຫານອິນຊູລິນເຮັດໃຫ້ນ້ ຳ ຕານໃນເລືອດຫຼຸດລົງຢ່າງກະທັນຫັນ. ບັນຫານີ້ມັກຈະເກີດຂື້ນຍ້ອນການເລືອກປະລິມານທີ່ບໍ່ຖືກຕ້ອງ.
ອາການເບື້ອງຕົ້ນຂອງການເປັນພະຍາດລະລາຍໃນເລືອດ:
- ຈຸດອ່ອນ
- pallor ຂອງຜິວຫນັງ
- ລັດກັງວົນ
- ວິນຫົວ
- ຄວາມເສີຍເມີຍ
- ແຂນຂາ, ລີ້ນ, ລີ້ນແລະສົບ,
- ແຂນສັ່ນ
- ເຫື່ອເຢັນ
- ຄວາມຮູ້ສຶກຫິວໂຫຍຢ່າງແຮງ
- ເຈັບຫົວ.
ຄວາມເສີຍຫາຍ; ຄວາມເສື່ອມໂຊມຢ່າງກະທັນຫັນໃນສະຫວັດດີພາບ
ຖ້າທ່ານສັງເກດເຫັນອາການດັ່ງກ່າວໃນຕົວທ່ານເອງ, ທ່ານ ຈຳ ເປັນຕ້ອງກິນອາຫານທີ່ມີທາດແປ້ງທີ່ຍ່ອຍໄດ້ງ່າຍ. ມັນສາມາດເປັນ cookies, ເຂົ້າ ໜົມ, ເຂົ້າ ໜົມ ້ ຳ ຕານຫລືເຂົ້າຈີ່ຂາວ. ຊາຫວານຊ່ວຍໃນສະຖານະການດັ່ງກ່າວ.
ຖ້າສະພາບການຊຸດໂຊມລົງ, ທ່ານຕ້ອງໂທຫາລົດສຸກເສີນ. ການເປັນໂລກເບົາຫວານອາດຈະເຮັດໃຫ້ຄົນເຈັບ ໝົດ ສະຕິຫຼືເສຍຊີວິດ.
ການໃສ່ອິນຊູລິນເປັນອັນຕະລາຍບໍ?
ສະບາຍດີ insulin Recombinant ບໍ່ແຕກຕ່າງຈາກ ທຳ ມະຊາດ. ເພື່ອໄດ້ຮັບມັນ, ເຊື້ອແບັກທີເຣັຍທີ່ຖືກດັດແປງພັນທຸ ກຳ ແມ່ນຖືກ ນຳ ໃຊ້.
ໂດຍ ນຳ ໃຊ້ເຕັກໂນໂລຢີດ້ານວິສະວະ ກຳ ທາງພັນທຸ ກຳ, ຕົວແທນ DNA ທີ່ມີເຊື້ອສາຍອິນຊູລິນຖືກຝັງເຂົ້າໃນຈຸລັງຂອງ E. coli. ສິ່ງມີຊີວິດທີ່ມີການປ່ຽນແປງທາງພັນທຸ ກຳ ແມ່ນຄູນແລະຜະລິດຮໍໂມນ. ຢາດັ່ງກ່າວມີປະສິດຕິຜົນສູງແລະມີລະດັບຄວາມບໍລິສຸດສູງ.
ອິນຊູລິນ ພາກທີ II ການຜະລິດອິນຊູລິນຈຸລິນຊີ

ອົງປະກອບ affinity - ຢ່າງຫຼວງຫຼາຍອໍານວຍຄວາມສະດວກໃຫ້ໂດດດ່ຽວຂອງທາດໂປຼຕີນປະສົມ.
ໃນກໍລະນີນີ້, ທັງສອງສ່ວນຂອງສ່ວນປະກອບເຫຼົ່ານີ້ສາມາດ ນຳ ສະ ເໜີ ພ້ອມກັນໃນສ່ວນປະກອບຂອງທາດໂປຼຕີນປະສົມ.
ນອກຈາກນັ້ນ, ໃນເວລາທີ່ສ້າງໂປຣຕີນປະສົມ, ຫຼັກການຂອງຫຼາຍຮູບແບບສາມາດ ນຳ ໃຊ້ໄດ້ (ນັ້ນແມ່ນ polypeptide ເປົ້າ ໝາຍ ຫຼາຍສະບັບທີ່ມີຢູ່ໃນທາດໂປຼຕີນປະສົມ) ເຊິ່ງສາມາດເພີ່ມຜົນຜະລິດຂອງຜະລິດຕະພັນເປົ້າ ໝາຍ ຢ່າງຫຼວງຫຼາຍ.
2 ການສະແດງອອກຂອງທາດໂປຣຕີນໃນຈຸລັງ E. coli ..
ໃນການເຮັດວຽກ, ຜູ້ຂຽນໄດ້ໃຊ້ສາຍພັນ JM 109 N1864 ດ້ວຍການຈັດລຽງ ລຳ ດັບ nucleotide ເຂົ້າໄປໃນ plasmid ສະແດງທາດໂປຼຕີນປະສົມ, ເຊິ່ງປະກອບດ້ວຍທາດໂປຣຕີນເສັ້ນແລະສ່ວນຂອງທາດໂປຼຕີນ Staphylococcus aureus A ຕິດກັບທາດ N-terminus ຂອງມັນຜ່ານທາດເສດ methionine.
ການປູກຝັງຂອງເຊື້ອໄຟຊີວະພາບທີ່ອີ່ມຕົວຂອງຈຸລັງຂອງສາຍພັນທີ່ສົມບູນແບບເຮັດໃຫ້ການເລີ່ມຕົ້ນຂອງການຜະລິດໂປຣຕີນປະສົມ, ການໂດດດ່ຽວແລະການຫັນເປັນ ລຳ ດັບເຊິ່ງໃນທໍ່ ນຳ ໄປສູ່ການເຮັດອິນຊູລິນ.
ນັກຄົ້ນຄວ້າອີກກຸ່ມ ໜຶ່ງ ໄດ້ຮັບທາດໂປຼຕີນທີ່ສົມບູນໃນລະບົບການສະແດງອອກຂອງແບັກທີເລຍຂອງທາດປະສົມທີ່ປະກອບດ້ວຍໂປຣຕີນຂອງມະນຸດແລະຫາງ polyhistidine ຕິດຢູ່ໃນມັນໂດຍຜ່ານສານຕົກຄ້າງ methionine. ມັນຖືກແຍກອອກໄປໂດຍການໃຊ້ຊິລິໂຄນທຽມໃນຖັນ Ni-agarose ຈາກອົງການຈັດຕັ້ງລວມແລະຍ່ອຍດ້ວຍສານຊີເມັນ Bromide.
ການສ້າງແຜນທີ່ແລະການວິເຄາະສັງເຄາະມະຫາສານກ່ຽວກັບທາດໂປຼຕິນທີ່ໄດ້ຮັບທີ່ບໍລິສຸດໂດຍ chromatography ແລກປ່ຽນທາດ ion ໃສ່ນ້ ຳ ຢາງແລກປ່ຽນ anion ແລະ RP (ໄລຍະປີ້ນກັບກັນ) HPLC (chromatography ແຫຼວທີ່ມີປະສິດຕິພາບສູງ) ໄດ້ສະແດງໃຫ້ເຫັນການມີຂອງຂົວ disulfide ທີ່ສອດຄ້ອງກັບຂົວ disulfide ຂອງ proinsulin ຂອງມະນຸດ. ເອກະສານລາຍງານກ່ຽວກັບການພັດທະນາວິທີການ ໃໝ່ ທີ່ມີການປັບປຸງ ໃໝ່ ໃນການຜະລິດອິນຊູລິນຂອງມະນຸດໂດຍວິສະວະ ກຳ ທາງພັນທຸ ກຳ ໃນຈຸລັງ prokaryotic. ຜູ້ຂຽນພົບວ່າຜົນຂອງ insulin ໃນໂຄງສ້າງແລະກິດຈະ ກຳ ທາງຊີວະວິທະຍາຂອງມັນແມ່ນຄ້າຍຄືກັນກັບຮໍໂມນທີ່ແຍກອອກມາຈາກກະຕ່າຍ.
ບໍ່ດົນມານີ້, ໄດ້ມີການເອົາໃຈໃສ່ຢ່າງໃກ້ຊິດໃນການເຮັດຂັ້ນຕອນງ່າຍໆໃນການຜະລິດອິນຊູລິນໂດຍວິສະວະ ກຳ ທາງພັນທຸ ກຳ. ດັ່ງນັ້ນ, ຜູ້ຂຽນໄດ້ຮັບທາດໂປຼຕີນຈາກການປະສົມປະສານທີ່ປະກອບດ້ວຍ peptide ຜູ້ນໍາຂອງ interleukin 2 ຕິດກັບ N-terminus ຂອງ proinsulin ຜ່ານທາດເສດເຫຼືອຂອງ lysine.
ທາດໂປຼຕີນດັ່ງກ່າວໄດ້ຖືກສະແດງອອກຢ່າງມີປະສິດຕິພາບແລະທ້ອງຖິ່ນໃນອົງການຈັດຕັ້ງລວມ. ຫຼັງຈາກໂດດດ່ຽວ, ທາດໂປຼຕີນໄດ້ຖືກຍ່ອຍດ້ວຍ trypsin ເພື່ອຜະລິດອິນຊູລິນແລະ C-peptide. ນັກຄົ້ນຄວ້າອີກກຸ່ມ ໜຶ່ງ ປະຕິບັດແບບດຽວກັນນີ້.
ທາດໂປຼຕີນປະສົມທີ່ປະກອບດ້ວຍ proinsulin ແລະສອງໂດເມນສັງເຄາະຂອງ staphylococcus ທາດ IgG ທີ່ຜູກມັດທາດໂປຼຕີນໄດ້ຖືກທ້ອງຖິ່ນໃນອົງການລວມ, ແຕ່ມີລະດັບການສະແດງອອກທີ່ສູງກວ່າ. ທາດໂປຼຕີນດັ່ງກ່າວໄດ້ຖືກແຍກອອກໂດຍ chromatography ທີ່ມີຄວາມເປັນເອກະພາບໂດຍໃຊ້ IgG ແລະປຸງແຕ່ງດ້ວຍ trypsin ແລະ carboxypeptidase B.
ຜົນຂອງ insulin ແລະ C-peptide ໄດ້ຖືກເຮັດໃຫ້ບໍລິສຸດໂດຍ RP HPLC. ໃນເວລາທີ່ສ້າງໂຄງສ້າງທີ່ຫລອກລວງ, ອັດຕາສ່ວນມະຫາຊົນຂອງທາດໂປຼຕີນຂອງບັນທຸກແລະ polypeptide ເປົ້າ ໝາຍ ແມ່ນມີຄວາມ ສຳ ຄັນຫຼາຍ.
ດັ່ງນັ້ນ, ວຽກງານດັ່ງກ່າວໄດ້ອະທິບາຍເຖິງການກໍ່ສ້າງໂຄງສ້າງຂອງການປະສົມ, ບ່ອນທີ່ໂປຕີນຂອງທາດໂປຼຕີນຈາກທາດໂປຼຕີນຂອງມະນຸດຖືກນໍາໃຊ້ເປັນ polypeptide ບັນທຸກ. ຫນຶ່ງ, ສາມແລະເຈັດ C-peptides ຖືກຕິດຢູ່ກັບມັນ.
C-peptides ໄດ້ຖືກເຊື່ອມຕໍ່ບົນພື້ນຖານຂອງຫົວ - ຫາງໂດຍໃຊ້ spacers ອາຊິດ amino ທີ່ບັນຈຸສະຖານທີ່ ຈຳ ກັດ Sfi I ແລະສານຕົກຄ້າງ arginine ສອງຕົ້ນໃນຕອນຕົ້ນແລະໃນຕອນທ້າຍຂອງ spacer ສຳ ລັບການແບ່ງທາດໂປຼຕີນຕໍ່ໆໄປກັບ trypsin. HPLC ຂອງຜະລິດຕະພັນການເກັບກູ້ໄດ້ສະແດງໃຫ້ເຫັນວ່າການ ກຳ ຈັດທາດ C-peptide ແມ່ນມີປະລິມານຫຼາຍ, ແລະນີ້ຊ່ວຍໃຫ້ການ ນຳ ໃຊ້ພັນທຸ ກຳ ສັງເຄາະແບບ multimeric ໄດ້ຮັບ polypeptides ເປົ້າ ໝາຍ ໃນລະດັບອຸດສາຫະ ກຳ.
ວຽກງານດັ່ງກ່າວໄດ້ອະທິບາຍເຖິງການກຽມຕົວຂອງໂປຣຕິນ proinsulin ເຊິ່ງມີການທົດແທນ Arg32Tyr. ໃນເວລາທີ່ທາດໂປຼຕີນນີ້ໄດ້ຖືກຮ່ວມກັນກັບ trypsin ແລະ carboxypeptidase B, insulin ພື້ນເມືອງແລະ C-peptide ທີ່ບັນຈຸສານເສດເຫຼືອ tyrosine ກໍ່ຕັ້ງຂຶ້ນ. ສຸດທ້າຍ, ຫຼັງຈາກຕິດປ້າຍ 125I, ຖືກ ນຳ ໃຊ້ຢ່າງຈິງຈັງໃນ radioimmunoassay. 3 ຄວາມບໍລິສຸດຂອງອິນຊູລິນ.
Insulin ມີຈຸດປະສົງໃນການຜະລິດຢາຕ້ອງມີຄວາມບໍລິສຸດສູງ. ດັ່ງນັ້ນ, ການຄວບຄຸມຄວາມບໍລິສຸດຂອງຜະລິດຕະພັນທີ່ໄດ້ຮັບໃນແຕ່ລະຂັ້ນຕອນຂອງການຜະລິດແມ່ນມີຄວາມ ຈຳ ເປັນສູງ. ກ່ອນ ໜ້າ ນີ້, RP ແລະ IO (ການແລກປ່ຽນທາດ ion) HPLC ໄດ້ຖືກ ນຳ ໃຊ້ເພື່ອຄຸນລັກສະນະຂອງ proinsulin-S-sulfonate, proinsulin, ສ່ວນບຸກຄົນ A- ແລະ B-chains, ແລະ S-sulfonates.
ຄວາມສົນໃຈໂດຍສະເພາະແມ່ນຍັງໄດ້ເອົາໃຈໃສ່ກັບອະນຸພັນຂອງອິນຊູລິນ fluorescent. ໃນການເຮັດວຽກ, ຜູ້ຂຽນໄດ້ຄົ້ນຄວ້າວິທີການ ນຳ ໃຊ້ແລະຂໍ້ມູນຂ່າວສານທີ່ເປັນຮູບປະ ທຳ ໃນການວິເຄາະຜະລິດຕະພັນໃນທຸກຂັ້ນຕອນຂອງການຜະລິດອິນຊູລິນຂອງມະນຸດແລະໄດ້ ກຳ ນົດຕາຕະລາງການປະຕິບັດງານຂອງ chromatographic ເພື່ອແຍກແລະຄຸນລັກສະນະຂອງຜະລິດຕະພັນທີ່ໄດ້ຮັບ.
ນອກຈາກນັ້ນ, ວິທີການຕ່າງໆ ກຳ ລັງຖືກພັດທະນາເພື່ອອັດຕະໂນມັດແລະເລັ່ງຂະບວນການຕ່າງໆໃນການ ກຳ ນົດຄວາມບໍລິສຸດແລະປະລິມານຂອງອິນຊູລິນ.
ເອກະສານລາຍງານກ່ຽວກັບການສຶກສາຄວາມເປັນໄປໄດ້ໃນການ ນຳ ໃຊ້ຊິລິໂຄນແຫຼວ RP ດ້ວຍການກວດຫາໄຟຟ້າເພື່ອການ ກຳ ນົດອິນຊູລິນ, ແລະວິທີການ ສຳ ລັບການ ກຳ ນົດອິນຊູລິນແຍກອອກຈາກ islet of Langerhans ໂດຍການຄົ້ນຄ້ວາພູມຕ້ານທານດ້ວຍການກວດຈັບສັງເຄາະໄດ້ຖືກພັດທະນາ.
ໃນການເຮັດວຽກ, ຄວາມເປັນໄປໄດ້ຂອງການໃຊ້ microdetermination insulin ຢ່າງໄວວາໂດຍໃຊ້ electrophoresis capillary ກັບການກວດຈັບແສງເລເຊີໄດ້ຖືກສືບສວນ. ການວິເຄາະແມ່ນປະຕິບັດໂດຍການເພີ່ມເຂົ້າໄປໃນຕົວຢ່າງປະລິມານທີ່ຮູ້ຈັກຂອງອິນຊູລິນທີ່ມີປ້າຍຊື່ phenylisothiocyanate (FITC) ແລະຊິ້ນ Fab ຂອງພູມຕ້ານທານອິນຊູລິນ. insulins ທີ່ມີປ້າຍຊື່ແລະເປັນປົກກະຕິສາມາດແຂ່ງຂັນກັບສະລັບສັບຊ້ອນ Fab. ອິນຊູລິນທີ່ມີປ້າຍຊື່ FITZ ແລະສະລັບສັບຊ້ອນຂອງມັນກັບ Fab ຖືກແຍກອອກເປັນເວລາ 30 ວິນາທີ.
ເມື່ອບໍ່ດົນມານີ້, ວຽກງານ ຈຳ ນວນຫຼວງຫຼາຍໄດ້ຖືກອຸທິດໃຫ້ແກ່ການປັບປຸງວິທີການຕ່າງໆໃນການຜະລິດອິນຊູລິນ, ພ້ອມທັງການສ້າງຮູບແບບຂະ ໜາດ ຢາໂດຍອີງໃສ່ມັນ.
ຍົກຕົວຢ່າງ, ໃນອາເມລິກາ, ຕົວຄ້າຍອະນຸມູນອິດສະລະ inspatospecific ແມ່ນຖືກຈົດສິດທິບັດ, ໂຄງສ້າງແຕກຕ່າງຈາກຮໍໂມນ ທຳ ມະຊາດຍ້ອນການແນະ ນຳ ທາດເສດເຫຼືອອາຊິດ amino ທີ່ແຕກຕ່າງກັນຢູ່ ຕຳ ແໜ່ງ 13-15 ແລະ 19 ຂອງຕ່ອງໂສ້ A ແລະຢູ່ ຕຳ ແໜ່ງ 16 ຂອງຕ່ອງໂສ້ B.
ຕົວຢ່າງທີ່ໄດ້ຮັບແມ່ນຖືກ ນຳ ໃຊ້ໃນຮູບແບບຕ່າງໆຂອງ parenteral (intravenous, intramuscular, subcutaneous), ຮູບແບບຂະ ໜາດ ທີ່ໃຊ້ໃນເສັ້ນເລືອດຫຼືການໃສ່ໃນຮູບແບບຂອງແຄບຊູນພິເສດໃນການຮັກສາໂລກເບົາຫວານ. ຂອງຄວາມກ່ຽວຂ້ອງໂດຍສະເພາະແມ່ນການສ້າງຮູບແບບຂະ ໜາດ ໃຫ້ບໍລິຫານໂດຍບໍ່ສັກ.
ເອກະສານລາຍງານກ່ຽວກັບການສ້າງລະບົບ macromolecular ສຳ ລັບການບໍລິຫານທາງປາກ, ເຊິ່ງແມ່ນອິນຊູລິນທີ່ບໍ່ມີປະລິມານໃນປະລິມານຂອງໂພລິເມີໄຮໂດຼລິກທີ່ຖືກດັດແປງດ້ວຍທາດໂປຼຕີນຈາກທາດໂປຣຕີນ proteolytic. ປະສິດທິຜົນຂອງຢາດັ່ງກ່າວແມ່ນ 70-80% ຂອງປະສິດທິຜົນຂອງການ ນຳ ສະ ເໜີ ອິນຊູລິນພື້ນເມືອງ.
ໃນວຽກງານອື່ນ, ຢາໄດ້ຮັບໂດຍການສັກຢາອິນຊູລິນ ໜຶ່ງ ບາດກ້າວ, ມີເມັດເລືອດແດງ, ປະຕິບັດໃນອັດຕາສ່ວນ 1-4: 100, ໂດຍມີຕົວແທນຜູກມັດ.ຜູ້ຂຽນລາຍງານການຮັບຢາດ້ວຍກິດຈະ ກຳ 1000 ໜ່ວຍ / g, ການຮັກສາກິດຈະ ກຳ ເຕັມຮູບແບບຫຼັງຈາກການບໍລິຫານທາງປາກແລະເກັບມ້ຽນເປັນເວລາຫຼາຍປີໃນຮູບແບບທີ່ໃຊ້ lyophilized.
ນອກ ເໜືອ ຈາກການສ້າງຢາແລະຮູບແບບຂະ ໜາດ ໃໝ່ ໂດຍອີງໃສ່ອິນຊູລິນ, ວິທີການ ໃໝ່ ກຳ ລັງຖືກພັດທະນາເພື່ອແກ້ໄຂບັນຫາໂລກເບົາຫວານ.
ດັ່ງນັ້ນ, ຜູ້ຂຽນປ່ຽນທາດໂປຼຕີນຈາກການສົ່ງທາດໂປຼຕີນ GUT2 glucose ທີ່ສົ່ງຜ່ານມາຢ່າງບໍ່ຢຸດຢັ້ງໃນເມື່ອກ່ອນມີການເຄື່ອນຍ້າຍຢ່າງເຕັມສ່ວນກັບ insulin cDNA ຂະ ໜາດ ເຕັມຂອງຈຸລັງ HEP G2.
ໃນ Clones ທີ່ໄດ້ຮັບ HEP G2 Insgl, glucose ກະຕຸ້ນໃຫ້ໃກ້ຊິດກັບຄວາມລັບຂອງ insulin ປົກກະຕິແລະ potentiates ການຕອບສະ ໜອງ ຄວາມລັບໃນການຊ່ວຍກະຕຸ້ນຄວາມລັບອື່ນໆ.
ກ້ອງຈຸລະທັດ Immunoelectron ໄດ້ເປີດເຜີຍທາດແປ້ງທີ່ມີທາດ insulin ທີ່ຄ້າຍຄືກັບເມັດເຂົ້າໃນຈຸລັງຂຂອງຈຸນລະສານ Langerhans. ຄວາມເປັນໄປໄດ້ຂອງການ ນຳ ໃຊ້“ ຈຸລັງທຽມ - ທຽມ” ທີ່ໄດ້ຮັບໂດຍວິທີການວິສະວະ ກຳ ທາງພັນທຸ ກຳ ສຳ ລັບການປິ່ນປົວໂຣກເບົາຫວານປະເພດ 1 ແມ່ນ ກຳ ລັງຢູ່ໃນການສົນທະນາຢ່າງຈິງຈັງ.
ຄຽງຄູ່ກັບການແກ້ໄຂບັນຫາຕົວຈິງ, ກົນໄກການປະຕິບັດຂອງອິນຊູລິນ, ເຊັ່ນດຽວກັນກັບຄວາມ ສຳ ພັນທາງດ້ານໂຄງສ້າງແລະການເຮັດວຽກໃນໂມເລກຸນກໍ່ໄດ້ຖືກສຶກສາ. ໜຶ່ງ ໃນວິທີການຄົ້ນຄ້ວາແມ່ນການສ້າງອະນຸພັນຕ່າງໆຂອງອິນຊູລິນແລະການສຶກສາຄຸນສົມບັດທາງກາຍະພາບແລະພູມຕ້ານທານຂອງພວກມັນ 23, 24.
ດັ່ງທີ່ໄດ້ກ່າວມາຂ້າງເທິງ, ຫຼາຍວິທີການ ສຳ ລັບການຜະລິດອິນຊູລິນແມ່ນອີງໃສ່ການໄດ້ຮັບຮໍໂມນນີ້ໃນຮູບແບບຂອງຄາຣະວາກ່ອນ (proinsulin), ຕິດຕາມດ້ວຍການລະບາດຂອງ enzymatic ກັບ insulin ແລະ C-peptide. ໃນປະຈຸບັນ, ການມີກິດຈະ ກຳ ທາງຊີວະວິທະຍາໄດ້ຖືກສະແດງໃຫ້ເຫັນ ສຳ ລັບ C-peptide, ເຊິ່ງເຮັດໃຫ້ມັນສາມາດ ນຳ ໃຊ້ເພື່ອຈຸດປະສົງການ ບຳ ບັດພ້ອມກັບອິນຊູລິນ.
ໃນບົດຂຽນຕໍ່ໄປນີ້ຂອງຊຸດນີ້, ຄຸນລັກສະນະທາງກາຍະພາບແລະຊີວະພາບຂອງ C-peptide, ພ້ອມທັງວິທີການຕ່າງໆ ສຳ ລັບການກະກຽມຂອງມັນ, ຈະຖືກພິຈາລະນາ.
ເຕັກໂນໂລຊີຊີວະພາບໃນການຜະລິດຢາ
ຄວາມສົນໃຈແມ່ນການພັດທະນາເພື່ອໃຫ້ໄດ້ຮູບແບບ STGh 20K. ວຽກທີ່ມີຄວາມ ໝາຍ ສຳ ຄັນແມ່ນການໄດ້ຮັບແລະສຶກສາບໍ່ພຽງແຕ່ຮູບແບບຕ່າງໆຂອງ STH ເທົ່ານັ້ນ, ແຕ່ຍັງເປັນໂຣກ STH ທີ່ບໍ່ສາມາດເຮັດໄດ້ເພື່ອໃຫ້ໄດ້ຮັບການກະ ທຳ ທີ່ຍາວນານຂອງຮໍໂມນ. ວິທີການຕົ້ນສະບັບໄດ້ຖືກພັດທະນາເພື່ອໃຫ້ໄດ້ຮັບ STHch ທີ່ບໍ່ມີປະໂຫຍດໂດຍມີການກະ ທຳ ທີ່ຍາວນານ.
ໃນຂະຫນານກັບການຜະລິດຂອງ STH, ເຕັກໂນໂລຢີທີ່ປະສົມປະສານຕົ້ນສະບັບສໍາລັບການຜະລິດຮໍໂມນ adenohypophysis, ລວມທັງຊະນິດທີ່ກ່ຽວຂ້ອງກັບຊະນິດພັນທັງ ໝົດ, ແລະບາງການດັດແປງຂອງມັນຈາກ GST, ຖືກສ້າງຂື້ນ. ຄວາມ ສຳ ຄັນທີ່ຍິ່ງໃຫຍ່ແມ່ນການຈັດຕັ້ງປະຕິບັດໂຄງການເປົ້າ ໝາຍ ເພື່ອສ້າງຢາ STH (somatogen) ບຳ ບັດໂດຍໄດ້ຮັບໂດຍວິສະວະ ກຳ ທາງພັນທຸ ກຳ.
ປະສົບການທາງດ້ານການຊ່ວຍໄດ້ສະແດງໃຫ້ເຫັນວ່າ, ການເພີ່ມປະສິດທິພາບຂອງການຮັກສາໂຣກສະມອງ, ມັນຄວນແນະ ນຳ ໃຫ້ມີການກຽມພ້ອມທາງດ້ານຢາທີ່ຄ້າຍຄືກັນຫຼາຍໆຢ່າງທີ່ໄດ້ຮັບໂດຍເຕັກໂນໂລຢີຕ່າງໆຫຼືວິທີການຕ່າງໆ (MF, Ausomatin, Somatogen).
ການຮັກສາໄລຍະຍາວ (ເປັນເວລາຫລາຍປີ) ດ້ວຍການກະກຽມ STHh ໜຶ່ງ ຄັ້ງເຮັດໃຫ້ມີຄວາມອ່ອນໄຫວໃນຮ່າງກາຍຫຼຸດລົງ.
ໃນບາງສ່ວນ, ນີ້ອາດຈະເປັນຜົນມາຈາກການສ້າງຕັ້ງພູມຕ້ານທານ, ແຕ່ເຫດຜົນຕົ້ນຕໍຕ້ອງໄດ້ສະແຫວງຫາໃນລະດັບຂອງຕົວຮັບແລະການປຸງແຕ່ງຮໍໂມນ.
ເຮັດວຽກຮ່ວມກັບ GST, ເຊັ່ນດຽວກັນກັບການສຶກສາທີ່ສົມບູນແບບຂອງຮໍໂມນທີ່ປິດລັບແລະຮູບແບບຕ່າງໆຂອງມັນເຮັດໃຫ້ມັນສາມາດສຶກສາລະບົບຕ່າງໆທີ່ສ້າງຂື້ນໂດຍ ທຳ ມະຊາດແລະເຂົ້າໃຈພວກມັນໄດ້ດີຂື້ນ. ການມີຢູ່ຂອງຮູບແບບຕ່າງໆຂອງເຊື້ອໂຣກ STH ໃນຮ່າງກາຍສະແດງໃຫ້ເຫັນເຖິງຄວາມເປັນໄປໄດ້ແລະການ ນຳ ໃຊ້ທີ່ເປັນໄປໄດ້, ຕົວຢ່າງ, ຢູ່ໃນຫ້ອງກວດພະຍາດ.
ໃນເວລາທີ່ການສ້າງການກະກຽມ STHch ໃຫມ່, ມັນເປັນສິ່ງຈໍາເປັນກ່ອນອື່ນຫມົດທີ່ຈະສຸມໃສ່ຮູບແບບທໍາມະຊາດຂອງຮໍໂມນແລະ, ຖ້າເຫມາະສົມ, ເພື່ອຂະຫຍາຍພວກມັນໂດຍວິສະວະກໍາພັນທຸກໍາ, ເຊັ່ນດຽວກັນກັບ STHch monomer.
ໃນການຜະລິດການກະກຽມຂອງ STHch ຈາກ GST, ເຕັກໂນໂລຢີອຸດສາຫະ ກຳ ທີ່ສົມບູນແບບ ສຳ ລັບການຜະລິດຮໍໂມນອື່ນໆຂອງ adenohypophysis (LGH, FSHch, TTGch ແລະອື່ນໆ) ແມ່ນຖືກຈັດຕັ້ງປະຕິບັດຢ່າງ ສຳ ເລັດຜົນ. ມັນເປັນສິ່ງຈໍາເປັນທີ່ຈະຕ້ອງເພີ່ມປະສິດທິພາບການຜະລິດໂດຍການແນະ ນຳ ວິທີການທີ່ກ້າວ ໜ້າ ໃໝ່ (ການສະກົດຈິດ, ແລະອື່ນໆ).
), ໄດ້ຮັບຮໍໂມນທີ່ບໍລິສຸດສູງໂດຍ ນຳ ໃຊ້ເຕັກໂນໂລຢີລວມ.
ມັນ ຈຳ ເປັນຕ້ອງໄດ້ຂະຫຍາຍການຜະລິດແລະການ ນຳ ໃຊ້ຊຸດພູມຕ້ານທານຂອງຮໍໂມນຂອງ adenohypophysis ສຳ ລັບການບົ່ງມະຕິແລະເຕັກໂນໂລຢີຊີວະພາບ, ເພື່ອ ດຳ ເນີນການຜະລິດທີ່ໄດ້ຮັບການ ກຳ ນົດຂອງພູມຕ້ານທານທີ່ໄດ້ມາດຕະຖານຂອງເກັດຕ່າງໆ, ເພື່ອສ້າງການກຽມຕົວ ໃໝ່ ຂອງ STHch, ລວມທັງສິ່ງທີ່ບໍ່ມີປະໂຫຍດ.
ຄວາມຈິງທີ່ວ່າ STH ສົ່ງຜົນກະທົບຕໍ່ທາດໂປຼຕີນ, ໄຂມັນແລະທາດແຮ່ທາດ, ເຮັດ ໜ້າ ທີ່ໃນລະດັບຈຸລັງໂດຍບໍ່ມີອະໄວຍະວະເປົ້າ ໝາຍ, ແລະເປັນ anabolic, ໃຫ້ຄວາມສົດໃສດ້ານທີ່ດີໃນການ ນຳ ໃຊ້ເພື່ອກະຕຸ້ນຂະບວນການສ້ອມແປງແລະປິ່ນປົວພະຍາດຕ່າງໆ. ການສຶກສາຢ່າງກວ້າງຂວາງກ່ຽວກັບບັນຫາເຫຼົ່ານີ້, ພ້ອມທັງຄວາມເປັນໄປໄດ້ຂອງການ ນຳ ໃຊ້ຮູບແບບທີ່ຖືກປ່ຽນແປງແລະການປ່ຽນແປງຂອງ STGch ແມ່ນວຽກທີ່ຮີບດ່ວນແລະມີຄວາມ ໝາຍ ດີ.
ການໄດ້ຮັບ insulin ໃນເຕັກໂນໂລຢີຊີວະພາບ
Insulin, ຮໍໂມນ peptide ຂອງບັນດາ islet ຂອງ Langerhans ຂອງ pancreas ແມ່ນການປິ່ນປົວຕົ້ນຕໍສໍາລັບພະຍາດເບົາຫວານ. ພະຍາດນີ້ແມ່ນເກີດມາຈາກການຂາດອິນຊູລິນແລະສະແດງອອກໂດຍການເພີ່ມຂື້ນຂອງນ້ ຳ ຕານໃນເລືອດ. ຈົນກ່ວາບໍ່ດົນມານີ້, insulin ແມ່ນໄດ້ມາຈາກກະດູກສັນຫຼັງຂອງງົວແລະຫມູ.
ຢານີ້ມີຄວາມແຕກຕ່າງຈາກລະດັບອິນຊູລິນຂອງມະນຸດໂດຍການທົດແທນອາຊິດ amino 1 ,3, ດັ່ງນັ້ນຈຶ່ງມີການຂົ່ມຂູ່ຕໍ່ອາການແພ້, ໂດຍສະເພາະໃນເດັກນ້ອຍ. ການ ນຳ ໃຊ້ຢາອິນຊູລິນຢ່າງແຜ່ຫຼາຍແມ່ນຖືກ ຈຳ ກັດໂດຍຄ່າໃຊ້ຈ່າຍສູງແລະຊັບພະຍາກອນທີ່ ຈຳ ກັດ.
ໂດຍການແກ້ໄຂທາງເຄມີ, ອິນຊູລິນຈາກສັດໄດ້ຖືກສ້າງຂື້ນໂດຍແຍກບໍ່ໄດ້ຈາກມະນຸດ, ແຕ່ນີ້ ໝາຍ ຄວາມວ່າລາຄາຜະລິດຕະພັນເພີ່ມຂື້ນຕື່ມ.
ຕັ້ງແຕ່ປີ 1982, EliLilly ໄດ້ຜະລິດອິນຊູລິນທີ່ມີການ ກຳ ເນີດທາງພັນທຸ ກຳ ໂດຍອີງໃສ່ການສັງເຄາະແຍກຕ່າງຫາກຂອງຕ່ອງໂສ້ E. coli A ແລະ B. ຄ່າໃຊ້ຈ່າຍຂອງຜະລິດຕະພັນໄດ້ຫຼຸດລົງຢ່າງຫຼວງຫຼາຍ, ຜົນຂອງ insulin ແມ່ນຄືກັນກັບມະນຸດ. ຕັ້ງແຕ່ປີ 1980, ມີລາຍງານຂ່າວໃນ ໜັງ ສືພິມກ່ຽວກັບການປິດຕົວຂອງ gene proinsulin, ເຊິ່ງເປັນຮໍໂມນຮໍໂມນທີ່ປ່ຽນເປັນຮູບແບບເກົ່າແກ່ທີ່ມີໂປຣໂມຊັ່ນ ຈຳ ກັດ.
ເຕັກໂນໂລຍີໃນການຝັງເຂັມຍັງຖືກ ນຳ ໃຊ້ເຂົ້າໃນການຮັກສາໂລກເບົາຫວານ: ຈຸລັງປ້ອງກັນພະຍາດເບົາຫວານໃນແຄບຊູນ, ແນະ ນຳ ເທື່ອ ໜຶ່ງ ເຂົ້າໃນຮ່າງກາຍຂອງຄົນເຈັບ, ຜະລິດອິນຊູລິນໃນປີ.
Genetics ແບບປະສົມປະສານໄດ້ເປີດຕົວຮໍໂມນທີ່ຊ່ວຍກະຕຸ້ນແລະ luteinizing. peptides ເຫຼົ່ານີ້ແມ່ນປະກອບດ້ວຍສອງສ່ວນຍ່ອຍ. ໃນວາລະກອງປະຊຸມແມ່ນການສັງເຄາະອຸດສາຫະ ກຳ ຂອງຮໍໂມນ oligopeptide ຂອງລະບົບປະສາດ - enkephalins, ເຊິ່ງກໍ່ສ້າງມາຈາກ 5 ອາຊິດ amino ທີ່ຍັງເຫຼືອ, ແລະ endorphins, ອະນາໄມຂອງ morphine.
ເມື່ອ ນຳ ໃຊ້ຢ່າງສົມເຫດສົມຜົນ, peptides ເຫຼົ່ານີ້ບັນເທົາອາການເຈັບ, ສ້າງໂປຣໄຟລທີ່ດີ, ເພີ່ມປະສິດທິພາບ, ເອົາໃຈໃສ່ສຸມໃສ່, ປັບປຸງຄວາມຊົງ ຈຳ, ແລະເຮັດໃຫ້ນອນຫຼັບແລະຕື່ນຕົວ.
ຕົວຢ່າງຂອງການ ນຳ ໃຊ້ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ ທີ່ປະສົບຜົນ ສຳ ເລັດແມ່ນການສັງເຄາະຂອງ p-endorphin ໂດຍ ນຳ ໃຊ້ເຕັກໂນໂລຍີໂປຼຕີນປະສົມທີ່ອະທິບາຍຂ້າງເທິງ ສຳ ລັບຮໍໂມນ peptide ອື່ນ, somatostatin.
ວິທີການຜະລິດອິນຊູລິນ
ທາງປະຫວັດສາດ, ວິທີ ທຳ ອິດທີ່ໄດ້ຮັບສານອິນຊູລິນ ສຳ ລັບຈຸດປະສົງການຮັກສາແມ່ນການໂດດດ່ຽວຂອງອະນາໄມຂອງຮໍໂມນນີ້ຈາກແຫຼ່ງ ທຳ ມະຊາດ (ບັນດາ islets ຂອງຝູງສັດປີກແລະ ໝູ).
ໃນຊຸມປີ 20 ຂອງສະຕະວັດທີ່ຜ່ານມາ, ມັນໄດ້ພົບວ່າ insulins bovine ແລະຫມູ (ເຊິ່ງຢູ່ໃກ້ກັບອິນຊູລິນຂອງມະນຸດໃນໂຄງສ້າງແລະລໍາດັບອາຊິດ amino) ສະແດງກິດຈະກໍາໃນຮ່າງກາຍຂອງມະນຸດທຽບກັບ insulin ຂອງມະນຸດ. ຫລັງຈາກນັ້ນ, ຢາອິນຊູລິນຫລືຫມູແມ່ນໃຊ້ໃນການປິ່ນປົວຄົນເຈັບທີ່ເປັນໂຣກເບົາຫວານຊະນິດ I.
ເຖິງຢ່າງໃດກໍ່ຕາມ, ຫຼັງຈາກເວລາໃດ ໜຶ່ງ ມັນໄດ້ສະແດງໃຫ້ເຫັນວ່າໃນບາງກໍລະນີພູມຕ້ານທານກັບອິນຊູລິນແລະທາດໂປຼຕີນຈາກ porcine ເລີ່ມສະສົມຢູ່ໃນຮ່າງກາຍຂອງມະນຸດ, ເຮັດໃຫ້ຜົນກະທົບຂອງມັນເສີຍຫາຍ.
ໃນທາງກົງກັນຂ້າມ, ຂໍ້ໄດ້ປຽບ ໜຶ່ງ ຂອງວິທີການນີ້ເພື່ອໃຫ້ໄດ້ຮັບອິນຊູລິນແມ່ນການມີວັດຖຸດິບ (insulin bovine ແລະຊີ້ນ ໝູ ສາມາດຫາໄດ້ງ່າຍໃນປະລິມານຫຼາຍ) ເຊິ່ງມີບົດບາດ ສຳ ຄັນໃນການພັດທະນາວິທີການ ທຳ ອິດໃນການຜະລິດອິນຊູລິນ.ວິທີການນີ້ເອີ້ນວ່າເຄິ່ງສັງເຄາະ.
ໃນວິທີການຜະລິດອິນຊູລິນຂອງມະນຸດ, insulin ໝູ ແມ່ນໃຊ້ເປັນອາຫານສັດ. C-terminal octapeptide ຂອງລະບົບຕ່ອງໂສ້ B ຖືກແຍກອອກຈາກອິນຊູລິນ porcine ທີ່ບໍລິສຸດ, ຫລັງຈາກນັ້ນ C-terminal octapeptide ຂອງ insulin ຂອງມະນຸດໄດ້ຖືກສັງເຄາະ.
ຫຼັງຈາກນັ້ນ, ມັນກໍ່ຖືກຕິດດ້ວຍທາງເຄມີ, ກຸ່ມປ້ອງກັນໄດ້ຖືກໂຍກຍ້າຍອອກແລະຜົນຂອງ insulin ຖືກເຮັດໃຫ້ບໍລິສຸດ. ໃນເວລາທີ່ທົດສອບວິທີການໃນການໄດ້ຮັບ insulin, ຕົວຕົນທີ່ສົມບູນຂອງຮໍໂມນທີ່ໄດ້ຮັບກັບ insulin ຂອງມະນຸດໄດ້ຖືກສະແດງໃຫ້ເຫັນ.
ຂໍ້ເສຍປຽບຕົ້ນຕໍຂອງວິທີການນີ້ແມ່ນຄ່າໃຊ້ຈ່າຍສູງຂອງອິນຊູລິນທີ່ໄດ້ຮັບ (ເຖິງແມ່ນວ່າໃນປັດຈຸບັນ, ການສັງເຄາະສານເຄມີຂອງ octapeptide ແມ່ນຄວາມສຸກທີ່ແພງ, ໂດຍສະເພາະໃນລະດັບອຸດສາຫະ ກຳ).
ໃນປະຈຸບັນ, ອິນຊູລິນຂອງມະນຸດສ່ວນຫຼາຍແມ່ນໄດ້ມາຈາກສອງທາງ: ໂດຍການດັດແກ້ອິນຊູລິນໂດຍວິທີການສັງເຄາະແລະໂດຍວິທີວິສະວະ ກຳ ທາງພັນທຸ ກຳ.
ໃນກໍລະນີ ທຳ ອິດ, ວິທີການແມ່ນອີງໃສ່ຄວາມຈິງທີ່ວ່າອິນຊູລິນມີຄວາມແຕກຕ່າງຈາກອິນຊູລິນຂອງມະນຸດໃນການທົດແທນ ໜຶ່ງ ທີ່ C-terminus ຂອງລະບົບຕ່ອງໂສ້ Ala30Thr B.
ການທົດແທນຂອງ alanine ດ້ວຍ threonine ແມ່ນປະຕິບັດໂດຍການລ້າງທາດ enanme-catalyzed ຂອງ alanine ແລະການເພີ່ມສານເສດເຫຼືອ threonine ທີ່ຖືກປົກປ້ອງໂດຍກຸ່ມ carboxy ແທນທີ່ຈະເປັນຂອງມັນ, ເຊິ່ງມີຢູ່ໃນສ່ວນໃຫຍ່ຂອງສ່ວນປະສົມຂອງປະຕິກິລິຍາ. ຫຼັງຈາກການລ້າງກຸ່ມ O-tert-butyl ທີ່ໄດ້ຮັບການປ້ອງກັນແລ້ວ, insulin ຂອງມະນຸດຈະໄດ້ຮັບ.
Insulin ແມ່ນທາດໂປຼຕີນ ທຳ ອິດທີ່ໄດ້ຮັບເພື່ອຈຸດປະສົງທາງການຄ້າໂດຍໃຊ້ເຕັກໂນໂລຍີ DNA ທີ່ສົມທົບ ໃໝ່. ມີສອງວິທີການຕົ້ນຕໍໃນການຜະລິດອິນຊູລິນຂອງມະນຸດທີ່ມີການ ກຳ ເນີດທາງພັນທຸ ກຳ.
ໃນກໍລະນີທໍາອິດ, ແຍກຕ່າງຫາກ (ສາຍຜູ້ຜະລິດທີ່ແຕກຕ່າງກັນ) ແມ່ນໄດ້ຮັບສໍາລັບຕ່ອງໂສ້ທັງສອງຕິດຕາມມາດ້ວຍການພັບໂມເລກຸນ (ການສ້າງຂົວຂ້າມ disulfide) ແລະການແຍກ isoforms.
ໃນຄັ້ງທີສອງ, ການຜະລິດໃນຮູບແບບຂອງຄາບກ່ອນ (proinsulin) ຕາມດ້ວຍການຍ່ອຍອາຫານ enzymatic ກັບ trypsin ແລະ carboxypeptidase B ກັບຮູບແບບຂອງຮໍໂມນທີ່ມີການເຄື່ອນໄຫວ.
ໃນປະຈຸບັນ, ມັນເປັນການດີທີ່ສຸດທີ່ຈະໄດ້ຮັບທາດອິນຊູລິນໃນຮູບແບບຂອງການປະກາດລ່ວງ ໜ້າ, ເຊິ່ງຮັບປະກັນການປິດສະພານ disulfide ທີ່ຖືກຕ້ອງ (ໃນກໍລະນີຂອງການກະກຽມລະບົບຕ່ອງໂສ້ແຍກຕ່າງຫາກ, ວົງຈອນທີ່ປະສົບຜົນ ສຳ ເລັດຂອງການປະຕິເສດ, ການແຍກແຍກ isoforms ແລະການປ່ຽນຊື່ ໃໝ່ ແມ່ນໄດ້ປະຕິບັດ).
ດ້ວຍວິທີການທັງສອງຢ່າງ, ມັນສາມາດທັງສອງສ່ວນບຸກຄົນເພື່ອໃຫ້ໄດ້ສ່ວນປະກອບເລີ່ມຕົ້ນ (A- ແລະ B-chains ຫລື proinsulin), ແລະເປັນສ່ວນ ໜຶ່ງ ຂອງໂປຣຕີນປະສົມ. ນອກເຫນືອໄປຈາກຕ່ອງໂສ້ A ແລະ B ຫຼື proinsulin, ທາດໂປຼຕີນປະສົມອາດມີ:
1) ທາດໂປຼຕີນຈາກການຂົນສົ່ງ - ສະ ໜອງ ການຂົນສົ່ງທາດໂປຼຕີນປະສົມເຂົ້າໄປໃນພື້ນທີ່ periplasmic ຂອງຫ້ອງຫຼືວັດທະນະ ທຳ ກາງ,
2) ອົງປະກອບທີ່ມີຄວາມເປັນເອກະພາບ - ຊ່ວຍ ອຳ ນວຍຄວາມສະດວກໃຫ້ໂດດດ່ຽວຂອງໂປຣຕີນປະສົມ.
ໃນກໍລະນີນີ້, ທັງສອງສ່ວນຂອງສ່ວນປະກອບເຫຼົ່ານີ້ສາມາດ ນຳ ສະ ເໜີ ພ້ອມກັນໃນສ່ວນປະກອບຂອງທາດໂປຼຕີນປະສົມ. ນອກຈາກນັ້ນ, ໃນເວລາທີ່ສ້າງໂປຣຕີນປະສົມ, ຫຼັກການຂອງຫຼາຍຮູບແບບສາມາດ ນຳ ໃຊ້ໄດ້ (ນັ້ນແມ່ນ polypeptide ເປົ້າ ໝາຍ ຫຼາຍສະບັບທີ່ມີຢູ່ໃນທາດໂປຼຕີນປະສົມ) ເຊິ່ງສາມາດເພີ່ມຜົນຜະລິດຂອງຜະລິດຕະພັນເປົ້າ ໝາຍ ຢ່າງຫຼວງຫຼາຍ.
ການສະແດງອອກຂອງທາດໂປຣຕີນໃນຈຸລັງ E. coli ..
Strain JM 109 N1864 ດ້ວຍ ລຳ ດັບ nucleotide ສະແດງທາດໂປຼຕີນຈາກທາດປະສົມ, ເຊິ່ງປະກອບດ້ວຍທາດໂປຼຕີນຈາກເສັ້ນແລະທາດໂປຼຕີນ Staphylococcus aureus ຊິ້ນສ່ວນ ໜຶ່ງ ທີ່ຕິດກັບ N-terminus ຂອງມັນຜ່ານທາດເສດ methionine, ຖືກ ນຳ ໃຊ້ເຂົ້າໃນວຽກງານ.
ການປູກຝັງຂອງເຊື້ອໄຟຊີວະພາບທີ່ອີ່ມຕົວຂອງຈຸລັງຂອງສາຍພັນທີ່ສົມບູນແບບເຮັດໃຫ້ການເລີ່ມຕົ້ນຂອງການຜະລິດໂປຣຕີນປະສົມ, ການໂດດດ່ຽວແລະການຫັນເປັນ ລຳ ດັບເຊິ່ງໃນທໍ່ ນຳ ໄປສູ່ການເຮັດອິນຊູລິນ.
ນັກຄົ້ນຄວ້າອີກກຸ່ມ ໜຶ່ງ ໄດ້ຮັບທາດໂປຼຕີນທີ່ສົມບູນໃນລະບົບການສະແດງອອກຂອງແບັກທີເລຍຂອງທາດປະສົມທີ່ປະກອບດ້ວຍໂປຣຕີນຂອງມະນຸດແລະຫາງ polyhistidine ຕິດຢູ່ໃນມັນໂດຍຜ່ານສານຕົກຄ້າງ methionine. ມັນຖືກແຍກອອກໄປໂດຍການໃຊ້ຊິລິໂຄນທຽມໃນຖັນ Ni-agarose ຈາກອົງການຈັດຕັ້ງລວມແລະຍ່ອຍດ້ວຍສານຊີເມັນ Bromide.
ການສ້າງແຜນທີ່ແລະການວິເຄາະສັງເຄາະມະຫາສານກ່ຽວກັບທາດໂປຼຕິນທີ່ໄດ້ຮັບທີ່ບໍລິສຸດໂດຍ chromatography ແລກປ່ຽນທາດ ion ໃສ່ນ້ ຳ ຢາງແລກປ່ຽນ anion ແລະ RP (ໄລຍະປີ້ນກັບກັນ) HPLC (chromatography ແຫຼວທີ່ມີປະສິດຕິພາບສູງ) ໄດ້ສະແດງໃຫ້ເຫັນການມີຂອງຂົວ disulfide ທີ່ສອດຄ້ອງກັບຂົວ disulfide ຂອງ proinsulin ຂອງມະນຸດ. ມັນຍັງຖືກລາຍງານກ່ຽວກັບການພັດທະນາວິທີການ ໃໝ່ ທີ່ມີການປັບປຸງ ໃໝ່ ໃນການຜະລິດອິນຊູລິນຂອງມະນຸດໂດຍວິສະວະ ກຳ ພັນທຸ ກຳ ໃນຈຸລັງ prokaryotic. ຜູ້ຂຽນພົບວ່າຜົນຂອງ insulin ໃນໂຄງສ້າງແລະກິດຈະ ກຳ ທາງຊີວະວິທະຍາຂອງມັນແມ່ນຄ້າຍຄືກັນກັບຮໍໂມນທີ່ແຍກອອກມາຈາກກະຕ່າຍ.
ບໍ່ດົນມານີ້, ໄດ້ມີການເອົາໃຈໃສ່ຢ່າງໃກ້ຊິດໃນການເຮັດຂັ້ນຕອນງ່າຍໆໃນການຜະລິດອິນຊູລິນໂດຍວິສະວະ ກຳ ທາງພັນທຸ ກຳ. ດັ່ງນັ້ນ, ທາດໂປຼຕີນປະສົມໄດ້ຮັບຈາກສານ peptide ຂອງ interleukin ຂອງຜູ້ ນຳ ຕິດກັບ N-terminus ຂອງ proinsulin ໂດຍຜ່ານສານຕົກຄ້າງຂອງ lysine. ທາດໂປຼຕີນດັ່ງກ່າວໄດ້ຖືກສະແດງອອກຢ່າງມີປະສິດຕິພາບແລະທ້ອງຖິ່ນໃນອົງການຈັດຕັ້ງລວມ.
ຫຼັງຈາກໂດດດ່ຽວ, ທາດໂປຼຕີນໄດ້ຖືກຍ່ອຍດ້ວຍ trypsin ເພື່ອຜະລິດອິນຊູລິນແລະ C-peptide. ນັກຄົ້ນຄວ້າອີກກຸ່ມ ໜຶ່ງ ປະຕິບັດແບບດຽວກັນນີ້. ທາດໂປຼຕີນປະສົມທີ່ປະກອບດ້ວຍ proinsulin ແລະສອງໂດເມນສັງເຄາະຂອງ staphylococcus ທາດ IgG ທີ່ຜູກມັດທາດໂປຼຕີນໄດ້ຖືກທ້ອງຖິ່ນໃນອົງການລວມ, ແຕ່ມີລະດັບການສະແດງອອກທີ່ສູງກວ່າ.
ທາດໂປຼຕີນດັ່ງກ່າວໄດ້ຖືກແຍກອອກໂດຍ chromatography ຄວາມສົນໃຈຂອງ IgG ແລະຍ່ອຍດ້ວຍ trypsin ແລະ carboxypeptidase B. ຜົນຂອງ insulin ແລະ C-peptide ໄດ້ຖືກເຮັດໃຫ້ບໍລິສຸດໂດຍ RP HPLC. ໃນເວລາທີ່ສ້າງໂຄງສ້າງທີ່ຫລອກລວງ, ອັດຕາສ່ວນມະຫາຊົນຂອງທາດໂປຼຕີນຂອງບັນທຸກແລະ polypeptide ເປົ້າ ໝາຍ ແມ່ນມີຄວາມ ສຳ ຄັນຫຼາຍ.
ການກໍ່ສ້າງຂອງການຜະສົມຜະສານໄດ້ຖືກອະທິບາຍວ່າບ່ອນທີ່ທາດໂປຼຕີນຈາກທາດໂປຼຕີນຈາກການຜູກມັດຂອງມະນຸດຖືກນໍາໃຊ້ເປັນ polypeptide ບັນທຸກ. ຫນຶ່ງ, ສາມແລະເຈັດ C-peptides ຖືກຕິດຢູ່ກັບມັນ.
C-peptides ໄດ້ຖືກເຊື່ອມຕໍ່ບົນພື້ນຖານຂອງຫົວ - ຫາງໂດຍໃຊ້ spacers ອາຊິດ amino ທີ່ບັນຈຸສະຖານທີ່ ຈຳ ກັດ Sfi I ແລະສານຕົກຄ້າງ arginine ສອງຕົ້ນໃນຕອນຕົ້ນແລະໃນຕອນທ້າຍຂອງ spacer ສຳ ລັບການແບ່ງທາດໂປຼຕີນຕໍ່ໆໄປກັບ trypsin. HPLC ຂອງຜະລິດຕະພັນການເກັບກູ້ໄດ້ສະແດງໃຫ້ເຫັນວ່າການ ກຳ ຈັດທາດ C-peptide ແມ່ນມີປະລິມານຫຼາຍ, ແລະນີ້ຊ່ວຍໃຫ້ການ ນຳ ໃຊ້ພັນທຸ ກຳ ສັງເຄາະແບບ multimeric ໄດ້ຮັບ polypeptides ເປົ້າ ໝາຍ ໃນລະດັບອຸດສາຫະ ກຳ.
ການໄດ້ຮັບສານໂປຣຕິນຊະນິດ mutant, ເຊິ່ງບັນຈຸທົດແທນ Arg32Tyr. ໃນເວລາທີ່ທາດໂປຼຕີນນີ້ໄດ້ຖືກຮ່ວມກັນກັບ trypsin ແລະ carboxypeptidase B, insulin ພື້ນເມືອງແລະ C-peptide ທີ່ບັນຈຸສານເສດເຫຼືອ tyrosine ກໍ່ຕັ້ງຂຶ້ນ. ສຸດທ້າຍ, ຫຼັງຈາກຕິດປ້າຍ 125I, ຖືກ ນຳ ໃຊ້ຢ່າງຈິງຈັງໃນ radioimmunoassay.
Insulin ມີຈຸດປະສົງໃນການຜະລິດຢາຕ້ອງມີຄວາມບໍລິສຸດສູງ. ດັ່ງນັ້ນ, ການຄວບຄຸມຄວາມບໍລິສຸດຂອງຜະລິດຕະພັນທີ່ໄດ້ຮັບໃນແຕ່ລະຂັ້ນຕອນຂອງການຜະລິດແມ່ນມີຄວາມ ຈຳ ເປັນສູງ. ກ່ອນ ໜ້າ ນີ້, RP ແລະ IO (ການແລກປ່ຽນທາດ ion) HPLC ໄດ້ຖືກ ນຳ ໃຊ້ເພື່ອຄຸນລັກສະນະຂອງ proinsulin-S-sulfonate, proinsulin, ສ່ວນບຸກຄົນ A- ແລະ B-chains, ແລະ S-sulfonates.
ຄວາມສົນໃຈໂດຍສະເພາະແມ່ນຍັງໄດ້ເອົາໃຈໃສ່ກັບອະນຸພັນຂອງອິນຊູລິນ fluorescent. ໃນການເຮັດວຽກ, ຜູ້ຂຽນໄດ້ຄົ້ນຄວ້າວິທີການ ນຳ ໃຊ້ແລະຂໍ້ມູນຂ່າວສານທີ່ເປັນຮູບປະ ທຳ ໃນການວິເຄາະຜະລິດຕະພັນໃນທຸກຂັ້ນຕອນຂອງການຜະລິດອິນຊູລິນຂອງມະນຸດແລະໄດ້ ກຳ ນົດຕາຕະລາງການປະຕິບັດງານຂອງ chromatographic ເພື່ອແຍກແລະຄຸນລັກສະນະຂອງຜະລິດຕະພັນທີ່ໄດ້ຮັບ.
ນອກຈາກນັ້ນ, ວິທີການຕ່າງໆ ກຳ ລັງຖືກພັດທະນາເພື່ອອັດຕະໂນມັດແລະເລັ່ງຂະບວນການຕ່າງໆໃນການ ກຳ ນົດຄວາມບໍລິສຸດແລະປະລິມານຂອງອິນຊູລິນ.
ການສຶກສາກ່ຽວກັບຄວາມເປັນໄປໄດ້ຂອງການໃຊ້ chromatography ແຫຼວ RP ດ້ວຍການກວດຫາໄຟຟ້າເພື່ອການ ກຳ ນົດຂອງອິນຊູລິນແມ່ນຖືກລາຍງານ, ແລະວິທີການ ສຳ ລັບການ ກຳ ນົດອິນຊູລິນແຍກອອກຈາກ Islet Langerhans ໂດຍການຄົ້ນພົບພູມຕ້ານທານດ້ວຍການກວດຈັບແສງສະຫວ່າງໄດ້ຖືກພັດທະນາ.
ໃນການເຮັດວຽກ, ຄວາມເປັນໄປໄດ້ຂອງການໃຊ້ microdetermination insulin ຢ່າງໄວວາໂດຍໃຊ້ electrophoresis capillary ກັບການກວດຈັບແສງເລເຊີໄດ້ຖືກສືບສວນ.ການວິເຄາະແມ່ນປະຕິບັດໂດຍການເພີ່ມເຂົ້າໄປໃນຕົວຢ່າງປະລິມານທີ່ຮູ້ຈັກຂອງອິນຊູລິນທີ່ມີປ້າຍຊື່ phenylisothiocyanate (FITC) ແລະຊິ້ນ Fab ຂອງພູມຕ້ານທານອິນຊູລິນ. insulins ທີ່ມີປ້າຍຊື່ແລະເປັນປົກກະຕິສາມາດແຂ່ງຂັນກັບສະລັບສັບຊ້ອນ Fab. ອິນຊູລິນທີ່ມີປ້າຍຊື່ FITZ ແລະສະລັບສັບຊ້ອນຂອງມັນກັບ Fab ຖືກແຍກອອກເປັນເວລາ 30 ວິນາທີ.
ອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ

ຄຳ ຖາມກ່ຽວກັບຢາອິນຊູລິນແມ່ນເຮັດໃຫ້ມີຄວາມສົນໃຈບໍ່ພຽງແຕ່ຕໍ່ບັນດາແພດ ໝໍ ແລະຮ້ານຂາຍຢາເທົ່ານັ້ນ, ແຕ່ມັນຍັງຈະເປັນຂອງຄົນເຈັບທີ່ເປັນໂລກເບົາຫວານ, ເຊັ່ນດຽວກັນກັບຍາດພີ່ນ້ອງແລະ ໝູ່ ເພື່ອນຂອງພວກເຂົາ ນຳ ອີກ.
ໃນມື້ນີ້, ຮໍໂມນທີ່ເປັນເອກະລັກແລະມີຄວາມ ສຳ ຄັນດັ່ງກ່າວ ສຳ ລັບສຸຂະພາບຂອງມະນຸດສາມາດໄດ້ຮັບຈາກວັດຖຸດິບຕ່າງໆໂດຍ ນຳ ໃຊ້ເຕັກໂນໂລຢີທີ່ພັດທະນາພິເສດແລະຖືກທົດສອບຢ່າງລະມັດລະວັງ. ອີງຕາມວິທີການກະກຽມ, ປະເພດອິນຊູລິນຕໍ່ໄປນີ້ແມ່ນ ຈຳ ແນກ:
- ຊີ້ນ ໝູ ຫລື bovine, ເຊິ່ງເອີ້ນກັນວ່າຜະລິດຕະພັນສັດ
- ໝູ ຊີວະພາບທີ່ຖືກປັບປຸງແກ້ໄຂ
- ວິສະວະກອນທີ່ໄດ້ຮັບການອອກແບບຫຼືຜະລິດຄືນ ໃໝ່
- ດັດແກ້ພັນທຸ ກຳ
- ສັງເຄາະ
insulin ຫມູໄດ້ຖືກນໍາໃຊ້ທີ່ຍາວທີ່ສຸດສໍາລັບພະຍາດເບົາຫວານ. ຄໍາຮ້ອງສະຫມັກຂອງມັນໄດ້ເລີ່ມຕົ້ນກັບຄືນໄປບ່ອນໃນ 20 ຂອງສະຕະວັດທີ່ຜ່ານມາ.
ມັນຄວນຈະໄດ້ຮັບການສັງເກດວ່າຫມູຫຼືສັດແມ່ນຢາເສບຕິດດຽວຈົນກ່ວາ 80s ຂອງສະຕະວັດທີ່ຜ່ານມາ. ເພື່ອທີ່ຈະໄດ້ຮັບມັນ, ເນື້ອງອກຂອງສັດຖືກ ນຳ ໃຊ້.
ເຖິງຢ່າງໃດກໍ່ຕາມ, ວິທີການນີ້ຍາກທີ່ຈະເອີ້ນວ່າດີທີ່ສຸດຫຼືງ່າຍດາຍ: ການເຮັດວຽກກັບວັດຖຸດິບທາງຊີວະພາບແມ່ນບໍ່ສະດວກສະ ເໝີ ໄປ, ແລະວັດຖຸດິບເອງກໍ່ບໍ່ພຽງພໍ.
ນອກຈາກນັ້ນ, ສ່ວນປະກອບຂອງອິນຊູລິນບໍ່ສົມບູນສົມບູນກັບສ່ວນປະກອບຂອງຮໍໂມນທີ່ຜະລິດໂດຍຄົນທີ່ມີສຸຂະພາບດີ: ສ່ວນປະສົມຂອງກົດອະມິໂນຕ່າງໆມີຢູ່ໃນໂຄງສ້າງຂອງມັນ. ມັນຄວນຈະໄດ້ຮັບການສັງເກດວ່າຮໍໂມນທີ່ຜະລິດໂດຍເມັດສັດປີກຂອງສັດລ້ຽງມີຄວາມແຕກຕ່າງຫຼາຍກວ່າເກົ່າ, ເຊິ່ງບໍ່ສາມາດເອີ້ນວ່າປະກົດການໃນທາງບວກ.
ໃນການກະກຽມດັ່ງກ່າວ, ນອກ ເໜືອ ໄປຈາກສານ multicomponent ບໍລິສຸດ, ທາດໂປຼຕີນທີ່ເອີ້ນວ່າ proinsulin ແມ່ນບັນຈຸທີ່ບໍ່ສາມາດແຍກອອກໄດ້, ສານທີ່ບໍ່ສາມາດແຍກອອກໄດ້ໂດຍໃຊ້ວິທີການກັ່ນຕອງທີ່ທັນສະ ໄໝ. ມັນແມ່ນລາວຜູ້ທີ່ມັກຈະກາຍເປັນແຫຼ່ງຂອງອາການແພ້, ເຊິ່ງເປັນອັນຕະລາຍໂດຍສະເພາະແມ່ນເດັກນ້ອຍແລະຜູ້ສູງອາຍຸ.
ຮ້ານຂາຍຢາອີກເທື່ອ ໜຶ່ງ ຕ້ອງການເງິນສົດ ສຳ ລັບຜູ້ປ່ວຍເບົາຫວານ. ມີຢາເສບຕິດທີ່ທັນສະໄຫມທີ່ມີປະສິດຕິພາບໃນປະເທດເອີຣົບ, ແຕ່ພວກເຂົາຮັກສາງຽບກ່ຽວກັບມັນ. ນີ້ແມ່ນ.
ດ້ວຍເຫດຜົນດັ່ງກ່າວ, ນັກວິທະຍາສາດທົ່ວໂລກໄດ້ສົນໃຈມາດົນແລ້ວໃນການ ນຳ ເອົາສ່ວນປະກອບຂອງຮໍໂມນທີ່ຜະລິດໂດຍສັດເຂົ້າສູ່ການປະຕິບັດຕາມຮໍໂມນ pancreatic ຂອງຄົນທີ່ມີສຸຂະພາບແຂງແຮງ. ການຄົ້ນພົບຕົວຈິງໃນການຢາແລະການຮັກສາໂລກເບົາຫວານແມ່ນການຜະລິດຢາເຄິ່ງສັງເຄາະທີ່ໄດ້ຮັບໂດຍການທົດແທນທາດອາມີໂນອາມີໂນໃນການກະກຽມສັດກັບ threonine.
ໃນເວລາດຽວກັນ, ວິທີການສັງເຄາະເຄິ່ງ ສຳ ລັບການຜະລິດຮໍໂມນແມ່ນອີງໃສ່ການ ນຳ ໃຊ້ການກະກຽມສັດ. ເວົ້າອີກຢ່າງ ໜຶ່ງ, ພວກມັນພຽງແຕ່ຖືກດັດແປງແລະກາຍເປັນຮໍໂມນທີ່ຜະລິດໂດຍມະນຸດ. ໃນບັນດາຂໍ້ໄດ້ປຽບຂອງພວກມັນແມ່ນຄວາມເຂົ້າກັນໄດ້ກັບຮ່າງກາຍຂອງມະນຸດແລະການບໍ່ມີປະຕິກິລິຍາແພ້.
ຂໍ້ເສຍປຽບຂອງວິທີການນີ້ປະກອບມີການຂາດແຄນວັດຖຸດິບແລະຄວາມຫຍຸ້ງຍາກໃນການເຮັດວຽກກັບວັດສະດຸຊີວະພາບພ້ອມທັງຄ່າໃຊ້ຈ່າຍສູງທັງເຕັກໂນໂລຢີເອງແລະຢາທີ່ສົ່ງຜົນໃຫ້ເກີດຂື້ນ.
ໃນເລື່ອງນີ້, ຢາທີ່ດີທີ່ສຸດ ສຳ ລັບການປິ່ນປົວໂຣກເບົາຫວານແມ່ນຢາອິນຊູລິນທີ່ໄດ້ຮັບໂດຍວິສະວະ ກຳ ທາງພັນທຸ ກຳ.
ໂດຍບັງເອີນ, ມັນມັກຈະຖືກເອີ້ນວ່າອິນຊູລິນທີ່ມີການ ກຳ ເນີດທາງພັນທຸ ກຳ, ດັ່ງນັ້ນຈຶ່ງສະແດງໃຫ້ເຫັນເຖິງວິທີການທີ່ຈະໄດ້ຮັບມັນ, ແລະຜະລິດຕະພັນທີ່ໄດ້ຮັບແມ່ນເອີ້ນວ່າອິນຊູລິນຂອງມະນຸດ, ດັ່ງນັ້ນຈຶ່ງເນັ້ນ ໜັກ ເຖິງເອກະລັກຂອງມັນຢ່າງແທ້ຈິງຕໍ່ຮໍໂມນທີ່ຜະລິດໂດຍກະຕ່າຍຂອງຄົນທີ່ມີສຸຂະພາບແຂງແຮງ.
ໃນບັນດາຂໍ້ໄດ້ປຽບຂອງອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ, ຄົນເຮົາຍັງຄວນສັງເກດເຫັນເຖິງຄວາມບໍລິສຸດແລະຂາດທາດໂປຼຕີນຊີນໃນລະດັບສູງ, ພ້ອມທັງຄວາມຈິງທີ່ວ່າມັນບໍ່ກໍ່ໃຫ້ເກີດປະຕິກິລິຍາແພ້ແລະບໍ່ມີຂໍ້ບົກຜ່ອງ.
ຄຳ ຖາມທີ່ຖືກຖາມເລື້ອຍໆແມ່ນສາມາດເຂົ້າໃຈໄດ້ວ່າ: ທາດອິນຊູລິນທີ່ຜະລິດເອງແມ່ນຫຍັງ? ມັນຫັນອອກວ່າຮໍໂມນນີ້ຖືກຜະລິດໂດຍສາຍພັນເຊື້ອລາ, ເຊັ່ນດຽວກັນກັບ Escherichia coli, ຖືກຈັດໃສ່ໃນສື່ສານອາຫານທີ່ມີສານອາຫານພິເສດ. ຍິ່ງໄປກວ່ານັ້ນ, ປະລິມານຂອງສານທີ່ໄດ້ຮັບແມ່ນມີຂະ ໜາດ ໃຫຍ່ຈົນສາມາດປະຖິ້ມການ ນຳ ໃຊ້ຢາທີ່ໄດ້ຮັບຈາກອະໄວຍະວະຂອງສັດ.
ແນ່ນອນ, ນີ້ບໍ່ແມ່ນກ່ຽວກັບ E. coli ງ່າຍດາຍ, ແຕ່ກ່ຽວກັບການປັບປຸງພັນທຸ ກຳ ແລະມີຄວາມສາມາດໃນການຜະລິດອິນຊູລິນທີ່ຜະລິດໂດຍມະເລັງ, ສ່ວນປະກອບແລະຄຸນສົມບັດຂອງມັນແມ່ນຄືກັນກັບຮໍໂມນທີ່ຜະລິດໂດຍຈຸລັງຂອງກະຕ່າຍຂອງຄົນທີ່ມີສຸຂະພາບດີ.
ຂໍ້ດີຂອງອິນຊູລິນວິສະວະ ກຳ ພັນທຸ ກຳ ບໍ່ພຽງແຕ່ມີຄວາມຄ້າຍຄືກັນຢ່າງແທ້ຈິງກັບຮໍໂມນຂອງມະນຸດເທົ່ານັ້ນ, ແຕ່ຍັງມີຄວາມງ່າຍໃນການກະກຽມ, ປະລິມານວັດຖຸດິບແລະ ຈຳ ນວນທີ່ພຽງພໍ.
ນັກວິທະຍາສາດທົ່ວໂລກເອີ້ນການຜະລິດອິນຊູລິນທີ່ຜະລິດເອງແມ່ນການຄົ້ນພົບທີ່ແທ້ຈິງໃນການຮັກສາໂລກເບົາຫວານ. ຄວາມ ສຳ ຄັນຂອງການຄົ້ນພົບນີ້ແມ່ນໃຫຍ່ຫຼວງແລະ ສຳ ຄັນທີ່ມັນຍາກທີ່ຈະຄິດເກີນຄວາມຈິງ.
ມັນງ່າຍດາຍພໍທີ່ຈະສັງເກດວ່າມື້ນີ້ເກືອບ 95% ຂອງຄວາມຕ້ອງການຂອງຮໍໂມນນີ້ແມ່ນໄດ້ຮັບການຊ່ວຍເຫຼືອຈາກອິນຊູລິນທີ່ໄດ້ຮັບການອອກແບບທາງພັນທຸ ກຳ.
ໃນເວລາດຽວກັນ, ຫລາຍພັນຄົນໃນເມື່ອກ່ອນຜູ້ທີ່ມີອາການແພ້ຢາເສບຕິດໄດ້ຮັບໂອກາດໃນຊີວິດປົກກະຕິ.
ຂ້ອຍເປັນໂຣກເບົາຫວານເປັນເວລາ 31 ປີ. ດຽວນີ້ລາວມີສຸຂະພາບແຂງແຮງດີ. ແຕ່ວ່າ, ແຄບຊູນເຫຼົ່ານີ້ບໍ່ສາມາດເຂົ້າເຖິງໄດ້ ສຳ ລັບຄົນ ທຳ ມະດາ, ພວກເຂົາບໍ່ຕ້ອງການຂາຍຮ້ານຂາຍຢາ, ມັນບໍ່ແມ່ນຜົນ ກຳ ໄລ ສຳ ລັບພວກເຂົາ.
ວິທີອິນຊູລິນວິສະວະ ກຳ ມະນຸດເຮັດວຽກແນວໃດ
ໃນການຮັກສາໂຣກເບົາຫວານປະເພດ 1, ອິນຊູລິນວິສະວະ ກຳ ພັນທຸ ກຳ ຂອງມະນຸດສອງໄລຍະແມ່ນໃຊ້. ໃນຮ້ານຂາຍຢາ, ມັນຖືກຂາຍໃນຮູບແບບຂອງການແກ້ໄຂແລະມີເຄື່ອງ ໝາຍ“ ຮັກ”. ພະຍາດຊະນິດທີສອງຍັງສາມາດປິ່ນປົວດ້ວຍຢາດັ່ງກ່າວຖ້າວ່າຢາທີ່ຖືກ ກຳ ນົດບໍ່ ເໝາະ ສົມກັບຄົນເປັນໂລກເບົາຫວານ.
ຢາອິນຊູລິນທີ່ມີການ ກຳ ເນີດທາງພັນທຸ ກຳ ກໍ່ຖືກ ນຳ ໃຊ້ໃນກໍລະນີທີ່ຄົນເຮົາເປັນໂຣກເບົາຫວານ. ແພດມັກຈະສັ່ງການສັກຢາໃຫ້ແມ່ຍິງຖືພາທີ່ກວດພົບວ່າເປັນໂຣກເບົາຫວານເມື່ອຢາຫຼຸດນ້ ຳ ຕານແລະອາຫານ ບຳ ບັດບໍ່ໄດ້ຊ່ວຍ.
ໂດຍທົ່ວໄປ, insulins ທີ່ໄດ້ຮັບການອອກແບບທາງພັນທຸ ກຳ ຫຼື GMOs ແມ່ນຖືກ ນຳ ໃຊ້ໃນເວລາເກີດລູກ, ໃນເວລາທີ່ພວກເຂົາ ກຳ ລັງຜ່າຕັດ, ຫຼືຖ້າວ່າພະຍາດເບົາຫວານໄດ້ຮັບບາດເຈັບສາຫັດ. ຢາດັ່ງກ່າວຊ່ວຍໃຫ້ທ່ານສາມາດປ່ຽນກັບການໃຊ້ຮໍໂມນທີ່ເຮັດໄດ້ໄວ.
- ກ່ອນທີ່ຈະ ນຳ ໃຊ້ວິສະວະ ກຳ ທາງພັນທຸ ກຳ ຂອງມະນຸດອິນຊູລິນ, ມັນ ຈຳ ເປັນຕ້ອງເຮັດການທົດສອບແລະຄົ້ນພົບວ່າຢາຊະນິດນີ້ ເໝາະ ສົມກັບຄົນເຈັບຫຼືບໍ່. ຖ້າຜູ້ເປັນໂຣກເບົາຫວານສະແດງໃຫ້ເຫັນການເປັນໂຣກເບົາຫວານ, ການໃຊ້ຢາບໍ່ໄດ້ຖືກແນະ ນຳ.
- ໂຄງການຂອງການກະ ທຳ ຂອງການແກ້ໄຂແມ່ນວ່າອິນຊູລິນທີ່ມີການ ກຳ ເນີດທາງພັນທຸ ກຳ ພົວພັນກັບຈຸລັງເຊິ່ງ ນຳ ໄປສູ່ການສ້າງສະລັບສັບຊ້ອນ. ເມື່ອຈຸລັງເຂົ້າສູ່ສະລັບສັບຊ້ອນເຫລົ່ານີ້, ມັນຈະຖືກກະຕຸ້ນແລະເລີ່ມຕົ້ນເຮັດວຽກຢ່າງຫ້າວຫັນ. ດັ່ງນັ້ນ, ຈຶ່ງມີການຜະລິດເອນໄຊຫລາຍຂື້ນ.
- ໃນຂະບວນການ, ທາດນ້ ຳ ຕານຈະຖືກດູດຊຶມໄວຂຶ້ນ, ທາດແປ້ງທີ່ເຂົ້າສູ່ຮ່າງກາຍຈະຖືກປຸງແຕ່ງຢ່າງຈິງຈັງ. ດັ່ງນັ້ນ, ຕັບຜະລິດນ້ ຳ ຕານດົນກວ່າເກົ່າ, ແລະທາດໂປຼຕີນສາມາດດູດຊືມໄດ້ໄວຂື້ນ.
ຫຼັກການຂອງການກະ ທຳ ຂອງຢາແມ່ນຂື້ນກັບຂະ ໜາດ, ປະເພດຂອງອິນຊູລິນ, ທາງເລືອກຂອງບ່ອນສັກຢາ. ຂັ້ນຕອນໃດກໍ່ຕາມຄວນເຮັດໄດ້ພຽງແຕ່ຫຼັງຈາກຕົກລົງກັບແພດທີ່ເຂົ້າຮ່ວມ. ການສັກຢາ ທຳ ອິດແມ່ນເຮັດພາຍໃຕ້ການຊີ້ ນຳ ຂອງແພດ.
ຄຳ ແນະ ນຳ ສຳ ລັບການໃຊ້ຢາ
ເຊັ່ນດຽວກັນກັບຫຼືອິນຊູລິນວິສະວະ ກຳ ພັນທຸ ກຳ ຂອງມະນຸດມີຊື່ການຄ້າທີ່ແຕກຕ່າງກັນ. ນອກຈາກນີ້, ຮໍໂມນສາມາດແຕກຕ່າງກັນໃນໄລຍະເວລາຂອງການປະຕິບັດ, ວິທີການຂອງການກະກຽມການແກ້ໄຂ. ຜະລິດຕະພັນມີຊື່ອີງຕາມປະເພດຂອງອິນຊູລິນ.
Insulins ທີ່ໄດ້ຮັບການອອກແບບທາງພັນທຸ ກຳ ແມ່ນສ່ວນ ໜຶ່ງ ຂອງຢາເຊັ່ນ: Humudar, Vozulim, Actrapid. ການປະກັນໄພ, Gensulin. ນີ້ບໍ່ແມ່ນບັນຊີລາຍຊື່ຄົບຖ້ວນຂອງຢາດັ່ງກ່າວ, ຈຳ ນວນຂອງມັນແມ່ນຂ້ອນຂ້າງໃຫຍ່.
ຢາທັງ ໝົດ ຂ້າງເທິງນີ້ແຕກຕ່າງກັນໃນແງ່ຂອງການ ສຳ ຜັດກັບຮ່າງກາຍ.GMOs ສາມາດໃຊ້ໄດ້ຫຼາຍຊົ່ວໂມງຫລືສາມາດເຄື່ອນໄຫວໄດ້ ໝົດ ມື້.
ຢາປະສົມປະສານສອງໄລຍະລວມມີຢາທີ່ປະກອບມີສ່ວນປະກອບບາງຢ່າງທີ່ປ່ຽນແປງໄລຍະເວລາຂອງການ ສຳ ຜັດກັບຢາ.
- ຢາດັ່ງກ່າວແມ່ນຂາຍໃນຮູບແບບຂອງການປະສົມລວມທັງຮໍໂມນທີ່ໄດ້ຮັບທາງພັນທຸ ກຳ.
- ເງິນເຫຼົ່ານີ້ລວມມີ Mikstard, Insuman, Gansulin, Gensulin.
- ຢາຖືກໃຊ້ສອງຄັ້ງຕໍ່ມື້, ເຄິ່ງຊົ່ວໂມງກ່ອນອາຫານ. ລະບົບດັ່ງກ່າວຄວນໄດ້ຮັບການຍຶດ ໝັ້ນ ຢ່າງເຂັ້ມງວດ, ເພາະວ່າຮໍໂມນມີສ່ວນພົວພັນໂດຍກົງກັບໄລຍະເວລາຂອງການໄດ້ຮັບອາຫານ.
ໂດຍການຜະລິດ gene ຂອງ insulin ຂອງມະນຸດ, ການກະກຽມແມ່ນໄດ້ຮັບເຊິ່ງມີເວລາ ສຳ ຜັດໂດຍສະເລ່ຍ.
- ການແກ້ໄຂມີຜົນບັງຄັບໃຊ້ພາຍໃນ 60 ນາທີ, ແຕ່ຊ່ວງເວລາຂອງກິດຈະ ກຳ ສູງສຸດແມ່ນສັງເກດຈາກເວລາ 6 ຫາ 7 ຊົ່ວໂມງຫຼັງຈາກສັກ.
- ຢາຖືກຍ້າຍອອກຈາກຮ່າງກາຍຢ່າງສົມບູນຫຼັງຈາກ 12 ຊົ່ວໂມງ.
- ຢາດັ່ງກ່າວປະກອບມີ Insuran, Insuman, Protafan, Rinsulin, Biosulin.
ມັນຍັງມີ GMOs ທີ່ມີໄລຍະເວລາສັ້ນໆຂອງການສໍາຜັດກັບຮ່າງກາຍ. ຢາເຫລົ່ານີ້ປະກອບມີຢາ Insulin Actrapid, Gansulin, Humulin, Insuran, Rinsulin, Bioinsulin. insulins ດັ່ງກ່າວມີໄລຍະທີ່ຫ້າວຫັນພາຍຫຼັງສອງຫາສາມຊົ່ວໂມງ, ແລະອາການ ທຳ ອິດຂອງການກະ ທຳ ຂອງຢາສາມາດເຫັນໄດ້ພາຍໃນເຄິ່ງຊົ່ວໂມງຫຼັງຈາກສັກ.
ກ່ອນທີ່ຈະສັກຢາອິນຊູລິນ, GMOs ຕ້ອງໄດ້ຮັບການກວດກາເພື່ອຄວາມໂປ່ງໃສແລະການບໍ່ມີສານຕ່າງປະເທດໃນທາດແຫຼວ. ຖ້າມີສານຕ່າງປະເທດກວດພົບໃນຢາ, ຄວາມວຸ່ນວາຍຫລືຝົນຕົກ, ນ້ ຳ ຢາຈະຕ້ອງຖືກຍົກເລີກ - ຢາບໍ່ ເໝາະ ສົມກັບການ ນຳ ໃຊ້.
ອິນຊູລິນໃຊ້ໃນອຸນຫະພູມຫ້ອງ. ປະລິມານຂອງຮໍໂມນຕ້ອງໄດ້ຮັບການດັດປັບຖ້າວ່າໂຣກເບົາຫວານມີພະຍາດຕິດຕໍ່, ພະຍາດທີ່ກ່ຽວກັບ thyroid, ພະຍາດ Addison, ໂຣກຕັບແຂງ, ແລະພະຍາດ ໝາກ ໄຂ່ຫຼັງ ຊຳ ເຮື້ອ.
ການໂຈມຕີຂອງທາດນ້ ຳ ຕານໃນເລືອດແມ່ນເປັນໄປໄດ້ດ້ວຍການກິນຢາຫຼາຍເກີນໄປ, ໃນກໍລະນີທີ່ມີການປ່ຽນໄປສູ່ລະບົບອິນຊູລິນຊະນິດ ໃໝ່, ເນື່ອງຈາກການກິນອາຫານເກີນ ກຳ ນົດຫລືການໃຊ້ສານເກີນ ກຳ ນົດ. ພ້ອມກັນນັ້ນຄວາມຜິດແມ່ນສາມາດເປັນພະຍາດທີ່ຫຼຸດຜ່ອນຄວາມຕ້ອງການຂອງຮໍໂມນ - ລະດັບທີ່ຮ້າຍແຮງຂອງພະຍາດ ໝາກ ໄຂ່ຫຼັງ, ພະຍາດຕັບ, ການຫຼຸດລົງຂອງຕ່ອມ thyroid, ໂຣກ adrenal, ແລະຕ່ອມນ້ ຳ ມູກ.
- ການຫຼຸດລົງຢ່າງຫຼວງຫຼາຍຂອງນ້ ຳ ຕານໃນເລືອດແມ່ນເປັນໄປໄດ້ໂດຍມີການປ່ຽນແປງບໍລິເວນສັກ. ດັ່ງນັ້ນ, ມັນ ຈຳ ເປັນຕ້ອງປ່ຽນຈາກອິນຊູລິນຊະນິດ ໜຶ່ງ ຢ່າງສົມເຫດສົມຜົນແລະພຽງແຕ່ຫລັງຈາກຕົກລົງກັບແພດທີ່ເຂົ້າຮ່ວມ.
- ຖ້າຜູ້ເປັນໂລກເບົາຫວານໃຊ້ອິນຊູລິນໃນໄລຍະສັ້ນ, ບາງຄັ້ງປະລິມານຂອງເນື້ອເຍື່ອໄຂມັນຫຼຸດລົງຢູ່ບ່ອນສັກຢາຫຼືກົງກັນຂ້າມ, ເພີ່ມຂື້ນ. ເພື່ອປ້ອງກັນສິ່ງນີ້, ການສັກຢາຕ້ອງໄດ້ເຮັດຢູ່ບ່ອນທີ່ແຕກຕ່າງກັນ.
ແມ່ຍິງຖືພາຕ້ອງຮູ້ວ່າຂໍ້ ກຳ ນົດຂອງອິນຊູລິນອາດຈະແຕກຕ່າງກັນໃນໄລຍະທີ່ແຕກຕ່າງກັນຂອງການຖືພາ. ເພື່ອເຮັດສິ່ງນີ້, ທ່ານ ຈຳ ເປັນຕ້ອງ ດຳ ເນີນການທົດສອບນ້ ຳ ຕານໃນເລືອດທຸກໆມື້ດ້ວຍນ້ ຳ ລາຍເຫຼື້ອມ.
ການກະ ທຳ ຂອງອິນຊູລິນໃນຮ່າງກາຍຂອງມະນຸດແມ່ນຖືກອະທິບາຍໄວ້ໃນລາຍລະອຽດໃນວິດີໂອໃນບົດຂຽນນີ້.
1. ໂຄງສ້າງແລະ ໜ້າ ທີ່ຂອງອິນຊູລິນ 5
1.1. ໂຄງສ້າງຂອງໂມເລກຸນອິນຊູລິນ 5
1.2. ຄວາມ ສຳ ຄັນທາງຊີວະພາບຂອງອິນຊູລິນ 7
1.3. ການຍັບຍັ້ງການວິເຄາະທາງອິນຊີ 8
2. ການສັງເຄາະອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ 10
2.1. ການໃຊ້ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ ສຳ ລັບການສັງເຄາະຢາ 10
2.2. ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ 11
2.3. ການຜະລິດອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ 14

ບົດສະຫຼຸບ 18
ອາການເກີນ
ເມື່ອໃຊ້ອິນຊູລິນ, ມັນເປັນສິ່ງ ສຳ ຄັນທີ່ຈະຕ້ອງປະຕິບັດຕາມ ຄຳ ແນະ ນຳ ຂອງທ່ານ ໝໍ ແລະສັງເກດປະລິມານຢາທີ່ຖືກ ກຳ ນົດ.
ໃນກໍລະນີທີ່ບໍ່ປະຕິບັດຕາມກົດລະບຽບແລະການກິນຫຼາຍເກີນໄປ, ຜູ້ເປັນໂລກເບົາຫວານເລີ່ມມີອາການເຈັບຫົວຢ່າງຮຸນແຮງ, ປວດທ້ອງ, ຫິວໂຫຍ, ເຫື່ອອອກ, ອັດຕາການເຕັ້ນຂອງຫົວໃຈ, ຄົນເຮົາກາຍເປັນຄົນທີ່ເຮັດວຽກ ໜັກ ເກີນໄປ, ເຮັດໃຫ້ເກີດອາການຄັນຄາຍ. ອາການ ໜາວ ສັ່ນໃນຮ່າງກາຍແລະສັ່ນສະເທືອນຍັງສາມາດສັງເກດໄດ້.
ອາການດັ່ງກ່າວແມ່ນຄ້າຍຄືກັນກັບສັນຍານຂອງການຫຼຸດລົງຂອງນ້ ຳ ຕານໃນເລືອດ.ດ້ວຍຂັ້ນຕອນຂອງອາການທີ່ບໍ່ຮຸນແຮງ, ຜູ້ເປັນໂລກເບົາຫວານສາມາດແກ້ໄຂບັນຫາໄດ້ຢ່າງອິດສະຫຼະແລະປັບປຸງສະພາບການ. ເພື່ອເຮັດສິ່ງນີ້, ກິນເຂົ້າ ໜົມ ອົມຫຼືຜະລິດຕະພັນຫວານອື່ນໆທີ່ປະກອບດ້ວຍນ້ ຳ ຕານ.
- ຖ້າຫາກວ່າເປັນໂຣກເບົາຫວານເກີດຂື້ນ, ພວກເຂົາໃຊ້ວິທີແກ້ໄຂບັນຫາ, ຢາຈະຖືກຄວບຄຸມຈົນກ່ວາຄົນເຈັບສະຕິ. ໃນອາການທີ່ ໜ້າ ສົງໄສຄັ້ງ ທຳ ອິດ, ມັນ ຈຳ ເປັນຕ້ອງໂທຫາລົດສຸກເສີນ, ເຊິ່ງຈະສາມາດ ນຳ ຄົນເຈັບໄປສູ່ຊີວິດໂດຍວິທີການສຸກເສີນ.
- ເປັນຜົນຂ້າງຄຽງຫລັງຈາກການໃຊ້ GMOs, ຄົນເຮົາຈະມີຕຸ່ມຜື່ນຕາມຜິວ ໜັງ ເປັນຮູບປະກອບ urticaria, ສ່ວນຕ່າງໆຂອງຮ່າງກາຍໃຄ່, ຄວາມດັນເລືອດຈະລຸດລົງຢ່າງແຮງ, ອາການຄັນແລະຫາຍໃຈສັ້ນກໍ່ຈະເກີດຂື້ນ. ນີ້ແມ່ນປະຕິກິລິຍາແພ້ຕໍ່ຢາ, ເຊິ່ງຫລັງຈາກນັ້ນກໍ່ຫາຍໄປເອງໂດຍບໍ່ມີການແຊກແຊງທາງການແພດ. ຖ້າສະຖານະການຍັງສືບຕໍ່, ທ່ານຄວນປຶກສາທ່ານຫມໍຂອງທ່ານ.
- ໃນມື້ ທຳ ອິດຂອງການກະກຽມອິນຊູລິນ, ຜູ້ເປັນໂລກເບົາຫວານມັກຈະເຮັດໃຫ້ຮ່າງກາຍຂາດນ້ ຳ, ຄົນເຮົາປະສົບກັບການຂາດນ້ ຳ, ຄວາມຢາກອາຫານຮ້າຍແຮງຂຶ້ນ, ມີອາການບວມຢູ່ແຂນແລະຂາ, ແລະມີອາການງ້ວງນອນຢູ່ເລື້ອຍໆ. ອາການແບບນີ້ມັກຈະຫາຍໄປໄວແລະບໍ່ເກີດຂື້ນອີກ.
ຄຳ ຄິດເຫັນແລະ ຄຳ ເຫັນ
ຂ້ອຍເປັນໂຣກເບົາຫວານປະເພດ 2 - ບໍ່ແມ່ນອິນຊູລິນ. ເພື່ອນຄົນ ໜຶ່ງ ໄດ້ແນະ ນຳ ໃຫ້ຫຼຸດນ້ ຳ ຕານໃນເລືອດກັບ DiabeNot. ຂ້ອຍໄດ້ສັ່ງຊື້ຜ່ານອິນເຕີເນັດ. ເລີ່ມຕົ້ນການຕ້ອນຮັບ.
ຂ້ອຍປະຕິບັດຕາມອາຫານທີ່ບໍ່ເຂັ້ມງວດ, ທຸກໆເຊົ້າຂ້ອຍເລີ່ມຍ່າງປະມານ 2-3 ກິໂລແມັດ. ໃນໄລຍະສອງອາທິດທີ່ຜ່ານມາ, ຂ້າພະເຈົ້າສັງເກດເຫັນການຫຼຸດລົງຂອງນ້ ຳ ຕານທີ່ລຽບໃນແມັດໃນຕອນເຊົ້າກ່ອນອາຫານເຊົ້າຈາກ 9.3 ເຖິງ 7.1, ແລະເຖິງແມ່ນວ່າຮອດ 6 ມື້ວານນີ້.
1! ຂ້ອຍຮຽນຕໍ່ວິທີປ້ອງກັນ. ຂ້ອຍຈະສະ ໝັກ ກ່ຽວກັບຄວາມ ສຳ ເລັດ.
Margarita Pavlovna, ຂ້ອຍຍັງນັ່ງຢູ່ Diabenot ດຽວນີ້. SD 2. ຂ້ອຍບໍ່ມີເວລາ ສຳ ລັບອາຫານການກິນແລະຍ່າງ, ແຕ່ຂ້ອຍບໍ່ໄດ້ລ່ວງລະເມີດເຂົ້າ ໜົມ ຫວານແລະທາດແປ້ງ, ຂ້ອຍຄິດວ່າ XE, ແຕ່ຍ້ອນອາຍຸ, ນ້ ຳ ຕານຍັງສູງ.
ຜົນໄດ້ຮັບກໍ່ບໍ່ໄດ້ດີເທົ່າກັບທ່ານ, ແຕ່ ສຳ ລັບນ້ ຳ ຕານ 7.0 ກໍ່ບໍ່ອອກມາເປັນເວລາ ໜຶ່ງ ອາທິດ. ທ່ານຄິດແນວໃດກັບນໍ້າຕານກັບ? ລາວສະແດງໃຫ້ເຈົ້າເຫັນ plasma ຫຼືເລືອດທັງ ໝົດ ບໍ? ຂ້ອຍຕ້ອງການປຽບທຽບຜົນໄດ້ຮັບຈາກການກິນຢາ.
ຂອບໃຈຫຼາຍໆ ສຳ ລັບການໂພສຂໍ້ມູນດັ່ງກ່າວ.
ການຜະລິດອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ

ເພື່ອເຮັດໃຫ້ບຸກຄົນມີຄວາມຮູ້ສຶກມີສຸຂະພາບແຂງແຮງ, ທ່ານ ຈຳ ເປັນຕ້ອງຕິດຕາມລະດັບອິນຊູລິນໃນຮ່າງກາຍ. ຮໍໂມນນີ້ຄວນຈະພຽງພໍເພື່ອໃຫ້ glucose ບໍ່ສະສົມໃນເລືອດ. ຖ້າບໍ່ດັ່ງນັ້ນ, ໃນກໍລະນີທີ່ມີຄວາມຜິດປົກກະຕິກ່ຽວກັບລະບົບທາງເດີນອາຫານ, ທ່ານ ໝໍ ຈະກວດພະຍາດເບົາຫວານ.
ການປິ່ນປົວ ສຳ ລັບຂັ້ນຕອນທີ່ກ້າວ ໜ້າ ຂອງໂລກເບົາຫວານແມ່ນເພື່ອເພີ່ມຄວາມເຂັ້ມຂົ້ນຂອງອິນຊູລິນ, ເຊິ່ງຮ່າງກາຍບໍ່ສາມາດຜະລິດໄດ້ຈາກ ທຳ ມະຊາດ. ສຳ ລັບສິ່ງນີ້, ທາດອິນຊູລິນລະລາຍຈະຖືກ ນຳ ໃຊ້, ເຊິ່ງຄ້າຍຄືກັນກັບເຄື່ອງຈັກ ກຳ ມະພັນຂອງມະນຸດ. ພະຍາດຕັບແມ່ນຮັບຜິດຊອບໃນການຜະລິດຮໍໂມນດັ່ງກ່າວ.
ສຳ ລັບການຜະລິດອິນຊູລິນບໍ່ພຽງແຕ່ ນຳ ໃຊ້ເຕັກໂນໂລຢີ ສຳ ລັບການຜະລິດຮໍໂມນ ທຳ ມະຊາດເທົ່ານັ້ນ, ຜູ້ຜະລິດຍັງໃຊ້ອິນຊູລິນທີ່ໄດ້ຮັບການປ່ຽນແປງແບບທຽມ. ຢາທີ່ມີຊື່ວ່າ "solubilis" ແມ່ນຖືກລະບຸວ່າເປັນຕົວລະລາຍ.
ປະເພດຢາ
ເຊັ່ນດຽວກັນກັບຫຼືອິນຊູລິນວິສະວະ ກຳ ພັນທຸ ກຳ ຂອງມະນຸດມີຊື່ການຄ້າທີ່ແຕກຕ່າງກັນ. ນອກຈາກນີ້, ຮໍໂມນສາມາດແຕກຕ່າງກັນໃນໄລຍະເວລາຂອງການປະຕິບັດ, ວິທີການຂອງການກະກຽມການແກ້ໄຂ. ຜະລິດຕະພັນມີຊື່ອີງຕາມປະເພດຂອງອິນຊູລິນ.
Insulins ທີ່ໄດ້ຮັບການອອກແບບທາງພັນທຸ ກຳ ແມ່ນສ່ວນ ໜຶ່ງ ຂອງຢາເຊັ່ນ: Humudar, Vozulim, Actrapid. ການປະກັນໄພ, Gensulin. ນີ້ບໍ່ແມ່ນບັນຊີລາຍຊື່ຄົບຖ້ວນຂອງຢາດັ່ງກ່າວ, ຈຳ ນວນຂອງມັນແມ່ນຂ້ອນຂ້າງໃຫຍ່.
ຢາທັງ ໝົດ ຂ້າງເທິງນີ້ແຕກຕ່າງກັນໃນແງ່ຂອງການ ສຳ ຜັດກັບຮ່າງກາຍ. GMOs ສາມາດໃຊ້ໄດ້ຫຼາຍຊົ່ວໂມງຫລືສາມາດເຄື່ອນໄຫວໄດ້ ໝົດ ມື້.
ຢາປະສົມປະສານສອງໄລຍະລວມມີຢາທີ່ປະກອບມີສ່ວນປະກອບບາງຢ່າງທີ່ປ່ຽນແປງໄລຍະເວລາຂອງການ ສຳ ຜັດກັບຢາ.
- ຢາດັ່ງກ່າວແມ່ນຂາຍໃນຮູບແບບຂອງການປະສົມລວມທັງຮໍໂມນທີ່ໄດ້ຮັບທາງພັນທຸ ກຳ.
- ເງິນເຫຼົ່ານີ້ລວມມີ Mikstard, Insuman, Gansulin, Gensulin.
- ຢາຖືກໃຊ້ສອງຄັ້ງຕໍ່ມື້, ເຄິ່ງຊົ່ວໂມງກ່ອນອາຫານ. ລະບົບດັ່ງກ່າວຄວນໄດ້ຮັບການຍຶດ ໝັ້ນ ຢ່າງເຂັ້ມງວດ, ເພາະວ່າຮໍໂມນມີສ່ວນພົວພັນໂດຍກົງກັບໄລຍະເວລາຂອງການໄດ້ຮັບອາຫານ.
ໂດຍການຜະລິດ gene ຂອງ insulin ຂອງມະນຸດ, ການກະກຽມແມ່ນໄດ້ຮັບເຊິ່ງມີເວລາ ສຳ ຜັດໂດຍສະເລ່ຍ.
- ການແກ້ໄຂມີຜົນບັງຄັບໃຊ້ພາຍໃນ 60 ນາທີ, ແຕ່ຊ່ວງເວລາຂອງກິດຈະ ກຳ ສູງສຸດແມ່ນສັງເກດຈາກເວລາ 6 ຫາ 7 ຊົ່ວໂມງຫຼັງຈາກສັກ.
- ຢາຖືກຍ້າຍອອກຈາກຮ່າງກາຍຢ່າງສົມບູນຫຼັງຈາກ 12 ຊົ່ວໂມງ.
- ຢາດັ່ງກ່າວປະກອບມີ Insuran, Insuman, Protafan, Rinsulin, Biosulin.
ມັນຍັງມີ GMOs ທີ່ມີໄລຍະເວລາສັ້ນໆຂອງການສໍາຜັດກັບຮ່າງກາຍ. ຢາເຫລົ່ານີ້ປະກອບມີຢາ Insulin Actrapid, Gansulin, Humulin, Insuran, Rinsulin, Bioinsulin. insulins ດັ່ງກ່າວມີໄລຍະທີ່ຫ້າວຫັນພາຍຫຼັງສອງຫາສາມຊົ່ວໂມງ, ແລະອາການ ທຳ ອິດຂອງການກະ ທຳ ຂອງຢາສາມາດເຫັນໄດ້ພາຍໃນເຄິ່ງຊົ່ວໂມງຫຼັງຈາກສັກ.
ຢາດັ່ງກ່າວແມ່ນຖືກຂັບຖ່າຍ ໝົດ ພາຍຫຼັງຫົກຊົ່ວໂມງ.
ການ ນຳ ໃຊ້ອິນຊູລິນທີ່ລະລາຍໂດຍວິສະວະ ກຳ ມະນຸດ ສຳ ລັບພະຍາດເບົາຫວານ

ອິນຊູລິນທີ່ມີການ ກຳ ເນີດທາງພັນທຸ ກຳ ຂອງມະນຸດແມ່ນການທົດແທນຮໍໂມນທົ່ວໄປ ສຳ ລັບອິນຊູລິນທີ່ຜະລິດກະຕຸກ. ບໍ່ພຽງແຕ່ຮໍໂມນມະນຸດທີ່ມີການປ່ຽນແປງທາງພັນທຸ ກຳ ເທົ່ານັ້ນທີ່ໃຊ້ ສຳ ລັບການສັງເຄາະ, ແຕ່ຍັງມີສານທີ່ສ້າງຂື້ນໂດຍທາງສັງເຄາະ. ຕົວເລືອກທີ່ມີຊື່ສຽງອີກຢ່າງ ໜຶ່ງ ສຳ ລັບການສ້າງຢາແມ່ນການໃຊ້ອິນຊູລິນ ໝູ ທີ່ຖືກປ່ຽນແປງ, ເພາະວ່າ ໃນສ່ວນປະກອບແລະ ໜ້າ ທີ່ຂອງມັນ, ມັນໃກ້ຄຽງກັບມະນຸດ. ຕາຕະລາງການຜະລິດອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ. ຢາອິນຊູລິນທີ່ຜະລິດໂດຍທາງພັນທຸ ກຳ ສາມາດໃຊ້ໄດ້ທັງພະຍາດເບົາຫວານຊະນິດ 1 ແລະພະຍາດເບົາຫວານຊະນິດທີ 2, ເມື່ອມີປະຕິກິລິຍາຢ່າງຕໍ່ເນື່ອງກັບຢາໃນປາກທີ່ມີລັກສະນະເປັນທາດ ນຳ ້ຕານໃນເລືອດ. ມັນສາມາດໃຊ້ໃນເວລາທີ່ຄົນເຈັບຢູ່ໃນສະພາບເສີຍໆບາງຢ່າງ. ຖ້າແມ່ຍິງຖືພາ ກຳ ລັງເລີ່ມເປັນໂລກເບົາຫວານ, ຫຼັງຈາກນັ້ນການ ນຳ ໃຊ້ອິນຊູລິນວິສະວະ ກຳ ສາດແມ່ນໄດ້ຮັບອະນຸຍາດ, ແຕ່ຖ້າອາຫານບໍ່ຊ່ວຍໃຫ້ມີຜົນຕໍ່ລະດັບ glucose. ການນໍາໃຊ້ຂອງມັນແມ່ນແນະນໍາໃຫ້ໃນກໍລະນີທີ່ມີການຕິດເຊື້ອທີ່ມີການຕິດເຊື້ອທີ່ hyperthermia ສາມາດສັງເກດໄດ້. ການກະກຽມເຊື້ອສາຍແມ່ນປະສົບຜົນ ສຳ ເລັດໃນການ ນຳ ໃຊ້ໃນໄລຍະເກີດລູກ, ການປະຕິບັດງານ, ການບາດເຈັບ, ຄວາມຜິດປົກກະຕິຂອງລະບົບທາງເດີນອາຫານແລະໃນກໍລະນີທີ່ຄ່ອຍໆຫັນປ່ຽນໄປສູ່ອິນຊູລິນດ້ວຍການກະ ທຳ ທີ່ຍາວນານ. ມັນຖືກຫ້າມບໍ່ໃຫ້ໃຊ້ການກະກຽມເຊື້ອພັນໂດຍທົດແທນຮໍໂມນດ້ວຍຄວາມກົດດັນໃນການເຮັດວຽກກັບບາງສ່ວນຂອງຢາແລະດ້ວຍການທີ່ມີທາດນ້ ຳ ຕານໃນເລືອດ. ຢາເສບຕິດຂອງປະເພດນີ້ມີປະຕິກິລິຍາກັບຕົວຮັບຂອງຈຸລັງທີ່ແນ່ນອນ, ສ້າງສະລັບສັບຊ້ອນກັບພວກມັນ. ເມື່ອມັນເຂົ້າໄປໃນຈຸລັງ, ສະລັບສັບຊ້ອນຂອງຢາມີຜົນກະທົບຕໍ່ການເຮັດວຽກ, ກະຕຸ້ນໃຫ້ມັນມີການເຄື່ອນໄຫວຫຼາຍຂຶ້ນແລະຜະລິດເອນໄຊເພີ່ມເຕີມ. ລະດັບນໍ້າຕານຫຼຸດລົງເນື່ອງຈາກຄວາມຈິງທີ່ວ່າມັນຖືກປຸງແຕ່ງໄວຂື້ນໂດຍຈຸລັງ. ຫລັງຈາກນັ້ນ, ຂະບວນການຂອງ lipogenesis, ການຜະລິດທາດໂປຼຕີນໄດ້ຖືກເລັ່ງແລະຄວາມໄວຂອງຕັບໃນການສ້າງໂກເລດແມ່ນຫຼຸດລົງ. ໄລຍະເວລາຂອງຢາຈະຂື້ນກັບສະຖານທີ່ສັກ, ປະເພດຢາ, ຂະ ໜາດ ແລະການຕອບສະ ໜອງ ຂອງຮ່າງກາຍຂອງຄົນ. ມີພຽງແຕ່ທ່ານ ໝໍ ເທົ່ານັ້ນທີ່ສາມາດ ກຳ ນົດປະລິມານຢາແລະສັ່ງຢາບາງຊະນິດໃນກຸ່ມນີ້. ໃນໄລຍະເລີ່ມຕົ້ນຂອງການໃຊ້ຢາ, ຄົນເຈັບໄດ້ຮັບການຕິດຕາມກວດກາຈາກແພດ ໝໍ ຢ່າງໃກ້ຊິດເພື່ອຮູ້ວ່າຢາຖືກປະຕິເສດ. ຢາອິນຊູລິນທີ່ຜະລິດໂດຍມະນຸດແມ່ນມີຢູ່ໃນຢາທີ່ມີຊື່ສຽງເຊັ່ນ: Insuran, Insuman, Vozulim, Penfill, Biosulin, Gensulin, Actrapid, Rinsulin, Humulin, Humudar, Rosinsulin ແລະບາງຊະນິດອື່ນໆ. ມີ insulin ຫຼາຍຊະນິດ.ຫນຶ່ງໃນການຈັດປະເພດທີ່ກ່ຽວຂ້ອງກັບໄລຍະເວລາຂອງຢາ. ອີງຕາມນາງ, insulin ລະລາຍສາມາດມີການກະ ທຳ ສັ້ນແລະຍາວ. ມີຢາເສບຕິດປະສົມປະສານ (insulin biphasic), ເຊິ່ງບັນຈຸສານທີ່ມີທັງການກະ ທຳ ໄວແລະຍາວນານ. ຢາຊະນິດນີ້ເອີ້ນວ່າການປະສົມ. ໃນນັ້ນມີຜູ້ທີ່ຖືກສ້າງຂື້ນດ້ວຍການປ່ຽນແປງຂອງຮໍໂມນຂອງມະນຸດ. Insulin ສອງໄລຍະແມ່ນ Mikstard, Gansulin, Insuman, Humulin ແລະ Gensulin. ພວກເຂົາຕ້ອງໄດ້ໃຊ້ສອງຄັ້ງຕໍ່ມື້, ເຄິ່ງຊົ່ວໂມງກ່ອນອາຫານ. ນີ້ແມ່ນເນື່ອງມາຈາກຄວາມຈິງທີ່ວ່າອິນຊູລິນສອງໄລຍະມີສານທີ່ເຮັດວຽກສັ້ນ, ການໄດ້ຮັບສານແມ່ນຂື້ນກັບອາຫານ. ການປຽບທຽບດ້ານວິສະວະ ກຳ ຂອງຮໍໂມນມະນຸດແມ່ນໃນບັນດາຢາທີ່ມີໄລຍະເວລາສະເລ່ຍ. insulin ລະລາຍນີ້ເລີ່ມປະຕິບັດພາຍຫຼັງ ໜຶ່ງ ຊົ່ວໂມງ, ແລະຈຸດສູງສຸດຂອງກິດຈະ ກຳ ຂອງມັນແມ່ນເກີດຂື້ນພາຍຫຼັງ 7 ຊົ່ວໂມງ. ຫຼັງຈາກ 12 ຊົ່ວໂມງ, ມັນຖືກສະແດງ. ຢາທີ່ຜະລິດໂດຍ ກຳ ມະພັນຂອງມະນຸດກຸ່ມນີ້ແມ່ນ Insuman, Protafan, Humulin, Rinsulin, Biosulin, Gensulin, Gansulin, Insuran. ມີຢາທີ່ໄດ້ຮັບການອອກ ກຳ ລັງກາຍຈາກມະນຸດໃນກຸ່ມກຸ່ມດ້ວຍການກະ ທຳ ສັ້ນ. ຍົກຕົວຢ່າງ, ເຫຼົ່ານີ້ລວມມີ Gansulin, Insuran, Humulin, Rinsulin, Gensulin, Bioinsulin ແລະ Actrapid. ອິນຊູລິນລະລາຍດັ່ງກ່າວເລີ່ມປະຕິບັດໃນເວລາເຄິ່ງຊົ່ວໂມງ, ແລະກິດຈະ ກຳ ຂອງມັນຮອດລະດັບສູງສຸດພາຍໃນສອງສາມຊົ່ວໂມງ. ຢາດັ່ງກ່າວແມ່ນຖືກໄລ່ອອກເປັນເວລາ 6 ຊົ່ວໂມງ. ໃນກໍລະນີທີ່ກິນຢາເກີນປະລິມານທີ່ມີອິນຊູລິນທີ່ຜະລິດໂດຍ ກຳ ມະພັນ, ອ່ອນເພຍ, ເຫງົານອນ, ເມື່ອຍລ້າ, ອາການຄັນຄາຍ, ໜາວ ສັ່ນ, ເພີ່ມຂື້ນຂອງເຫື່ອເຢັນ, ການສັ່ນສະເທືອນ, ປັ່ນປ່ວນ, palpitations, ອາການເຈັບຫົວ, ປວດແລະຄວາມອຶດຢາກສາມາດເກີດຂື້ນໄດ້. ທັງ ໝົດ ເຫຼົ່ານີ້ແມ່ນອາການຂອງການເປັນໂລກເບົາຫວານ. ຖ້າວ່າພະຍາດນີ້ຫາກໍ່ເລີ່ມພັດທະນາແລະຢູ່ໃນໄລຍະກ່ອນໆ, ງ່າຍກວ່າ, ຫຼັງຈາກນັ້ນທ່ານສາມາດ ກຳ ຈັດອາການທັງ ໝົດ ອອກດ້ວຍຕົວທ່ານເອງ. ເພື່ອເຮັດສິ່ງນີ້, ທ່ານ ຈຳ ເປັນຕ້ອງກິນອາຫານທີ່ມີນ້ ຳ ຕານແລະມີຄາໂບໄຮເດຣດສູງເຊິ່ງສາມາດຍ່ອຍໄດ້ງ່າຍ. ການແກ້ໄຂບັນຫາ Glucagon ແລະ dextrose ສາມາດຖືກແນະ ນຳ ເຂົ້າໃນຮ່າງກາຍ. ຖ້າບຸກຄົນໃດ ໜຶ່ງ ຕົກຢູ່ໃນສະຕິ, ທ່ານ ຈຳ ເປັນຕ້ອງສັກວິທີແກ້ໄຂ dextrose ທີ່ປ່ຽນແປງຈົນກວ່າສະຖານະການຈະດີຂື້ນ. ບາງຄົນອາດຈະເກີດອາການແພ້ຕໍ່ການໃຊ້ຢາທີ່ຖືກດັດແປງພັນທຸ ກຳ ກັບອິນຊູລິນ. ອາການຕ່າງໆອາດປະກອບມີອາການຄັນ, ໃຄ່ບວມ, ສູນເສຍຄວາມແຂງແຮງ, ຄວາມດັນເລືອດຕໍ່າ, ຫາຍໃຈສັ້ນ, ຜື່ນ, ໄຂ້, ແລະຄັນ. ໃນບາງກໍລະນີ, ການລະລາຍນ້ ຳ ຕານໃນເລືອດແລະອາການມຶນເມົາເກີດຂື້ນ. ບັນຫາກ່ຽວກັບສະຕິຂອງມະນຸດແລະແມ່ນແຕ່ສະຕິບໍ່ສາມາດເກີດຂື້ນໄດ້. ຖ້າຄົນເຈັບຂາດຢາ, ຫຼັງຈາກນັ້ນລາວອາດຈະພັດທະນາ hyperglycemia. ມັນປະກົດວ່າເນື່ອງຈາກປະລິມານທີ່ຕໍ່າໃນເບື້ອງຕົ້ນ, ດ້ວຍການພັດທະນາຂອງປະກົດການຕິດເຊື້ອໃນຮ່າງກາຍ, ແລະຍັງຖ້າທ່ານບໍ່ປະຕິບັດຕາມກົດລະບຽບຂອງຄາບອາຫານ. ໃນບາງກໍລະນີ, ຄົນເຈັບອາດຈະພັດທະນາ lipodystrophy ໃນສະຖານທີ່ທີ່ໃຊ້ຢາ. ໃນໄລຍະເລີ່ມຕົ້ນຂອງການໃຊ້ຢາ, ຄວາມອວດຕົວ, ການຂາດນ້ ຳ, ຄວາມງ້ວງເຫງົາແລະຄວາມຢາກອາຫານອາດຈະເກີດຂື້ນ. ແຕ່ປະກົດການເຫລົ່ານີ້ແມ່ນຊົ່ວຄາວ. ການໃຊ້ແທນອິນຊູລິນ ທຳ ມະຊາດເຊັ່ນ: ສານທີ່ຜະລິດໂດຍ ກຳ ມະພັນແມ່ນສານເສີມທີ່ດີເລີດໃນການຮັກສາໂລກເບົາຫວານ. ມັນຊ່ວຍໃນການຫຼຸດລະດັບນໍ້າຕານເນື່ອງຈາກຄວາມຈິງທີ່ວ່າທາດນ້ ຳ ຕານໄດ້ຮັບການດູດຊຶມຈາກຈຸລັງຫຼາຍຂື້ນ, ແລະຂະບວນການຂອງການຂົນສົ່ງກໍ່ປ່ຽນໄປ. ແຕ່ວ່າຢາເຫຼົ່ານີ້ ຈຳ ເປັນຕ້ອງໄດ້ຖືກ ນຳ ໃຊ້ຢ່າງເຂັ້ມງວດຕາມໃບສັ່ງແພດຂອງທ່ານ ໝໍ, ເພາະວ່າ ມັນສາມາດສົ່ງຜົນກະທົບຕໍ່ສຸຂະພາບທີ່ບໍ່ຕ້ອງການ ສຳ ລັບຄົນເຈັບ. Insulin ແມ່ນຢາຕົ້ນຕໍ ສຳ ລັບປິ່ນປົວໂຣກເບົາຫວານປະເພດ 1. ບາງຄັ້ງມັນຍັງຖືກ ນຳ ໃຊ້ເພື່ອເຮັດໃຫ້ຄົນເຈັບມີສະຖຽນລະພາບແລະປັບປຸງສະຫວັດດີພາບຂອງລາວໃນປະເພດພະຍາດທີ່ສອງ. ສານນີ້ໂດຍ ທຳ ມະຊາດຂອງມັນແມ່ນຮໍໂມນທີ່ມີຄວາມສາມາດສົ່ງຜົນກະທົບຕໍ່ການເຜົາຜະຫລານທາດແປ້ງໃນປະລິມານ ໜ້ອຍ. ໂດຍປົກກະຕິ, ກະຕຸກຈະຜະລິດອິນຊູລິນພຽງພໍ, ເຊິ່ງຊ່ວຍຮັກສາລະດັບການເຄື່ອນໄຫວຂອງນ້ ຳ ຕານໃນເລືອດ. ແຕ່ວ່າມີຄວາມຜິດປົກກະຕິຂອງໂຣກ endocrine ທີ່ຮ້າຍແຮງ, ໂອກາດດຽວທີ່ຈະຊ່ວຍຄົນເຈັບເລື້ອຍໆແມ່ນການສັກຢາອິນຊູລິນຢ່າງຊັດເຈນ. ແຕ່ຫນ້າເສຍດາຍ, ມັນເປັນໄປບໍ່ໄດ້ທີ່ຈະກິນມັນທາງປາກ (ໃນຮູບແບບຂອງເມັດ), ເພາະວ່າມັນຖືກ ທຳ ລາຍຢ່າງສົມບູນໃນທໍ່ຍ່ອຍອາຫານແລະສູນເສຍຄຸນຄ່າທາງຊີວະພາບຂອງມັນ. ການໄດ້ຮັບຮໍໂມນຮໍໂມນນີ້ຈາກ ໝູ ແລະຫມູແມ່ນເຕັກໂນໂລຢີເກົ່າທີ່ຫາຍາກໃນປະຈຸບັນນີ້. ນີ້ແມ່ນເນື່ອງມາຈາກຄຸນນະພາບຕໍ່າຂອງຢາທີ່ໄດ້ຮັບ, ແນວໂນ້ມຂອງມັນທີ່ຈະເຮັດໃຫ້ເກີດອາການແພ້ແລະລະດັບການບໍລິສຸດບໍ່ພຽງພໍ. ຄວາມຈິງແມ່ນວ່າເນື່ອງຈາກວ່າຮໍໂມນແມ່ນສານທາດໂປຼຕີນ, ມັນປະກອບດ້ວຍຊຸດອາຊິດ amino ທີ່ແນ່ນອນ. ທາດອິນຊູລິນທີ່ຜະລິດໃນຮ່າງກາຍຂອງ ໝູ ແຕກຕ່າງກັນໃນສ່ວນປະກອບຂອງກົດອະມິໂນຈາກອິນຊູລິນຂອງມະນຸດໂດຍ 1 ອາຊິດ amino, ແລະ insulin bovine ໂດຍ 3. ໃນຕອນເລີ່ມຕົ້ນແລະກາງຂອງສະຕະວັດທີ 20, ໃນເວລາທີ່ບໍ່ມີຢາຄ້າຍຄືກັນ, ເຖິງແມ່ນວ່າອິນຊູລິນດັ່ງກ່າວກໍ່ແມ່ນການຄົ້ນພົບທາງດ້ານການແພດແລະຊ່ວຍໃຫ້ການປິ່ນປົວຄົນເຈັບເບົາຫວານໃນລະດັບ ໃໝ່. ຮໍໂມນທີ່ໄດ້ຮັບໂດຍວິທີການນີ້ເຮັດໃຫ້ນ້ ຳ ຕານໃນເລືອດຫຼຸດລົງ, ແຕ່ວ່າມັນມັກຈະເຮັດໃຫ້ເກີດຜົນຂ້າງຄຽງແລະອາການແພ້. ຄວາມແຕກຕ່າງຂອງສ່ວນປະກອບຂອງກົດອະມິໂນແລະຄວາມບໍ່ສະອາດໃນຢາມີຜົນກະທົບຕໍ່ສະພາບຂອງຄົນເຈັບ, ໂດຍສະເພາະໃນ ໝວດ ຄົນເຈັບທີ່ມີຄວາມສ່ຽງຫຼາຍກວ່າເກົ່າ (ເດັກນ້ອຍແລະຜູ້ເຖົ້າ). ເຫດຜົນອີກຢ່າງ ໜຶ່ງ ທີ່ເຮັດໃຫ້ຄວາມອົດທົນບໍ່ດີຂອງອິນຊູລິນດັ່ງກ່າວແມ່ນການປະກົດຕົວຂອງຢາທີ່ບໍ່ມີປະສິດຕິພາບໃນຢາ (proinsulin), ເຊິ່ງເປັນໄປບໍ່ໄດ້ທີ່ຈະ ກຳ ຈັດຄວາມແຕກຕ່າງຂອງຢານີ້ໄດ້. ປະຈຸບັນນີ້ມີ insulins ໝູ ທີ່ກ້າວ ໜ້າ ເຊິ່ງບໍ່ມີຂໍ້ບົກຜ່ອງເຫຼົ່ານີ້. ພວກມັນໄດ້ຮັບຈາກຕັບຂອງ ໝູ, ແຕ່ຫລັງຈາກນັ້ນພວກມັນຕ້ອງໄດ້ຜ່ານການປຸງແຕ່ງແລະການກັ່ນຕອງຕື່ມ. ພວກເຂົາແມ່ນ multicomponent ແລະມີຕົວແທນ. ອິນຊູລິນຊີ້ນ ໝູ ທີ່ຖືກປ່ຽນແປງແມ່ນປະຕິບັດບໍ່ແຕກຕ່າງຈາກຮໍໂມນຂອງມະນຸດ, ສະນັ້ນມັນຍັງຖືກ ນຳ ໃຊ້ໃນການປະຕິບັດ ຢາດັ່ງກ່າວຖືກຍອມຮັບໂດຍຄົນເຈັບດີຂື້ນກວ່າເກົ່າແລະການປະຕິບັດບໍ່ກໍ່ໃຫ້ເກີດປະຕິກິລິຍາທາງລົບ, ພວກມັນບໍ່ຍັບຍັ້ງລະບົບພູມຕ້ານທານແລະຫຼຸດນໍ້າຕານໃນເລືອດໄດ້ຢ່າງມີປະສິດຕິຜົນ. Insulin Bovine ບໍ່ໄດ້ຖືກ ນຳ ໃຊ້ໃນຢາໃນມື້ນີ້, ເພາະວ່າເນື່ອງຈາກໂຄງສ້າງຕ່າງປະເທດມັນມີຜົນກະທົບທາງລົບຕໍ່ລະບົບພູມຕ້ານທານແລະລະບົບອື່ນໆຂອງຮ່າງກາຍຂອງມະນຸດ. ທາດ insulin ຂອງມະນຸດ, ເຊິ່ງໃຊ້ ສຳ ລັບຜູ້ປ່ວຍເບົາຫວານ, ໃນລະດັບອຸດສາຫະ ກຳ ແມ່ນໄດ້ຮັບໃນສອງທາງ: ເງື່ອນໄຂການເກັບຮັກສາສານອິນຊູລິນຕົວຊີ້ບອກແລະ contraindications
ການປະຕິບັດຢາຂອງຢາ
ຕົວຢ່າງຂອງຢາອິນຊູລິນທີ່ໄດ້ຮັບການອອກແບບຈາກມະນຸດ
ອິນຊູລິນຜະລິດຈາກຫຍັງ?

ການກະກຽມທີ່ໄດ້ມາຈາກວັດຖຸດິບຕົ້ນ ກຳ ເນີດຂອງສັດ
ອິນຊູລິນວິສະວະ ກຳ ພັນທຸ ກຳ
ດ້ວຍການປ່ຽນແປງທາງກາຍທາງເຄມີ - ທາດເຄມີ, ໂມເລກຸນຂອງອິນຊູລິນໃນອິນໂດເນເຊຍພິເສດກາຍເປັນທາດອິນຊູລິນ. ສ່ວນປະກອບຂອງກົດອະມິໂນຂອງການກະກຽມທີ່ອອກມາແມ່ນບໍ່ແຕກຕ່າງຈາກສ່ວນປະກອບຂອງຮໍໂມນ ທຳ ມະຊາດທີ່ຜະລິດຢູ່ໃນຮ່າງກາຍຂອງມະນຸດ.
ໃນລະຫວ່າງຂັ້ນຕອນການຜະລິດ, ຢາໄດ້ຜ່ານການເຮັດຄວາມບໍລິສຸດສູງ, ສະນັ້ນມັນບໍ່ກໍ່ໃຫ້ເກີດອາການແພ້ຫຼືການສະແດງທີ່ບໍ່ຕ້ອງການອື່ນໆ.
ແຕ່ສ່ວນຫຼາຍແລ້ວ, ອິນຊູລິນແມ່ນໄດ້ຮັບໂດຍໃຊ້ຈຸລິນຊີທີ່ຖືກປັບປຸງ (ດັດແປງພັນທຸ ກຳ). ການ ນຳ ໃຊ້ວິທີການທາງຊີວະວິທະຍາ, ເຊື້ອແບັກທີເຣັຍຫຼືເຊື້ອລາແມ່ນຖືກດັດແປງດ້ວຍວິທີທີ່ພວກເຂົາເອງສາມາດຜະລິດອິນຊູລິນ.
ນອກເຫນືອໄປຈາກການຜະລິດອິນຊູລິນຕົນເອງ, ການກັ່ນຕອງຂອງມັນມີບົດບາດ ສຳ ຄັນ. ເພື່ອວ່າຢາຈະບໍ່ເຮັດໃຫ້ເກີດອາການແພ້ແລະອັກເສບ, ແຕ່ລະໄລຍະມັນ ຈຳ ເປັນຕ້ອງໄດ້ຕິດຕາມກວດກາຄວາມບໍລິສຸດຂອງເຊື້ອຈຸລິນຊີແລະທຸກວິທີແກ້ໄຂ, ພ້ອມທັງສ່ວນປະກອບທີ່ ນຳ ໃຊ້.
ມີ 2 ວິທີການໃນການຜະລິດອິນຊູລິນ. ທຳ ອິດຂອງພວກມັນແມ່ນອີງໃສ່ການໃຊ້ສອງສາຍພັນທີ່ແຕກຕ່າງກັນ (ສາຍພັນ) ຂອງຈຸລິນຊີດຽວ.
ພວກມັນແຕ່ລະ synthesizes ພຽງແຕ່ລະບົບຕ່ອງໂສ້ຂອງໂມເລກຸນ DNA ຮໍໂມນ (ມີພຽງແຕ່ສອງຂອງມັນເທົ່ານັ້ນ, ແລະພວກມັນຖືກບິດຮ່ວມກັນ).
ຫຼັງຈາກນັ້ນ, ຕ່ອງໂສ້ເຫຼົ່ານີ້ແມ່ນເຊື່ອມຕໍ່ກັນ, ແລະໃນການແກ້ໄຂທີ່ໄດ້ຮັບແລ້ວມັນກໍ່ເປັນໄປໄດ້ທີ່ຈະແຍກຮູບແບບການເຄື່ອນໄຫວຂອງອິນຊູລິນອອກຈາກຕົວທີ່ບໍ່ມີຄວາມ ສຳ ຄັນທາງຊີວະພາບ.
ວິທີທີສອງທີ່ຈະໄດ້ຮັບຢາໂດຍໃຊ້ Escherichia coli ຫຼືເຊື້ອລາແມ່ນອີງໃສ່ຄວາມຈິງທີ່ວ່າຈຸລິນຊີ ທຳ ອິດຜະລິດອິນຊູລິນທີ່ບໍ່ມີປະສິດຕິຜົນ (ນັ້ນແມ່ນຕົວຢ່າງຂອງມັນແມ່ນ proinsulin). ຈາກນັ້ນ, ໂດຍ ນຳ ໃຊ້ວິທີການຮັກສາ enzymatic, ແບບຟອມນີ້ຖືກເປີດໃຊ້ແລະ ນຳ ໃຊ້ໃນທາງການແພດ.
ພະນັກງານຜູ້ທີ່ເຂົ້າເຖິງສະຖານທີ່ຜະລິດທີ່ແນ່ນອນຄວນນຸ່ງເຄື່ອງປ້ອງກັນທີ່ເປັນຫມັນ, ເຊິ່ງ ກຳ ຈັດການຕິດຕໍ່ຂອງຢາດ້ວຍທາດແຫຼວທາງຊີວະພາບຂອງມະນຸດ.
ຂະບວນການທັງ ໝົດ ນີ້ແມ່ນປົກກະຕິແລ້ວໂດຍອັດຕະໂນມັດ, ອາກາດແລະທຸກ ໜ້າ ທີ່ຕິດຕໍ່ກັບ ampoules ແລະ vials ແມ່ນບໍ່ເປັນຫມັນ, ແລະສາຍທີ່ມີອຸປະກອນຕ່າງໆແມ່ນຜະນຶກເຂົ້າກັນໂດຍ hermetically.
ວິທີການເຕັກໂນໂລຢີຊີວະພາບສາມາດຊ່ວຍໃຫ້ນັກວິທະຍາສາດຄິດກ່ຽວກັບວິທີແກ້ໄຂທາງເລືອກຂອງໂລກເບົາຫວານ.
ຍົກຕົວຢ່າງ, ມາຮອດປະຈຸບັນ, ການສຶກສາ preclinical ກ່ຽວກັບການຜະລິດຈຸລັງທົດລອງ pancreatic ປອມແມ່ນໄດ້ຖືກດໍາເນີນ, ເຊິ່ງສາມາດໄດ້ຮັບໂດຍໃຊ້ວິທີການວິສະວະກໍາພັນທຸກໍາ.
ບາງທີໃນອະນາຄົດພວກມັນຈະຖືກ ນຳ ໃຊ້ເພື່ອປັບປຸງການເຮັດວຽກຂອງອະໄວຍະວະນີ້ໃນຄົນເຈັບ.
ການຜະລິດການກະກຽມອິນຊູລິນທີ່ທັນສະ ໄໝ ແມ່ນຂະບວນການເຕັກໂນໂລຢີທີ່ສັບສົນທີ່ກ່ຽວຂ້ອງກັບການອັດຕະໂນມັດແລະການແຊກແຊງຂອງມະນຸດ ໜ້ອຍ ທີ່ສຸດ
ສ່ວນປະກອບເພີ່ມເຕີມ
ການຜະລິດອິນຊູລິນໂດຍບໍ່ມີຜູ້ຂັບໄລ່ໃນໂລກຍຸກ ໃໝ່ ເກືອບຈະເປັນໄປບໍ່ໄດ້ທີ່ຈະຈິນຕະນາການ, ເພາະວ່າພວກມັນສາມາດປັບປຸງຄຸນສົມບັດທາງເຄມີຂອງມັນ, ຂະຫຍາຍເວລາປະຕິບັດງານແລະບັນລຸຄວາມບໍລິສຸດໃນລະດັບສູງ.
ໂດຍຄຸນສົມບັດຂອງມັນ, ສ່ວນປະກອບເພີ່ມເຕີມທັງ ໝົດ ສາມາດແບ່ງອອກເປັນຊັ້ນຮຽນຕໍ່ໄປນີ້:
- ການຍືດເຍື້ອ (ສານທີ່ໃຊ້ເພື່ອໃຫ້ໄລຍະເວລາດົນກວ່າຂອງການກະ ທຳ ຂອງຢາ),
- ສ່ວນປະກອບທີ່ຂ້າເຊື້ອ
- ສະຖຽນລະພາບ, ເນື່ອງຈາກວ່າກົດທີ່ດີທີ່ສຸດແມ່ນຮັກສາໄວ້ໃນການແກ້ໄຂຢາ.
ການຍືດອາຍຸເພີ່ມ
ມີ insulins ທີ່ມີການເຄື່ອນໄຫວມາດົນນານເຊິ່ງກິດຈະ ກຳ ທາງຊີວະວິທະຍາຂອງລາວມີເວລາ 8 - 42 ຊົ່ວໂມງ (ຂຶ້ນກັບກຸ່ມຂອງຢາ). ຜົນກະທົບນີ້ແມ່ນບັນລຸໄດ້ເນື່ອງຈາກການເພີ່ມສານພິເສດ - ສານຍືດຍາວໃຫ້ກັບວິທີການສັກຢາ. ສ່ວນຫຼາຍມັກ, ໜຶ່ງ ໃນທາດປະສົມຕໍ່ໄປນີ້ແມ່ນໃຊ້ເພື່ອຈຸດປະສົງນີ້:
ທາດໂປຼຕີນທີ່ຍືດອາຍຸການປະຕິບັດຂອງຢາໄດ້ຮັບການ ຊຳ ລະລ້າງລາຍລະອຽດແລະມີສານແພ້ຕ່ ຳ (ຕົວຢ່າງທາດໂປຼຕີນ). ເກືອສັງກະສີຍັງບໍ່ສົ່ງຜົນກະທົບຕໍ່ກິດຈະ ກຳ ຂອງອິນຊູລິນຫຼືສະຫວັດດີການຂອງຄົນເຮົາ.
ຢາຂ້າເຊື້ອໂລກໃນສ່ວນປະກອບຂອງອິນຊູລິນແມ່ນມີຄວາມ ຈຳ ເປັນເພື່ອໃຫ້ພືດພັນຈຸລິນຊີບໍ່ຄູນໃນລະຫວ່າງການເກັບຮັກສາແລະ ນຳ ໃຊ້ໃນນັ້ນ. ສານເຫຼົ່ານີ້ແມ່ນສານກັນບູດແລະຮັບປະກັນການຮັກສາການເຄື່ອນໄຫວທາງຊີວະພາບຂອງຢາ.
ນອກຈາກນັ້ນ, ຖ້າຄົນເຈັບບໍລິຫານຮໍໂມນຈາກຫຼອດດຽວໃຫ້ຕົວເອງ, ຫຼັງຈາກນັ້ນຢາອາດຈະຢູ່ເປັນເວລາຫຼາຍມື້.
ເນື່ອງຈາກອົງປະກອບຕ້ານເຊື້ອແບັກທີເຣັຍທີ່ມີຄຸນນະພາບສູງ, ລາວຈະບໍ່ມີຄວາມຕ້ອງການທີ່ຈະຖິ້ມຢາທີ່ບໍ່ໄດ້ໃຊ້ເນື່ອງຈາກຄວາມເປັນໄປໄດ້ທາງທິດສະດີຂອງການສືບພັນໃນການແກ້ໄຂຂອງຈຸລິນຊີ.
ສານຕໍ່ໄປນີ້ສາມາດໃຊ້ເປັນຢາຂ້າເຊື້ອໂລກໃນການຜະລິດອິນຊູລິນ:
ຖ້າວິທີແກ້ໄຂບັນຈຸທາດໄອອອນສັງກະສີ, ພວກມັນກໍ່ເຮັດ ໜ້າ ທີ່ເປັນສານກັນບູດເພີ່ມເຕີມຍ້ອນຄຸນສົມບັດຂອງຢາຕ້ານເຊື້ອ
ສຳ ລັບການຜະລິດອິນຊູລິນແຕ່ລະຊະນິດ, ສ່ວນປະກອບຢາຂ້າເຊື້ອບາງຊະນິດແມ່ນ ເໝາະ ສົມ. ການປະຕິ ສຳ ພັນຂອງພວກເຂົາກັບຮໍໂມນນັ້ນຕ້ອງໄດ້ຮັບການສືບສວນໃນຂັ້ນຕອນຂອງການທົດລອງ preclinical, ເພາະວ່າສານກັນບູດບໍ່ຕ້ອງລົບກວນກິດຈະ ກຳ ທາງຊີວະພາບຂອງອິນຊູລິນຫຼືຖ້າບໍ່ດັ່ງນັ້ນຈະສົ່ງຜົນກະທົບທາງລົບຕໍ່ຄຸນລັກສະນະຂອງມັນ.
ການໃຊ້ສານກັນບູດໃນກໍລະນີຫຼາຍທີ່ສຸດເຮັດໃຫ້ຮໍໂມນສາມາດບໍລິຫານພາຍໃຕ້ຜິວ ໜັງ ໂດຍບໍ່ໄດ້ຮັບການຮັກສາກ່ອນດ້ວຍເຫຼົ້າຫຼືຢາຕ້ານເຊື້ອອື່ນໆ (ຜູ້ຜະລິດມັກຈະກ່າວເຖິງສິ່ງນີ້ຕາມ ຄຳ ແນະ ນຳ).
ນີ້ຈະເຮັດໃຫ້ການບໍລິຫານຢາງ່າຍຂື້ນແລະຫຼຸດຜ່ອນ ຈຳ ນວນເຄື່ອງມືກະກຽມກ່ອນການສີດເອງ.
ແຕ່ ຄຳ ແນະ ນຳ ນີ້ໃຊ້ໄດ້ຜົນເທົ່ານັ້ນຖ້າວິທີແກ້ໄຂໄດ້ຖືກຄຸ້ມຄອງໂດຍໃຊ້ເຂັມຂັດອິນຊູລິນໂດຍບຸກຄົນທີ່ມີເຂັມບາງໆ.
ສະຖຽນລະພາບ
ສະຖຽນລະພາບແມ່ນມີຄວາມຈໍາເປັນເພື່ອໃຫ້ pH ຂອງການແກ້ໄຂຖືກຮັກສາໄວ້ໃນລະດັບໃດຫນຶ່ງ. ການຮັກສາຢາ, ກິດຈະ ກຳ ແລະຄວາມ ໝັ້ນ ຄົງຂອງຄຸນສົມບັດທາງເຄມີແມ່ນຂື້ນກັບລະດັບຂອງກົດ. ໃນການຜະລິດຮໍໂມນສີດ ສຳ ລັບຄົນເຈັບທີ່ເປັນໂລກເບົາຫວານ, ຟອສເຟດແມ່ນຖືກ ນຳ ໃຊ້ເພື່ອຈຸດປະສົງນີ້.
ສຳ ລັບອິນຊູລິນກັບສັງກະສີ, ເຄື່ອງແກ້ໄຂສະຖຽນລະພາບແມ່ນບໍ່ ຈຳ ເປັນສະ ເໝີ ໄປ, ເພາະວ່າທາດໂລຫະຊ່ວຍຮັກສາຄວາມສົມດຸນທີ່ ຈຳ ເປັນ.
ຖ້າຫາກວ່າພວກມັນຖືກ ນຳ ໃຊ້ຢ່າງໃດກໍ່ຕາມ, ຫຼັງຈາກນັ້ນສານປະສົມເຄມີອື່ນໆກໍ່ຖືກ ນຳ ໃຊ້ແທນຟອສເຟດ, ເພາະວ່າການປະສົມສານເຫຼົ່ານີ້ ນຳ ໄປສູ່ການຂາດສະຕິແລະບໍ່ ເໝາະ ສົມກັບຢາ.
ຊັບສົມບັດທີ່ ສຳ ຄັນທີ່ສະແດງໃຫ້ເຫັນເຖິງສະຖຽນລະພາບທັງ ໝົດ ແມ່ນຄວາມປອດໄພແລະຄວາມບໍ່ສາມາດທີ່ຈະປະຕິກິລິຍາໃດໆກັບອິນຊູລິນ.
ຜູ້ຊ່ຽວຊານດ້ານ endocrinologist ທີ່ມີຄຸນນະພາບຄວນຈັດການກັບການເລືອກເອົາຢາສັກ ສຳ ລັບຄົນເຈັບແຕ່ລະຄົນ.
ວຽກງານຂອງອິນຊູລິນບໍ່ພຽງແຕ່ຮັກສາລະດັບນ້ ຳ ຕານໃນເລືອດປົກກະຕິເທົ່ານັ້ນ, ແຕ່ຍັງບໍ່ເປັນອັນຕະລາຍຕໍ່ອະໄວຍະວະອື່ນໆແລະລະບົບຕ່າງໆອີກດ້ວຍ. ຢາດັ່ງກ່າວຄວນຈະມີຄວາມເປັນກາງທາງເຄມີ, ມີສານແພ້ຕ່ ຳ ແລະ ເໝາະ ສົມ.
ມັນຍັງສະດວກດີຖ້າວ່າອິນຊູລິນທີ່ຖືກເລືອກສາມາດປະສົມກັບລຸ້ນອື່ນໆຕາມໄລຍະເວລາຂອງການປະຕິບັດ.
ການໄດ້ຮັບສານອິນຊູລິນ, ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ, ເຕັກໂນໂລຊີຊີວະພາບ - ວຽກວິຊາ

1. ໂຄງສ້າງແລະ ໜ້າ ທີ່ຂອງອິນຊູລິນ 5
1.1. ໂຄງສ້າງຂອງໂມເລກຸນອິນຊູລິນ 5
1.2. ຄວາມ ສຳ ຄັນທາງຊີວະພາບຂອງອິນຊູລິນ 7
1.3. ການຍັບຍັ້ງການວິເຄາະທາງອິນຊີ 8
2. ການສັງເຄາະອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ 10
2.1. ການໃຊ້ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ ສຳ ລັບການສັງເຄາະຢາ 10
2.2. ວິທີການວິສະວະ ກຳ ພັນທຸ ກຳ 11
2.3. ການຜະລິດອິນຊູລິນວິສະວະ ກຳ ທາງພັນທຸ ກຳ 14