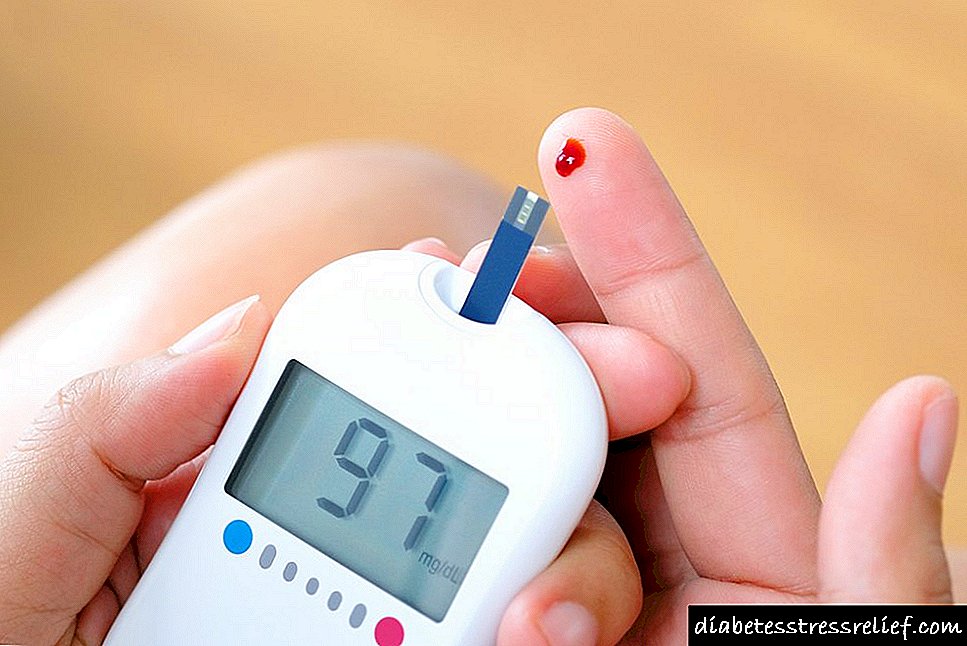
Telmisartan (Mikardis)
ລາຍລະອຽດກ່ຽວຂ້ອງກັບ 04.11.2016
- ຄຳ ນາມ: Telmisartan
- ລະຫັດ ATX: C09CA07
- ສານທີ່ໃຊ້ໄດ້: Telmisartan (Telmisartan)
- ຜູ້ຜະລິດ: ໂຮງງານຜະລິດຢາ TEVA, JSC ສຳ ລັບ Ratiopharm International GmbH, ຮົງກາລີ / ເຢຍລະມັນ
ອີງຕາມຮູບແບບຂອງການປ່ອຍ, ໜຶ່ງ ເມັດມີ 80 ຫຼື 40 ມລກຂອງສານທີ່ໃຊ້ໄດ້.
ແພດການຢາ
Telmisartan ແມ່ນຕົວຕ້ານທານ angiotensin II receptor. ມັນແຂ່ງຂັນກັບ angiotensin ເພື່ອຜູກກັບ receptors AT1. ບໍ່ມີຄວາມ ໜ້າ ເຊື່ອຖື ສຳ ລັບເຄື່ອງຮັບອື່ນໆແມ່ນຖືກຍົກໃຫ້ເຫັນ.
Telmisartan ບໍ່ສະກັດກັ້ນການກະ ທຳ ຂອງ renin, ACE, ບໍ່ກີດຂວາງຊ່ອງທາງທີ່ຮັບຜິດຊອບໃນການ ດຳ ເນີນງານ ions, ຫຼຸດຜ່ອນເນື້ອຫາ aldosterone ໃນ ເລືອດ.
ປະລິມານຂອງ 80 ມລກເກືອບຈະລົບລ້າງການເພີ່ມຂື້ນດັ່ງກ່າວ ຄວາມດັນເລືອດເກີດມາຈາກ angiotensin II. ຜົນສູງສຸດຈະແກ່ຍາວເຖິງ 24 ຊົ່ວໂມງ, ຈາກນັ້ນກໍ່ຄ່ອຍໆຫຼຸດລົງ. ໃນກໍລະນີນີ້, ຜົນກະທົບທີ່ ສຳ ຄັນຂອງຢາຈະຮູ້ສຶກໄດ້ຢ່າງ ໜ້ອຍ 48 ຊົ່ວໂມງຫລັງຈາກກິນຢາ.
Telmisartan ຫຼຸດຜ່ອນທັງຄວາມກົດດັນຂອງ systolic ແລະ diastolic, ແຕ່ບໍ່ມີຜົນຕໍ່ອັດຕາການເຕັ້ນຂອງເສັ້ນເລືອດ. ບໍ່ມີຜົນກະທົບຂອງສິ່ງເສບຕິດຫລືການສະສົມທີ່ ສຳ ຄັນທາງຄລີນິກໃນຮ່າງກາຍ.
ແພດການຢາ
ຫຼັງຈາກກິນ, ຢາກໍ່ໄດ້ດີແລະດູດຊືມໄວ. Bioavailability ແມ່ນປະມານ 50%. ມັນຜູກພັນໄດ້ດີກັບໂປຕີນ plasma.
ຄວາມເຂັ້ມຂຸ້ນຂອງ plasma ສູງສຸດແມ່ນສູງກວ່າປົກກະຕິໃນແມ່ຍິງເມື່ອກິນຄັ້ງດຽວກັນ. ແຕ່ນີ້ບໍ່ໄດ້ສົ່ງຜົນກະທົບຕໍ່ປະສິດທິຜົນ.
ການເຜົາຜານອາຫານ ເກີດຂື້ນໃນຕັບ. ນີ້ປະກອບເປັນການເຄື່ອນໄຫວ ທາດແປ້ງການ ກຳ ຈັດສິ່ງທີ່ເກີດຂື້ນສ່ວນໃຫຍ່ແມ່ນຜ່ານ ລຳ ໄສ້. ເຄິ່ງຊີວິດຂອງຮ່າງກາຍແມ່ນປະມານ 20 ຊົ່ວໂມງ.
ຕົວຊີ້ບອກ ສຳ ລັບການ ນຳ ໃຊ້
ມັນຖືກນໍາໃຊ້ເພື່ອປິ່ນປົວ hypertension ເສັ້ນເລືອດແດງ ແລະ ສຳ ລັບການປ້ອງກັນການຕາຍຂອງໂລກຈາກລະບົບຫລອດເລືອດຫົວໃຈ ເສັ້ນເລືອດຕັນໃນ, ຫົວໃຈວາຍພະຍາດຂອງເຮືອຂ້າງຄຽງ, hypertrophy ventricular ຊ້າຍ.
Contraindications
ມັນຖືກຫ້າມບໍ່ໃຫ້ສັ່ງຢາ Telmisartan ກັບ:
- ພະຍາດຕິດຕໍ່ຂອງກະເພາະ ລຳ ໃສ້,
- ຮ້າຍແຮງ ຄວາມລົ້ມເຫຼວຂອງຕັບ,
- ປະຖົມ aldosteronism,
- fructose intolerance,
- ຄວາມອ່ອນໄຫວຫຼາຍເກີນໄປກັບສານທີ່ໃຊ້ໄດ້ຫຼືສ່ວນປະກອບອື່ນໆທີ່ເປັນສ່ວນ ໜຶ່ງ ຂອງຢາ,
- ການຖືພາ,
- ອາຍຸຕ່ ຳ ກວ່າ 18 ປີ.
ຜົນຂ້າງຄຽງ
ຜົນຂ້າງຄຽງແມ່ນຫາຍາກ.
ໜຶ່ງ ໃນ 100-1000 ຄົນເຈັບທີ່ກິນຢາມີອາການດັ່ງຕໍ່ໄປນີ້:
ໃນ 1 ຂອງ 1000-10000 ຄົນເຈັບໄດ້ສັງເກດເຫັນ:
- ການຕິດເຊື້ອທາງເດີນປັດສະວະແລະລະບົບຫາຍໃຈ (cystitis, pharyngitis, sinusitis) ຫຼື sepsis,
- thrombocytopenia,
- ການຫຼຸດຜ່ອນລະດັບ hemoglobin,
- ຄວາມຮູ້ສຶກກັງວົນໃຈ
- ຄວາມລົບກວນດ້ານສາຍຕາ
- tachycardia,
- ຫຼຸດລົງໃນຄວາມດັນເລືອດໃນເວລາທີ່ການປ່ຽນແປງຕໍາແຫນ່ງຂອງຮ່າງກາຍ (ຈາກອອກຕາມລວງນອນກັບຕັ້ງ),
- ກະເພາະອາຫານ
- ປາກແຫ້ງ
- ການເຮັດວຽກຂອງຕັບທີ່ພິການ,
- ກິດຈະ ກຳ ຕັບເພີ່ມຂື້ນ enzymes,
- ຄວາມເຂັ້ມຂົ້ນຂອງ plasma ເພີ່ມຂື້ນຂອງອາຊິດ uric,
- ອາການເຈັບປວດຮ່ວມກັນ
- erythema,
- ໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກ,
- ຜື່ນເປັນພິດ
- ຜື່ນ eczematous.
ຜົນຂ້າງຄຽງທີ່ຫາຍາກຫຼາຍຫຼືຄວາມຖີ່ຂອງການບໍ່ສາມາດ ກຳ ນົດໄດ້ຢ່າງແນ່ນອນ:
- tendon ອາການເຈັບປວດຄ້າຍຄືກັນກັບ tendonitis,
- ລະດັບເພີ່ມຂື້ນຂອງ eosinophils ໃນເລືອດ.
ການໂຕ້ຕອບ
ການໂຕ້ຕອບຂອງ Telmisartan ກັບຢາອື່ນໆ:
- Baclofen, Amifostine ແລະຕົວແທນຕ້ານໂຣກເບົາຫວານອື່ນໆ - ຜົນກະທົບທີ່ສົມເຫດສົມຜົນໄດ້ຖືກປັບປຸງ,
- barbiturates, ຢາເສບຕິດ narcotic, ethanol ແລະ antidepressants - ການສະແດງຂອງ hypotension orthostatic ແມ່ນຮ້າຍແຮງກວ່າເກົ່າຫຼືຄວາມສ່ຽງຂອງການປະກົດຕົວຂອງມັນເພີ່ມຂື້ນ,
- Furosemide, Hydrochlorothiazide ແລະບາງຢາປິ່ນປົວພະຍາດອື່ນໆ - ຜົນກະທົບຕໍ່ hypotensive ເພີ່ມຂື້ນ,
- Digoxin - ຄວາມເຂັ້ມຂົ້ນເພີ່ມຂື້ນ Digoxin ໃນ plasma
- ການກຽມຕົວ lithium - ການເພີ່ມຂື້ນ ໃໝ່ ໃນຄວາມເຂັ້ມຂົ້ນຂອງ lithium ໃນເລືອດ, ການຕິດຕາມຕົວຊີ້ວັດນີ້ແມ່ນມີຄວາມ ຈຳ ເປັນ,
- NSAIDs - ຄວາມສ່ຽງຂອງອາການສ້ວຍແຫຼມເພີ່ມຂື້ນ ຄວາມລົ້ມເຫຼວຂອງ renalໂດຍສະເພາະກັບການຂາດນໍ້າ
- ໂພແທດຊຽມທີ່ເຮັດດ້ວຍໂພແທສຊຽມ, ໂພແທດຊຽມ, Heparin, Cyclosporin, ທາຄາເລີໂມມິ, Trimethoprim - ການເພີ່ມຄວາມເຂັ້ມຂົ້ນຂອງໂພແທດຊຽມໃນເຊລັ່ມເລືອດ,
- GCS - ຜົນກະທົບຕໍ່ hypotensive ຖືກຫຼຸດລົງ,
- Amlodipine - ປະສິດທິຜົນຂອງ Telmisartan ແມ່ນເພີ່ມຂື້ນ.
ການປະຕິບັດດ້ານການຢາ
ສັດຕູພືດຕ້ານໂຣກ Angiotensin II.
Telmisartan ແມ່ນຕົວຕ້ານທານສະເພາະຂອງ receptors angiotensin II. ມັນມີຄວາມເປັນເອກະພາບສູງ ສຳ ລັບປະເພດ AT1 receptor ຍ່ອຍຂອງ angiotensin II, ໂດຍຜ່ານການປະຕິບັດຂອງ angiotensin II ໄດ້ຖືກຮັບຮູ້. Telmisartan ເຄື່ອນຍ້າຍ angiotensin II ຈາກການຜູກມັດຂອງມັນກັບເຄື່ອງຮັບ, ຂາດການກະທໍາຂອງ agonist ທີ່ກ່ຽວຂ້ອງກັບ receptor ນີ້. Telmisartan ພຽງແຕ່ຜູກກັບ AT1 receptor ຍ່ອຍຂອງ angiotensin II. ການຜູກມັດແມ່ນຕໍ່ເນື່ອງ. Telmisartan ບໍ່ມີຄວາມ ສຳ ພັນກັບຜູ້ຮັບອື່ນ (ລວມທັງ AT2 receptors) ແລະ receptors angiotensin ທີ່ບໍ່ໄດ້ຮັບການສຶກສາ. ຄວາມ ສຳ ຄັນທີ່ເປັນປະໂຫຍດຂອງເຄື່ອງຮັບເຫຼົ່ານີ້, ພ້ອມທັງຜົນກະທົບຂອງການກະຕຸ້ນທີ່ເປັນໄປໄດ້ຫຼາຍເກີນໄປຂອງພວກມັນດ້ວຍໂຣກ angiotensin II, ຄວາມເຂັ້ມຂົ້ນຂອງມັນເພີ່ມຂື້ນກັບການແຕ່ງຕັ້ງ telmisartan, ບໍ່ໄດ້ຖືກສຶກສາ. ມັນຊ່ວຍຫຼຸດຜ່ອນຄວາມເຂັ້ມຂົ້ນຂອງ aldosterone ໃນເລືອດ, ບໍ່ຍັບຍັ້ງການ renin ໃນ plasma ໃນເລືອດແລະບໍ່ກີດຂວາງຊ່ອງທາງ ion, ບໍ່ຍັບຍັ້ງ ACE (kininase II, ເຊິ່ງເປັນ enzyme ທີ່ ທຳ ລາຍ bradykinin). ເພາະສະນັ້ນ, ການເພີ່ມຂື້ນຂອງຜົນຂ້າງຄຽງທີ່ເກີດຈາກ bradykinin ບໍ່ໄດ້ຄາດຫວັງ.
Telmisartan ໃນປະລິມານ 80 ມລກຈະເຮັດໃຫ້ຜົນກະທົບ hypertensive ຂອງ angiotensin II ສູງສົມບູນ. ການເລີ່ມຕົ້ນຂອງການປະຕິບັດ hypotensive ແມ່ນສັງເກດເຫັນພາຍໃນ 3 ຊົ່ວໂມງຫຼັງຈາກການບໍລິຫານຄັ້ງທໍາອິດຂອງ telmisartan. ຜົນກະທົບຂອງຢາຈະແກ່ຍາວເຖິງ 24 ຊົ່ວໂມງແລະຍັງມີຄວາມ ສຳ ຄັນສູງເຖິງ 48 ຊົ່ວໂມງຜົນກະທົບທີ່ ໜ້າ ປະທັບໃຈທີ່ອອກສຽງມັກຈະພັດທະນາ 4-8 ອາທິດຫລັງຈາກໄດ້ຮັບເຂົ້າເປັນປະ ຈຳ.
ໃນຜູ້ປ່ວຍທີ່ເປັນໂລກຄວາມດັນໂລຫິດແດງ, telmisartan ຫຼຸດຜ່ອນຄວາມດັນເລືອດ systolic ແລະ diastolic, ໂດຍບໍ່ມີຜົນກະທົບຕໍ່ອັດຕາການເຕັ້ນຂອງຫົວໃຈ.
ໃນກໍລະນີຂອງການຍົກເລີກ telmisartan ຢ່າງກະທັນຫັນ, ຄວາມດັນເລືອດຈະຄ່ອຍໆກັບມາຢູ່ໃນລະດັບເດີມໂດຍບໍ່ມີການພັດທະນາຂອງໂຣກຖອນ.
ປະລິມານຢາແລະການບໍລິຫານ
ຢາດັ່ງກ່າວແມ່ນຖືກ ກຳ ນົດທາງປາກ, ບໍ່ວ່າຈະເປັນການກິນອາຫານ.
ດ້ວຍຄວາມດັນໂລຫິດແດງ, ປະລິມານທີ່ແນະ ນຳ ໃນເບື້ອງຕົ້ນຂອງຢາແມ່ນ 1 ເມັດ (40 ມລກ) ມື້ລະຄັ້ງ. ໃນກໍລະນີທີ່ຜົນການປິ່ນປົວບໍ່ໄດ້ຮັບຜົນ, ປະລິມານຢາແມ່ນສູງເຖິງ 80 ມລກມື້ລະເທື່ອ. ໃນເວລາທີ່ຕັດສິນໃຈວ່າຈະເພີ່ມປະລິມານຢາ, ມັນຄວນຈະຖືກພິຈາລະນາວ່າຜົນກະທົບຕໍ່ຕ້ານໂຣກຕັບສູງສຸດແມ່ນມັກຈະບັນລຸໄດ້ພາຍໃນ 4-8 ອາທິດຫຼັງຈາກການເລີ່ມຕົ້ນການປິ່ນປົວ.
ເພື່ອຫຼຸດຜ່ອນການເປັນພະຍາດຫຼອດເລືອດຫົວໃຈແລະອັດຕາການຕາຍ, ປະລິມານທີ່ແນະ ນຳ ແມ່ນ 1 ເມັດ (80 ມລກ) 1 ເທື່ອຕໍ່ມື້. ໃນໄລຍະເລີ່ມຕົ້ນຂອງການປິ່ນປົວ, ຕ້ອງມີການແກ້ໄຂຄວາມດັນເລືອດເພີ່ມ.
ຜູ້ປ່ວຍທີ່ເປັນໂຣກຫົວໃຈຊຸດໂຊມ (ລວມທັງຜູ້ທີ່ເປັນໂຣກຕັບອັກເສບ), ຄົນເຈັບຜູ້ສູງອາຍຸ, ການປັບປະລິມານຢາແມ່ນບໍ່ ຈຳ ເປັນ.
ໃນຄົນເຈັບທີ່ມີພາວະຕັບອ່ອນເພຍອ່ອນໆແລະປານກາງ (ຊັ້ນ A ແລະ B ໃນລະດັບ Child-Pugh), ປະລິມານປະ ຈຳ ວັນບໍ່ຄວນເກີນ 40 ມກ.
ຜົນຂ້າງຄຽງ
ກໍລະນີທີ່ສັງເກດຈາກຜົນຂ້າງຄຽງບໍ່ກ່ຽວຂ້ອງກັບເພດ, ອາຍຸຫຼືເຊື້ອຊາດຂອງຄົນເຈັບ.
ການຕິດເຊື້ອ: ໂຣກ sepsis, ລວມທັງໂຣກ sepsis ທີ່ເປັນອັນຕະລາຍ, ການຕິດເຊື້ອທາງເດີນປັດສະວະ (ລວມທັງ cystitis), ການຕິດເຊື້ອທາງເດີນຫາຍໃຈເທິງ.
ຈາກລະບົບ hemopoietic: ການຫຼຸດລົງຂອງ hemoglobin, ພະຍາດເລືອດຈາງ, eosinophilia, thrombocytopenia.
ຈາກຂ້າງຂອງລະບົບປະສາດສ່ວນກາງ: ນອນບໍ່ຫຼັບ, ກັງວົນໃຈ, ຊຶມເສົ້າ, ວິນຫົວ.
ຈາກລະບົບຫຼອດເລືອດຫົວໃຈ: ໝາຍ ເຖິງການຫຼຸດລົງຂອງຄວາມດັນເລືອດ (ລວມທັງໂຣກ hypotension orthostatic), bradycardia, tachycardia, fainting.
ຈາກລະບົບຫາຍໃຈ: ຫາຍໃຈສັ້ນ.
ຈາກລະບົບກ່ຽວກັບເຄື່ອງຍ່ອຍ: ປາກແຫ້ງ, ກະເພາະອາຫານ, ບໍ່ສະບາຍໃນກະເພາະອາຫານ, ຮາກ, ທ້ອງບິດ, ຖອກທ້ອງ, ເຈັບທ້ອງ, ເຮັດໃຫ້ຕັບອ່ອນເພຍ, ກິດຈະ ກຳ ທີ່ເພີ່ມຂື້ນຂອງການປ່ຽນຖ່າຍຕັບອັກເສບ.
ຈາກລະບົບທາງເດີນປັດສະວະ: ການເຮັດວຽກຂອງ ໝາກ ໄຂ່ຫຼັງທີ່ເສີຍຫາຍ (ລວມທັງຄວາມຜິດປົກກະຕິຂອງ ໝາກ ໄຂ່ຫຼັງທີ່ເປັນໂຣກສ້ວຍແຫຼມ), ພະຍາດເສັ້ນປະສາດຂ້າງນອກ, hypercreatininemia.
ຈາກລະບົບ musculoskeletal: arthralgia, ເຈັບຫລັງ, spasms ກ້າມເນື້ອ (ປວດກ້າມເນື້ອຂອງ calf), ຄວາມເຈັບປວດໃນສ່ວນຕ່ ຳ, myalgia, ເຈັບໃນ tendons (ອາການຄ້າຍຄືກັບການສະແດງອອກຂອງ tendonitis), ເຈັບທ້ອງ.
ຕິກິລິຍາອາການແພ້: ຕິກິລິຍາ anaphylactic ຕິກິລິຢາ hypersensitivity ກັບສານເສບຕິດການເຄື່ອນໄຫວຫຼືອົງປະກອບອົງການຊ່ອຍເຫລືອຂອງການກະກຽມ, angioedema, eczema, erythema, pruritus ຜື່ນ (ລວມທັງຂະຫນາດ), urticaria, eruption ພິດ.
ຕົວຊີ້ວັດໃນຫ້ອງທົດລອງ: hyperuricemia, ລະດັບເພີ່ມຂຶ້ນຂອງເລືອດ CPK, hyperkalemia.
ອື່ນໆ: hyperhidrosis, ໂຣກຄ້າຍຄືກັບໄຂ້ຫວັດໃຫຍ່, ຄວາມບົກຜ່ອງດ້ານສາຍຕາ, ໂຣກປະສາດຕາ (ອ່ອນເພຍ).
ການໃຊ້ຢາMIKARDIS®ໃນລະຫວ່າງການຖືພາແລະການດູດນົມ
Mikardis®ແມ່ນ contraindicated ໃນການຖືພາແລະ lactation.
ດ້ວຍການຖືພາທີ່ວາງແຜນໄວ້, Mikardis®ຄວນໄດ້ຮັບການທົດແທນດ້ວຍຢາຕ້ານໂຣກຮໍໂມນອື່ນໆ. ເມື່ອການຖືພາຖືກສ້າງຕັ້ງຂຶ້ນ, Mikardis ຄວນໄດ້ຮັບການຢຸດເຊົາໃນໄວທີ່ສຸດ.
ໃນການສຶກສາ preclinical, ບໍ່ມີຜົນກະທົບ teratogenic ຂອງຢາ, ແຕ່ຜົນກະທົບຂອງ fetotoxic ໄດ້ຖືກສັງເກດເຫັນ.
ຄຳ ແນະ ນຳ ພິເສດ
ໃນຜູ້ປ່ວຍບາງຄົນ, ຍ້ອນການສະກັດກັ້ນຂອງ RAAS, ໂດຍສະເພາະໃນເວລາທີ່ການໃຊ້ຢາປະສົມປະສານກັບລະບົບນີ້, ການເຮັດວຽກຂອງ ໝາກ ໄຂ່ຫຼັງ (ລວມທັງຄວາມຜິດປົກກະຕິຂອງ ໝາກ ໄຂ່ຫຼັງທີ່ເປັນໂຣກສ້ວຍແຫຼມ) ແມ່ນພິການ. ດັ່ງນັ້ນ, ການປິ່ນປົວທີ່ປະກອບດ້ວຍການປິດ RAAS ສອງຄັ້ງດັ່ງກ່າວຄວນໄດ້ຮັບການປະຕິບັດຢ່າງເຂັ້ມງວດເປັນສ່ວນບຸກຄົນແລະມີການຕິດຕາມກວດກາຢ່າງລະມັດລະວັງກ່ຽວກັບການເຮັດວຽກຂອງ ໝາກ ໄຂ່ຫຼັງ (ລວມທັງການຕິດຕາມກວດກາແຕ່ລະໄລຍະຂອງຄວາມເຂັ້ມຂຸ້ນຂອງ serum potassium ແລະຄວາມເຂັ້ມຂຸ້ນຂອງ creatinine).
ໃນກໍລະນີຂອງການເພິ່ງພາອາການໂຕນຂອງຫລອດເລືອດແລະການເຮັດວຽກຂອງ ໝາກ ໄຂ່ຫຼັງສ່ວນໃຫຍ່ແມ່ນກ່ຽວກັບກິດຈະ ກຳ RAAS (ຕົວຢ່າງ, ໃນຄົນເຈັບທີ່ເປັນໂຣກຫົວໃຈຊຸດໂຊມ, ຫຼືພະຍາດ ໝາກ ໄຂ່ຫຼັງ, ລວມທັງໂຣກເສັ້ນເລືອດແດງໃນເສັ້ນປະສາດຫຼືເສັ້ນເລືອດແດງຂອງ ໝາກ ໄຂ່ຫຼັງດຽວ), ການແຕ່ງຕັ້ງຢາທີ່ມີຜົນຕໍ່ລະບົບນີ້, ອາດຈະປະກອບດ້ວຍການພັດທະນາຂອງ hypotension ເສັ້ນເລືອດແດງສ້ວຍແຫຼມ, hyperazotemia, oliguria, ແລະ, ໃນກໍລະນີທີ່ຫາຍາກ, ຄວາມລົ້ມເຫຼວຂອງຫມາກໄຂ່ຫຼັງສ້ວຍແຫຼມ.
ອີງຕາມປະສົບການຂອງການໃຊ້ຢາຊະນິດອື່ນທີ່ສົ່ງຜົນຕໍ່ RAAS, ໂດຍການໃຊ້ຮ່ວມກັນຂອງMikardis®ແລະຢາ diuretics ທີ່ມີໂພແທດຊຽມ, ການເພີ່ມທາດໂປຕາຊຽມ, ເກືອທີ່ມີສານໂພແທດຊຽມ, ແລະຢາອື່ນໆທີ່ຊ່ວຍເພີ່ມຄວາມເຂັ້ມຂົ້ນຂອງໂປຕີນໃນເລືອດ (ຕົວຢ່າງ, heparin), ຕົວຊີ້ວັດນີ້ຄວນໄດ້ຮັບການຕິດຕາມກວດກາໃນຄົນເຈັບ.
ອີກທາງເລືອກ ໜຶ່ງ, Mikardis®ສາມາດໃຊ້ຮ່ວມກັບ thiazide diuretics, ເຊັ່ນ hydrochlorothiazide, ນອກຈາກນັ້ນຍັງມີຜົນກະທົບທີ່ ໜ້າ ຫຼົງໄຫຼ (ຕົວຢ່າງ: MikardisPlus® 40 mg / 12.5 mg, 80 mg / 12.5 mg).
ໃນຜູ້ປ່ວຍທີ່ເປັນໂລກຄວາມດັນໂລຫິດແດງຢ່າງຮຸນແຮງ, ປະລິມານຂອງ telmisartan 160 ມລກຕໍ່ມື້ໃນການປະສົມກັບ hydrochlorothiazide 12,5-25 ມລກແມ່ນມີຄວາມທົນທານແລະມີປະສິດຕິຜົນ.
Mikardis®ແມ່ນປະສິດຕິຜົນຫນ້ອຍໃນຜູ້ປ່ວຍຂອງເຊື້ອຊາດ Negroid.
ປ່ອຍແບບຟອມແລະສ່ວນປະກອບ
ຮູບແບບປະລິມານຢາ - ຊະນິດເມັດ: ຮອບ, ຮູບຊົງກະບອກ, ມີກະດາດຊາຍແລະດອກໄມ້, ສີຂາວຫຼືສີຂາວ - ສີເຫຼືອງ (5, 7, 10 ແລະ 20 ເມັດ) ໃນຊອງເປັນແຜ່ນ, ໃນມັດກະດາດຊາຍ 1, 2, 3, 4, 5, 8 ຫຼື 10 ຊອງ, 10, 20, 28, 30, 40, 50, ແລະ 100 ຊິ້ນແຕ່ລະອັນ, ໃນກະປcອງທີ່ເຮັດດ້ວຍຝາອັດດ້ວຍການຄວບຄຸມທີ່ມີຝາຄວບຄຸມຫຼືໃຊ້ຝາອັດດ້ວຍ screw-on ທີ່ມີລະບົບຍູ້ຫລືມີການຄວບຄຸມ tamper ຄັ້ງ ທຳ ອິດ, ໃນກ່ອງ cardboard 1 ແຕ່ລະຊອງຍັງມີ ຄຳ ແນະ ນຳ ສຳ ລັບການ ນຳ ໃຊ້ Telmisartan).
ສ່ວນປະກອບຂອງ 1 ເມັດ:
- ສ່ວນປະກອບທີ່ເຄື່ອນໄຫວ: telmisartan - 40 ຫຼື 80 ມລກ,
- excipients (ເມັດ 40/80 mg): croscarmellose sodium - 12/24 mg, sodium hydroxide - 3.35 / 6.7 mg, povidone-K25 - 12/24 mg, lactose monohydrate (ນ້ ຳ ຕານນົມ) - 296.85 / 474,9 mg, stearate ແມກນີຊຽມ - 3.80 / 6.4 ມກ, meglumine - 12/24 ມກ.
ໂລກຄວາມດັນເລືອດສູງ
ການໃຊ້ telmisartan ໃນປະລິມານ 80 ມລກສະກັດກັ້ນຜົນກະທົບ hypertensive ຂອງ AT II. ຜົນກະທົບຂອງການຕ້ານການອັກເສບຈະພັດທະນາພາຍໃນປະມານ 3 ຊົ່ວໂມງຫຼັງຈາກປະລິມານຄັ້ງ ທຳ ອິດ, ແກ່ຍາວເຖິງ 24 ຊົ່ວໂມງແລະຍັງມີຄວາມ ສຳ ຄັນຈົນເຖິງ 48 ຊົ່ວໂມງ.
ໃນໂລກຄວາມດັນໂລຫິດແດງ, telmisartan ຫຼຸດລົງຄວາມດັນເລືອດ systolic ແລະ diastolic (BP) ໂດຍບໍ່ມີຜົນກະທົບຕໍ່ອັດຕາການເຕັ້ນຂອງຫົວໃຈ (HR).
ຫຼັງຈາກການຢຸດຢາຢ່າງຮຸນແຮງ, ລະດັບຄວາມດັນເລືອດຈະກັບຄືນສູ່ມູນຄ່າເດີມຂອງມັນເປັນເວລາຫລາຍມື້. ໂຣກຖອນເງິນບໍ່ພັດທະນາ.
ອີງຕາມການສຶກສາທາງດ້ານການຊ່ວຍປຽບທຽບ, ຜົນກະທົບທີ່ສົມເຫດສົມຜົນຂອງ telmisartan ແມ່ນປຽບທຽບກັບຢາຂອງຫ້ອງຮຽນອື່ນໆ (ຕົວຢ່າງ, atenolol, hydrochlorothiazide, enalapril, lisinopril, amlodipine). ເຖິງຢ່າງໃດກໍ່ຕາມ, ອາການໄອແຫ້ງໃນຄົນເຈັບທີ່ໄດ້ຮັບ telmisartan ແມ່ນເກີດຂື້ນເລື້ອຍໆກ່ວາຄົນເຈັບທີ່ໃຊ້ຢາຍັບຍັ້ງ ACE.
ການປ້ອງກັນພະຍາດ cardiovascular
ໃນຜູ້ປ່ວຍທີ່ມີອາຍຸ 55 ປີຂຶ້ນໄປທີ່ມີການໂຈມຕີໂຣກ ischemic ຊົ່ວຄາວ, ເສັ້ນເລືອດຕັນໃນ, ພະຍາດເສັ້ນເລືອດໃນຕັບແຂງ (CHD), ໂຣກເສັ້ນເລືອດໃນຕຸ່ມແລະພະຍາດເບົາຫວານປະເພດ 2 (ເຊັ່ນໂຣກ hypertrophy ຊ້າຍ, micro- ຫຼື macroalbuminuria, ໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກໂຣກ. ກຸ່ມສ່ຽງຕໍ່ການເປັນໂຣກຫົວໃຈວາຍ, telmisartan ມີຜົນກະທົບຄ້າຍຄືກັບ ramipril ໃນການຫຼຸດຜ່ອນຈຸດຈົບປະສົມປະສານຂັ້ນຕົ້ນ: ການເຂົ້າໂຮງ ໝໍ ຍ້ອນໂຣກຫົວໃຈຊຸດໂຊມ ເສັ້ນເລືອດຕັນໃນ neostatal, infarction myocardial nonfatal, ອັດຕາການຕາຍຂອງຫົວໃຈ.
Telmisartan, ຄ້າຍຄືກັບ ramipril, ຍັງໄດ້ສະແດງໃຫ້ເຫັນວ່າມີປະສິດຕິຜົນໃນການຫຼຸດຜ່ອນຄວາມຖີ່ຂອງຈຸດທີສອງ: ເສັ້ນເລືອດຕັນໃນທີ່ບໍ່ແມ່ນຄວາມຕາຍ, ການອັກເສບ myocardial ທີ່ບໍ່ແມ່ນໄຂມັນ, ແລະອັດຕາການຕາຍຂອງຫົວໃຈ.
ປະສິດທິຜົນຂອງ telmisartan ໃນປະລິມານທີ່ຕໍ່າກວ່າ 80 ມລກເພື່ອຫຼຸດຜ່ອນຄວາມສ່ຽງຂອງການຕາຍຂອງເສັ້ນເລືອດຫົວໃຈຍັງບໍ່ທັນໄດ້ຖືກສຶກສາ.
ບໍ່ຄືກັບ ramipril, telmisartan ບໍ່ຄ່ອຍຈະມີຜົນຂ້າງຄຽງເຊັ່ນ: ໄອແຫ້ງແລະໂຣກຊືມເສົ້າ. ຢ່າງໃດກໍ່ຕາມ, ຕໍ່ກັບຄວາມເປັນມາຂອງການໄດ້ຮັບຂອງມັນ, ການຍັບຍັ້ງເສັ້ນເລືອດແດງມັກຈະເກີດຂື້ນເລື້ອຍໆ.
ແບບຟອມຢາ:
1 ເມັດມີ:
ຂະ ໜາດ 40 ມກ
ສານທີ່ຫ້າວຫັນ: telmisartan - 40 ມລກ
excipients: sodium hydroxide - 3.4 mg, povidone K 30 (ນ້ ຳ ໜັກ ໂມເລກຸນ polyvinylpyrrolidone) - 12.0 ມລກ, meglumine - 12.0 ມລກ, mannitol - 165,2 mg, stearate ແມກນີຊຽມ - 2,4 mg, talc - 5.0 ມລກ .
ຂະ ໜາດ ຂອງ 80 ມກ
ສານທີ່ຫ້າວຫັນ: telmisartan - 80 ມລກ
ຜູ້ຊ່ຽວຊານ: sodium hydroxide - 6.8 mg, povidone K 30 (ນ້ ຳ ໜັກ ໂມເລກຸນ polyvinylpyrrolidone) - 24.0 ມລກ, meglumine - 24.0 ມລກ, mannitol - 330,4 mg, stearate ແມກນີຊຽມ - 4,8 mg, talc - 10.0 ມລກ.
ແທັບເລັດມີສີຂາວຫລືສີຂາວເກືອບ, ເປັນຮູບກົມ, ມີຮູບຊົງກົມ, ເປັນຮູບກົມແລະເປັນຮູ.
ຄຸນສົມບັດທາງການຢາ
ແພດການຢາ
Telmisartan ແມ່ນຕົວຕ້ານທານ angiotensin II ທີ່ສະເພາະ (ປະເພດ AT1), ມີປະສິດຕິຜົນເມື່ອກິນທາງປາກ. ມັນມີຄວາມເປັນເອກະພາບສູງ ສຳ ລັບ subtype AT1 angiotensin II receptors ໂດຍຜ່ານການປະຕິບັດຂອງ angiotensin II ແມ່ນຖືກຮັບຮູ້. ສະແດງ angiotensin II ຈາກການເຊື່ອມຕໍ່ກັບຕົວຮັບ, ບໍ່ມີການກະ ທຳ ຂອງ agonist ທີ່ກ່ຽວຂ້ອງກັບຕົວຮັບນີ້.
Telmisartan ຜູກມັດພຽງແຕ່ກັບປະເພດ AT1 receptors angiotensin II. ການເຊື່ອມຕໍ່ແມ່ນຕໍ່ເນື່ອງ. ບໍ່ມີຄວາມ ໜ້າ ເຊື່ອຖື ສຳ ລັບຜູ້ຮັບອື່ນ, ລວມທັງພູມຕ້ານທານ2 receptor ແລະ receptors angiotensin ທີ່ໄດ້ສຶກສາຫນ້ອຍ. ຄວາມ ສຳ ຄັນທີ່ເປັນປະໂຫຍດຂອງເຄື່ອງຮັບເຫຼົ່ານີ້, ພ້ອມທັງຜົນກະທົບຂອງການກະຕຸ້ນທີ່ເປັນໄປໄດ້ຫຼາຍເກີນໄປກັບ angiotensin II, ຄວາມເຂັ້ມຂົ້ນຂອງມັນເພີ່ມຂື້ນກັບການແຕ່ງຕັ້ງ telmisartan, ບໍ່ໄດ້ຖືກສຶກສາ. ມັນຊ່ວຍຫຼຸດຜ່ອນຄວາມເຂັ້ມຂົ້ນຂອງ aldosterone ໃນເລືອດ, ບໍ່ຍັບຍັ້ງການ renin ໃນ plasma ໃນເລືອດແລະບໍ່ກີດຂວາງຊ່ອງທາງ ion.Telmisartan ບໍ່ຍັບຍັ້ງການໃຫ້ທາດ enzyme ທີ່ປ່ຽນເປັນທາດ angiotensin (kininase II) (ເປັນເອນໄຊທີ່ເຮັດໃຫ້ລະລາຍ bradykinin). ເພາະສະນັ້ນ, ການເພີ່ມຂື້ນຂອງຜົນຂ້າງຄຽງທີ່ເກີດຈາກ bradykinin ບໍ່ໄດ້ຄາດຫວັງ.
ໃນຜູ້ປ່ວຍ, telmisartan ໃນປະລິມານ 80 ມລກຈະເຮັດໃຫ້ຜົນກະທົບ hypertensive ຂອງ angiotensin II ສູງຂື້ນ. ການເລີ່ມຕົ້ນຂອງການປະຕິບັດການຕ້ານການອັກເສບແມ່ນສັງເກດພາຍໃນ 3 ຊົ່ວໂມງຫຼັງຈາກການບໍລິຫານຄັ້ງທໍາອິດຂອງ telmisartan. ຜົນກະທົບຂອງຢາຍັງຄົງຢູ່ຕະຫຼອດ 24 ຊົ່ວໂມງແລະຍັງມີຄວາມ ສຳ ຄັນເຖິງ 48 ຊົ່ວໂມງ. ຜົນກະທົບຕໍ່ຕ້ານຫລອດເລືອດສະແດງອອກຕາມປົກກະຕິຈະພັດທະນາ 4-8 ອາທິດຫຼັງຈາກການບໍລິຫານທາງປາກເປັນປະ ຈຳ.
ໃນຄົນເຈັບທີ່ເປັນໂລກຄວາມດັນໂລຫິດແດງ, telmisartan ຫຼຸດລົງຄວາມດັນເລືອດ systolic ແລະ diastolic (BP) ໂດຍບໍ່ມີຜົນກະທົບຕໍ່ອັດຕາການເຕັ້ນຂອງຫົວໃຈ (HR).
ໃນກໍລະນີຂອງການຍົກເລີກ telmisartan ຢ່າງກະທັນຫັນ, ຄວາມດັນເລືອດຈະຄ່ອຍໆກັບມາຢູ່ໃນລະດັບເດີມໂດຍບໍ່ມີການພັດທະນາຂອງໂຣກ "ຍົກເລີກ".
ແພດການຢາ
ເມື່ອກິນທາງປາກ, ມັນຈະຖືກດູດຊືມຈາກ ລຳ ໄສ້ໃຫຍ່. Bioavailability ແມ່ນ 50%. ເມື່ອກິນພ້ອມໆກັບອາຫານ, ການຫຼຸດລົງຂອງ AUC (ພື້ນທີ່ພາຍໃຕ້ເສັ້ນໂຄ້ງຂອງເວລາຄວາມເຂັ້ມຂົ້ນ) ແມ່ນຕັ້ງແຕ່ 6% (ໃນລະດັບປະລິມານ 40 ມກ) ຫາ 19% (ໃນປະລິມານ 160 ມກ). 3 ຊົ່ວໂມງຫລັງຈາກກິນ, ຄວາມເຂັ້ມຂົ້ນຂອງ plasma ໃນເລືອດແມ່ນລະດັບ, ບໍ່ວ່າຈະເປັນເວລາກິນເຂົ້າ. ມີຄວາມແຕກຕ່າງກັນໃນຄວາມເຂັ້ມຂົ້ນຂອງ plasma ໃນຜູ້ຊາຍແລະແມ່ຍິງ. ກັບສູງສຸດທີ່ເຄຍ(ຄວາມເຂັ້ມຂົ້ນສູງສຸດ) ແລະ AUC ແມ່ນປະມານ 3 ແລະ 2 ເທື່ອ, ຕາມ ລຳ ດັບ, ສູງກວ່າແມ່ຍິງທຽບກັບຜູ້ຊາຍໂດຍບໍ່ມີຜົນກະທົບທີ່ມີປະສິດຕິຜົນສູງ.
ການສື່ສານກັບໂປຼຕີນ plasma ໃນເລືອດ - 99,5%, ສ່ວນໃຫຍ່ແມ່ນມີທາດ albumin ແລະ alpha-1 glycoprotein. ມູນຄ່າສະເລ່ຍຂອງປະລິມານການແຈກຢາຍທີ່ຊັດເຈນໃນຄວາມເຂັ້ມຂົ້ນຂອງຄວາມສົມດຸນແມ່ນ 500 ລິດ. ມັນແມ່ນ metabolized ໂດຍ conjugation ກັບກົດ glucuronic. Metabolites ແມ່ນຢາທີ່ບໍ່ມີປະໂຫຍດ. ການລົບລ້າງເຄິ່ງຊີວິດແມ່ນຫຼາຍກ່ວາ 20 ຊົ່ວໂມງ. ມັນໄດ້ຖືກຖ່າຍອອກຜ່ານ ລຳ ໄສ້ທີ່ບໍ່ປ່ຽນແປງ, ເປັນ ໜິ້ວ ໂດຍ ໝາກ ໄຂ່ຫຼັງ - ໜ້ອຍ ກວ່າ 2% ຂອງປະລິມານທີ່ກິນ. ການ ຊຳ ລະລ້າງ plasma ທັງ ໝົດ ແມ່ນສູງ (900 ມລ / ນາທີ) ເມື່ອທຽບກັບກະແສເລືອດ "ຕັບອັກເສບ" (ປະມານ 1500 ມລ / ນາທີ).
ຢາ pharmacokinetics ຂອງ telmisartan ໃນຜູ້ປ່ວຍຜູ້ສູງອາຍຸບໍ່ແຕກຕ່າງຈາກຄົນເຈັບ ໜຸ່ມ. ການດັດປັບປະລິມານແມ່ນບໍ່ ຈຳ ເປັນ.
ຄົນເຈັບທີ່ເປັນໂຣກ ໝາກ ໄຂ່ຫລັງ
ການປ່ຽນແປງຂອງຄົນເຈັບທີ່ມີຄວາມຜິດປົກກະຕິຂອງ ໝາກ ໄຂ່ຫຼັງແມ່ນບໍ່ ຈຳ ເປັນ, ລວມທັງຄົນເຈັບທີ່ເປັນໂຣກຕັບອັກເສບ. Telmisartan ບໍ່ໄດ້ຖືກເອົາອອກໂດຍ hemodialysis.
ຄົນເຈັບທີ່ເປັນໂຣກຕັບ
ໃນຄົນເຈັບທີ່ມີພາວະຕັບອ່ອນເພຍອ່ອນໆແລະປານກາງ (ຊັ້ນ A ແລະ B ໃນລະດັບ Child-Pugh), ປະລິມານປະ ຈຳ ວັນບໍ່ຄວນເກີນ 40 ມກ.
ການໃຊ້ຢາເດັກ
ຕົວຊີ້ວັດຕົ້ນຕໍຂອງ pharmacokinetics ຂອງ telmisartan ໃນເດັກອາຍຸ 6 ຫາ 18 ປີຫຼັງຈາກກິນ telmisartan ໃນປະລິມານ 1 mg / kg ຫຼື 2 mg / kg ເປັນເວລາ 4 ອາທິດ, ໂດຍທົ່ວໄປແລ້ວແມ່ນສາມາດປຽບທຽບກັບຂໍ້ມູນທີ່ໄດ້ຮັບໃນການປິ່ນປົວຜູ້ໃຫຍ່, ແລະຢືນຢັນຄວາມບໍ່ສອດຄ່ອງຂອງ pharmacokinetics ຂອງ telmisartan ໂດຍສະເພາະກ່ຽວກັບ Cສູງສຸດທີ່ເຄຍ.
ການພົວພັນຢາ
Telmisartan ອາດຈະເພີ່ມຜົນກະທົບ hypotensive ຂອງຕົວແທນ antihypertensive ອື່ນໆ. ປະເພດອື່ນຂອງການໂຕ້ຕອບຂອງຄວາມ ສຳ ຄັນທາງຄລີນິກບໍ່ໄດ້ຖືກ ກຳ ນົດ.
ການໃຊ້ຮ່ວມກັນກັບ digoxin, warfarin, hydrochlorothiazide, glibenclamide, ibuprofen, paracetamol, simvastatin ແລະ amlodipine ບໍ່ໄດ້ ນຳ ໄປສູ່ການພົວພັນທີ່ ສຳ ຄັນທາງຄລີນິກ. ການເພີ່ມຂື້ນຢ່າງເດັ່ນຊັດຂອງຄວາມເຂັ້ມຂຸ້ນສະເລ່ຍຂອງ digoxin ໃນ plasma ໃນເລືອດໂດຍສະເລ່ຍ 20% (ໃນກໍລະນີ ໜຶ່ງ, 39%). ດ້ວຍການບໍລິຫານພ້ອມດຽວກັນຂອງ telmisartan ແລະ digoxin, ຄວນມີການ ກຳ ນົດແຕ່ລະໄລຍະໃນການ ກຳ ນົດຄວາມເຂັ້ມຂົ້ນຂອງ digoxin ໃນເລືອດ.
ດ້ວຍການໃຊ້ telmisartan ແລະ ramipril ພ້ອມໆກັນ, ການເພີ່ມຂື້ນ 2,5 ເທົ່າຂອງ AUC0-24 ແລະ Cmax ຂອງ ramipril ແລະ ramipril ໄດ້ຖືກສັງເກດເຫັນ. ຄວາມ ສຳ ຄັນທາງດ້ານຄລີນິກຂອງປະກົດການນີ້ຍັງບໍ່ທັນໄດ້ຖືກສ້າງຕັ້ງຂຶ້ນ.
ດ້ວຍການບໍລິຫານພ້ອມໆກັນຂອງຕົວຍັບຍັ້ງ ACE ແລະການກະກຽມ lithium, ການເພີ່ມຂື້ນຢ່າງສິ້ນເຊີງໃນຄວາມເຂັ້ມຂົ້ນຂອງ lithium ໃນເລືອດໄດ້ຖືກສັງເກດເຫັນ, ປະກອບດ້ວຍຜົນກະທົບທີ່ເປັນພິດ. ໃນກໍລະນີທີ່ຫາຍາກ, ການປ່ຽນແປງດັ່ງກ່າວໄດ້ຖືກລາຍງານກັບການບໍລິຫານຂອງ receptors angiotensin II antagonist. ດ້ວຍການບໍລິຫານພ້ອມໆກັນຂອງ lithium ແລະ angiotensin II receptor antagonists, ມັນໄດ້ຖືກແນະນໍາໃຫ້ກໍານົດຄວາມເຂັ້ມຂົ້ນຂອງ lithium ໃນເລືອດ.
ການຮັກສາດ້ວຍ NSAIDs, ລວມທັງກົດ acetylsalicylic, ຕົວຍັບຍັ້ງ COX-2, ແລະ NSAIDs ທີ່ບໍ່ເລືອກ, ສາມາດເຮັດໃຫ້ເກີດຄວາມຜິດປົກກະຕິຂອງ ໝາກ ໄຂ່ຫຼັງໃນຜູ້ປ່ວຍທີ່ຂາດນ້ ຳ. ຢາທີ່ປະຕິບັດໃນລະບົບ renin-angiotensin-aldosterone (RAAS) ອາດຈະມີຜົນກະທົບທີ່ເປັນເອກະພາບກັນ. ໃນຜູ້ປ່ວຍທີ່ໄດ້ຮັບ NSAIDs ແລະ telmisartan, bcc ຕ້ອງໄດ້ຮັບການຊົດເຊີຍໃນຕອນເລີ່ມຕົ້ນຂອງການຮັກສາແລະການເຮັດວຽກຂອງ ໝາກ ໄຂ່ຫຼັງທີ່ຖືກກວດສອບ.
ການຫຼຸດລົງຂອງຜົນກະທົບຂອງຕົວແທນຕ້ານການອັກເສບ, ເຊັ່ນ: telmisartan, ໂດຍຜ່ານການສະກັດກັ້ນຜົນກະທົບຂອງ vasodilating ຂອງ prostaglandins ໄດ້ຖືກສັງເກດເຫັນວ່າມີການຮ່ວມມືກັບ NSAIDs.
ປະລິມານຢາແລະການບໍລິຫານ
ຢາເມັດ Telmisartan ແມ່ນມີຈຸດປະສົງໃນການບໍລິຫານປາກປະ ຈຳ ວັນແລະກິນດ້ວຍແຫຼວ, ມີຫລືບໍ່ມີອາຫານ.
ການຮັກສາໂລກຄວາມດັນໂລຫິດແດງທີ່ ສຳ ຄັນ
ປະລິມານ ສຳ ລັບຜູ້ໃຫຍ່ທີ່ແນະ ນຳ ແມ່ນ 40 ມລກມື້ລະເທື່ອ.
ໃນກໍລະນີທີ່ຄວາມດັນເລືອດທີ່ຕ້ອງການບໍ່ບັນລຸໄດ້, ປະລິມານຂອງTelsartan®ສາມາດເພີ່ມສູງສຸດ 80 ມລກມື້ລະຄັ້ງ.
ໃນເວລາທີ່ເພີ່ມປະລິມານຢາ, ມັນຄວນຈະຖືກພິຈາລະນາວ່າຜົນກະທົບຕໍ່ຕ້ານໂຣກສູງສຸດແມ່ນບັນລຸໄດ້ຕາມປົກກະຕິພາຍໃນສີ່ຫາແປດອາທິດຫຼັງຈາກການເລີ່ມຕົ້ນການປິ່ນປົວ.
Telsartan®ສາມາດຖືກນໍາໃຊ້ໃນການປະສົມປະສານກັບ thiazide diuretics, ຍົກຕົວຢ່າງ, hydrochlorothiazide, ເຊິ່ງໃນການປະສົມປະສານກັບ telmisartan ມີຜົນກະທົບ hypotensive ເພີ່ມເຕີມ.
ໃນຜູ້ປ່ວຍທີ່ເປັນໂລກຄວາມດັນໂລຫິດແດງຢ່າງຮຸນແຮງ, ປະລິມານຂອງ telmisartan ແມ່ນ 160 ມລກ / ມື້ (ສອງເມັດຂອງTelsartan® 80 ມລກ) ແລະປະສົມກັບ hydrochlorothiazide 12,5-25 ມກ / ມື້ແມ່ນໄດ້ຮັບການຍອມຮັບໄດ້ດີແລະມີປະສິດຕິຜົນ.
ການປ້ອງກັນພະຍາດຫຼອດເລືອດຫົວໃຈແລະອັດຕາການຕາຍ
ປະລິມານທີ່ແນະ ນຳ ແມ່ນ 80 ມລກ 1 ເທື່ອ / ມື້.
ມັນຍັງບໍ່ທັນໄດ້ ກຳ ນົດວ່າປະລິມານທີ່ຕ່ ຳ ກວ່າ 80 ມລກມີປະສິດຕິຜົນໃນການຫຼຸດຜ່ອນການເປັນພະຍາດຫຼອດເລືອດຫົວໃຈແລະອັດຕາການຕາຍ.
ໃນໄລຍະເລີ່ມຕົ້ນຂອງການໃຊ້ຢາTelsartan® ສຳ ລັບການປ້ອງກັນພະຍາດຫຼອດເລືອດຫົວໃຈແລະອັດຕາການຕາຍ, ແນະ ນຳ ໃຫ້ຄວບຄຸມຄວາມດັນເລືອດ (BP), ແລະການປັບຄວາມດັນເລືອດກັບຢາທີ່ຊ່ວຍຫຼຸດຄວາມດັນເລືອດສູງກໍ່ອາດຈະມີຄວາມ ຈຳ ເປັນເຊັ່ນກັນ.
Telsartan®ສາມາດປະຕິບັດໄດ້ໂດຍບໍ່ສົນເລື່ອງອາຫານການກິນ.
ການປ່ຽນແປງຂອງຄົນເຈັບທີ່ມີຄວາມຜິດປົກກະຕິຂອງ ໝາກ ໄຂ່ຫຼັງແມ່ນບໍ່ ຈຳ ເປັນ, ລວມທັງຄົນເຈັບທີ່ເປັນໂຣກຕັບອັກເສບ. ມີປະສົບການທີ່ ຈຳ ກັດໃນການປິ່ນປົວຄົນເຈັບທີ່ເປັນໂຣກຫົວໃຈຊຸດໂຊມຮ້າຍແຮງແລະເປັນໂຣກຕັບແຂງ. ສຳ ລັບຄົນເຈັບດັ່ງກ່າວ, ແນະ ນຳ ໃຫ້ເລີ່ມຈາກປະລິມານທີ່ຕໍ່າກວ່າ 20 ມກ. Telsartan®ບໍ່ໄດ້ຖືກຍ້າຍອອກຈາກເລືອດໃນລະຫວ່າງການເປັນໂຣກເສັ້ນເລືອດ.
ໃນຄົນເຈັບທີ່ເປັນໂຣກຕັບອ່ອນເພຍເຖິງເບົາບາງສ່ວນ, ປະລິມານປະ ຈຳ ວັນບໍ່ຄວນເກີນ 40 ມລກມື້ລະເທື່ອ.
ການດັດປັບປະລິມານແມ່ນບໍ່ ຈຳ ເປັນ.
ການຈັດປະເພດ Nosological (ICD-10)
| ຢາຄຸມ ກຳ ເນີດ | 1 ແຖບ. |
| ສານທີ່ຫ້າວຫັນ: | |
| telmisartan | 40/80 ມກ |
| ຜູ້ຊ່ຽວຊານ: sodium hydroxide - 3.4 / 6.8 mg, povidone K30 (ນ້ ຳ ໜັກ ໂມເລກຸນຂະ ໜາດ ກາງ polyvinylpyrrolidone) - 12,24 ມກ, meglumine - 12/24 mg, mannitol - 165,2 / 330,4 mg, stearate ແມກນີຊຽມ - 2,4 / 4 , 8 mg, talc - 5/10 ມກ |
ຜູ້ຜະລິດ:
Severnaya Zvezda CJSC, ຣັດເຊຍ
ທີ່ຢູ່ທາງກົດ ໝາຍ ຂອງຜູ້ຜະລິດ:
111141, ມອດໂກ, Zeleny prospekt, ງ. ວັນທີ 5/12, ໜ້າ 1
ອ້າງເອົາການຜະລິດແລະທີ່ຢູ່ທີ່ຍອມຮັບ:
188663, ພາກພື້ນ Leningrad., ເມືອງ Vsevolozhsk, ການຕັ້ງຖິ່ນຖານຂອງຕົວເມືອງ Kuzmolovsky, ອາຄານ ສຳ ນັກງານເລກທີ 188
ການຖືພາແລະ lactation
ການນໍາໃຊ້ Telmisartan-SZ ແມ່ນ contraindicated ໃນລະຫວ່າງການຖືພາ. ເມື່ອບົ່ງມະຕິການຖືພາ, ຢາຄວນຢຸດທັນທີ. ຖ້າ ຈຳ ເປັນ, ການປິ່ນປົວທາງເລືອກອື່ນຄວນຖືກ ກຳ ນົດໄວ້ (ຫ້ອງຮຽນອື່ນຂອງຢາຕ້ານໂຣກຮໍໂມນທີ່ຖືກອະນຸມັດໃຫ້ໃຊ້ໃນເວລາຖືພາ).
ການນໍາໃຊ້ຂອງ ARA II ໃນໄລຍະ trimesters ທີສອງແລະທີສາມຂອງການຖືພາແມ່ນ contraindicated.
ໃນການສຶກສາ preclinical ຂອງ telmisartan, ຜົນກະທົບ teratogenic ບໍ່ໄດ້ຖືກກວດພົບ, ແຕ່ວ່າ fetotoxicity ໄດ້ຖືກສ້າງຕັ້ງຂຶ້ນ. ມັນເປັນທີ່ຮູ້ກັນວ່າການ ສຳ ຜັດກັບ ARA II ໃນຊ່ວງໄຕມາດທີສອງແລະທີສາມຂອງການຖືພາເຮັດໃຫ້ເກີດການເສື່ອມໂຊມຂອງຄົນໃນຮ່າງກາຍ (ການ ທຳ ງານຂອງ ໝາກ ໄຂ່ຫຼັງທີ່ຫຼຸດລົງ, oligohydroamnion, ການຫົດຕົວຂອງກະໂຫຼກທີ່ຊັກຊ້າ), ເຊັ່ນດຽວກັນກັບຄວາມເປັນພິດຂອງໂຣກ neonatal (ຄວາມລົ້ມເຫຼວຂອງຫມາກໄຂ່ຫຼັງ, ໂຣກເສັ້ນເລືອດແດງ, hyperkalemia). ຄົນເຈັບທີ່ວາງແຜນການຖືພາຄວນໄດ້ຮັບການປິ່ນປົວດ້ວຍທາງເລືອກ. ຖ້າການຮັກສາຂອງ ARA II ເກີດຂື້ນໃນຊ່ວງໄຕມາດທີສອງຂອງການຖືພາ, ມັນໄດ້ຖືກແນະ ນຳ ໃຫ້ປະເມີນການເຮັດວຽກຂອງ renal ແລະສະພາບຂອງກະໂຫຼກໃນລູກໃນທ້ອງໂດຍ ultrasound.
ເດັກເກີດ ໃໝ່ ທີ່ແມ່ຂອງພວກເຂົາໄດ້ຮັບ ARA II ຄວນໄດ້ຮັບການຕິດຕາມກວດກາຢ່າງໃກ້ຊິດກ່ຽວກັບການເຮັດວຽກຂອງເສັ້ນເລືອດໃນເສັ້ນເລືອດແດງ.
ການປິ່ນປົວດ້ວຍ Telmisartan-SZ ແມ່ນ contraindicated ໃນໄລຍະໃຫ້ນົມລູກ.
ການສຶກສາກ່ຽວກັບຜົນກະທົບຂອງການຈະເລີນພັນບໍ່ໄດ້ຖືກ ດຳ ເນີນ.